Clear Sky Science · he
פרוטאזות התלויות ב-K48-אוביקוויטין חותכות חלבונים לאחר ה-ER
איך התאים מחליטים אילו חלבונים להרוס
התאים שלנו מסלקים כל העת חלבונים בלויים או פגומים, במיוחד כאלה הטמונים בממברנות ומשמשים כשערים וחיישנים. המאמר הזה חושף שהתאים משתמשים בתווית זעירה בשם אוביקוויטין לא רק כ"תווית זבל" כללית, אלא כקוד שמציין לחלבוני ממברנה בדיוק כיצד הם יפורקו. הבנת הקוד הזו מסייעת להסביר כיצד התאים שומרים על בריאותם ועלולה להנחות טיפולים עתידיים שמכוונים להשמיד באופן מכוון חלבונים הגורמים למחלות.
ברקוד תאי להשלכת חלבונים
התאים מעטרים חלבונים לא רצויים בשרשראות של חלבון קטן הנקרא אוביקוויטין. השרשראות הללו יכולות להיות מקושרות בדרכים שונות, בדומה לחרוזים המחוברים דרך חורים שונים, וכל דפוס יכול לסמן גורל שונה. המחברים התמקדו בחלבוני ממברנה שכבר עזבו את הרשת האנדופלסמית (ER) ונעים דרך קומפרטמנטים כגון הגולג'י ואנדוזומים. הם שאלו האם שני סוגי השרשראות הנפוצים, K48 ו-K63, הם תוויות ניתנות להחלפה או שמא הם מכוונים את המטען לנתיבי השמדה שונים.
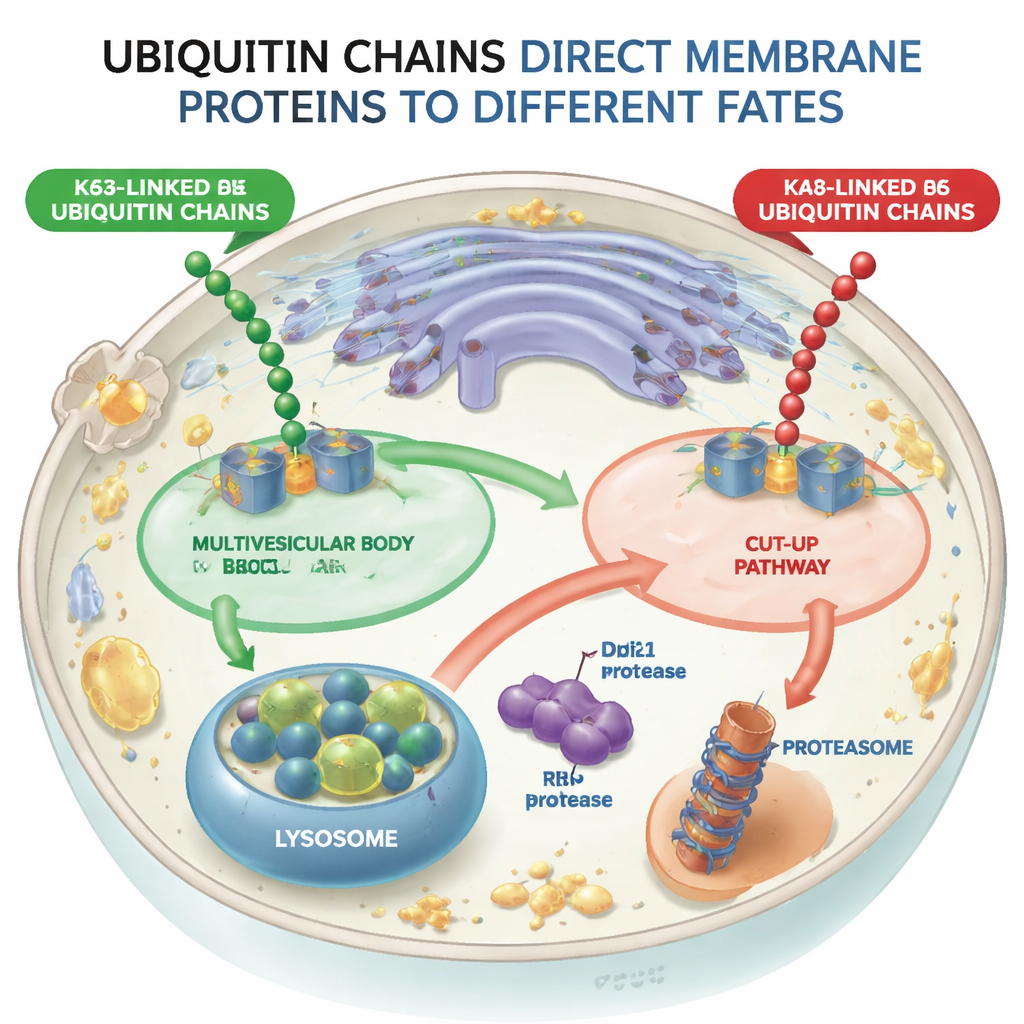
שני מסלולים המתפצלים לחלבונים מתוייגים
בעזרת תאי שמרים כמודל, החוקרים תכננו מכונת מולקולות (ליגזות אוביקוויטין) שיכולה לצרף לשרשרת מבחן אחת של חלבון ממברנה — קולטן מיון בשם Vps10 — או שרשראות K48 או K63. כאשר Vps10 קיבל שרשראות K63, נשלח לתוך הווסיקולות הפנימיות שבתוך האנדוזומים — מבנים הידועים כגופיפי וריקולות מרובות (multivesicular bodies) — שאחר כך מתמזגים עם הליזוזום, תא הקיבול החסר. לעומת זאת, כש-Vps10 נשא שרשראות K48, הוא לא עבר דרך מרובת הווסיקולות. במקום זאת פורק בדרך שונה לחלוטין, דבר שמראה שהתא מבחין בין שני סוגי השרשראות ושהמסלול המולטי-ווסיקולרי דוחה באופן יעיל מטען המסומן ב-K48.
מסלול "חתוך-וקטע" שמחלק חלבונים לשניים
הצוות גילה ששרשראות K48 מעוררות מסלול חיתוך חלבונים שהם מכנים CUT-UP, קיצור של Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. במקום לגרוף את כל החלבון החוצה מהממברנה בבת אחת, CUT-UP חותך אותו לחתיכות שמסתיימות בהשמדה על ידי מערכות הסילוק הקיימות בתא. אנזים מרכזי, Ddi1, שוחים בציטוזול וחותכים את החלק של חלבון הממברנה הפונה לציטוזול. אותו קטע מעובד לאחר מכן על ידי הפרוטאוזום, המטחנת החלבונים הראשית של התא. במקביל, אנזים אחר, Rbd2, יושב בממברנה עצמה וחותך את החלק של החלבון הפונה לחלל הקומפרטמנט, ומשחרר אותו לחלל שמוביל בסופו של דבר לליזוזום. חסימת Ddi1, Rbd2, הפרוטאוזום ואנזימי הליזוזום יחד הייתה נחוצה כדי להגן באופן מלא על Vps10 המסומן ב-K48 מפירוק, ובכך לאשש שכל הרכיבים הללו משתפים פעולה במסלול CUT-UP.
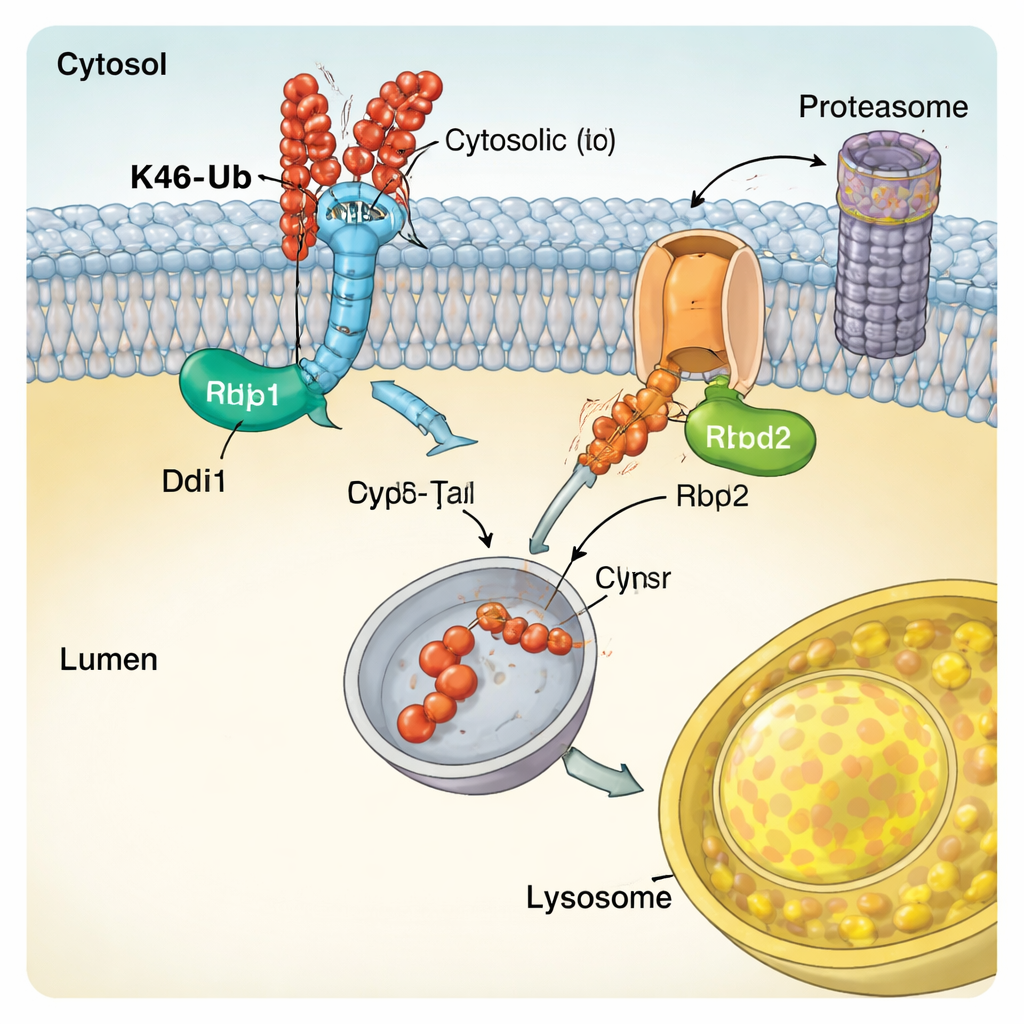
אנזימים מתמחים שקוראים את קוד האוביקוויטין
כדי להבין כיצד CUT-UP מזהה את מטרותיו, המחברים בחנו את התכונות המולקולריות של Ddi1. הם הראו שהגרעין הקטליטי המרכזי של Ddi1 לא רק חותך חלבונים אלא גם יכול לקשור אוביקוויטין ישירות, ושהפעילות שלו ממותנת על ידי אזורים נוספים שנצמדים לשרשראות אוביקוויטין. Ddi1 הראה תלות ייחודית בשרשראות מסוג K48, המתאימה לתפקידו ב-CUT-UP. Rbd2, לעומת זאת, הוא פרוטאזה רמבווידית שחוצה את הממברנה. המחקר מצא שהאתר הפעיל של Rbd2 חיוני לחיתוך החלקים של Vps10 הפונים ללומן ושהאסנזים נודד דרך מספר קומפרטמנטים סקרטוריים, מה שמאפשר לו לפעול במיקומים תאיים מרובים. אנזימים דומים קיימים בתאים אנושיים וקושרו למצבים הנעים מניורודגנרציה ועד סרטן, מה שמציע שמנגנוני CUT-UP דומים עשויים להיות חשובים במגוון רחב של מצבים.
מדוע זה חשוב לבריאות ולטיפול
בהדגשה שלפיה סוגי שרשראות אוביקוויטין שונים שולחים את אותו חלבון ממברנה לגורלות נבדלים — או למיון דרך גופיפי וריקולות מרובות או לחיתוך באמצעות CUT-UP — עבודה זו מספקת ראיה חזקה שהתאים משתמשים ב"קוד אוביקוויטין" ממשי כדי לכייל את הסילוק החלבוני. הגילוי של CUT-UP מבהיר כיצד חלבוני ממברנה עקשנים יכולים להיות מפורקים חתיכה אחר חתיכה ומדגיש את Ddi1 ו-Rbd2 כשחקנים מרכזיים שקוראים ומאכפים את הקוד הזה. עבור קהל שאינו מומחה, המסקנה היא שהתאים אינם פשוט מסמנים חלבונים כזבל; הם מציינים גם כיצד הזבל יוסר. ככל שמפתחי תרופות מעצבים כלים שמצמידים אוביקוויטין לחלבונים מזיקים כדי להסירם, הבנת מסלולים כמו CUT-UP תהיה חיונית כדי לחזות אילו שברים יווצרו ואיך זה עלול להשפיע על התנהגות התא.
ציטוט: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
מילות מפתח: קוד האוביקוויטין, דעיכת חלבונים, חלבוני ממברנה, פרוטאוזום, ליזוזום