Clear Sky Science · he
RNA saVPg מהונדס משיג הצפנה מדויקת של חלבונים טיפוליים בחי ללא תלות ב׳כיפה׳ ובדלקתיות נמוכה
שכתוב החוקים לתרופות RNA
חיסונים מבוססי RNA שליח (mRNA) סייעו לשנות את מהלך מגפת הקורונה, אך שימוש במולקולות דומות להחלפה או להשלים חלבונים חסרים במחלות כרוניות קשה הרבה יותר. הגוף נוטה לפרק RNA זר במהירות ולהפעיל תגובות חיסוניות חזקות, ועיצובי RNA מתעצם עצמי רבים עלולים לעשות שגיאות בעת שכפולם. המחקר מתאר סוג חדש של RNA מתעצם עצמי — מבוסס מרכיבים של נורו-וירוס אנושי — שהונדס להיות עמיד יותר לאורך זמן, פחות דלקתי ובעל דיוק יוצא דופן, מה שפותח דלת לתרופות RNA מדויקות ועמידות יותר.
RNA מעתיק-עצמו חכם יותר
תרופות mRNA מסורתיות נושאות מתכון יחיד לחלבון ונקראות בידי התא פעם אחת לפני פירוקן. RNA מתעצם עצמי (saRNA) כולל מכונות ויראליות נוספות שמאפשרות ל-RNA לשכפל את עצמו בתוך תאים, ובכך להגביר משמעותית את התפוקה ממנה בנפח מינימלי. מערכות saRNA הנחקרות ביותר מקורן באלפא-וירוסים, אך הן גדולות, מפעילות הגנות אנטיוויראליות חזקות ושוכפלות בפחות דיוק. החוקרים פנו במקום זאת לנורו-וירוס האנושי, גורם שכיח ל׳שפעת הקיבה׳. הם בודדו מקטע קומפקטי של חומר גנטי מנורו-וירוס ובנו אותו כנשא לגנים טיפוליים. בלב העיצוב עומד VPg, חלבון ויראלי קטן הקשור כימית לקצה הקדמי של ה-RNA. VPg מחליף את מבנה ה״כיפה״ הרגיל הנמצא על mRNA אנושי ומאפשר לתרגום ה-RNA להיעשות על ידי מערך גורמי תרגום שונים, שפחות רגישים לאותות לחץ מסוימים. 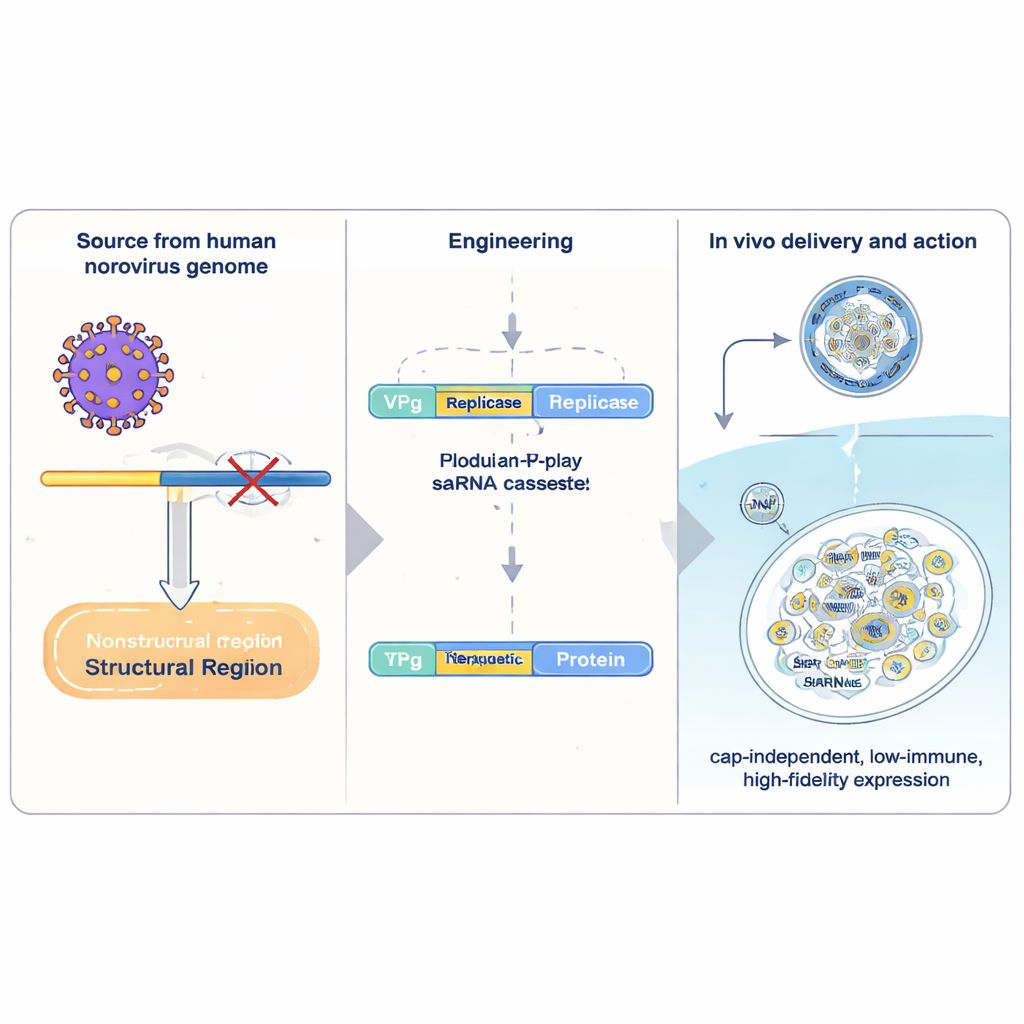
דיוק גבוה בלי עוררות יתר של המערכת החיסונית
לתרופות חלבון, הדיוק חשוב: אפילו שגיאות שכפול קטנות יכולות לשנות את התנהגות התרופה או ליצור תוצרי לוואי רעילים. הצוות הראה שכאשר VPg מנורו-וירוס נקשר לאנזים השכפול של ה-RNA (פולימראז), הוא מאט את קצב הוספת רכיבי הבנייה השגויים, מה שמפחית בחדות את שיעור השגיאות. הם זיהו חומצות אמינו ספציפיות ב-VPg שמקשרות לאזור בקרה מרכזי בפולימראז והדגימו כי הפרעה בממשק זה מפחיתה את הדיוק. במקביל, עיצובים קלאסיים של saRNA מייצרים כמות גדולה של RNA דו-גדילי, פעמון אזעקה מולקולרי שמפעיל הגנות אנטיוויראליות ומשבית את ייצור החלבון. באמצעות שכתוב הפולימראז כך שיועדף צורה התחלתית אחת המחוברת ל-VPg ובאמצעות ארגון מחדש של הגנום כך שרק הגדיל הטיפולי מיוצר ביעילות, המחברים הקטינו משמעותית את יצירת ה-RNA הדו-גדילי. הם כיווננו גם אזור זנב ב-RNA כך ש-VPg יתחבר באתר הנכון, למניעת קטעים קצרים בלתי מכוונים שיכולים לתרגם לפפטידים מקריים.
עובד במקום שבו mRNA סטנדרטי נכשל
ה-saRNA המבוסס על VPg נבחן בהקשרים מחלה תובעניים שבהם mRNA מצופה בכיפה מתקשה. בקאקסיה קשורה בסרטן — תסמונת בזבוז שבה שרירים ושומן נעלמים — גורמי תרגום מרכזיים המזהים את כיפת ה-mRNA הרגילה מושתקים, מה שהופך mRNA תלוי-כיפה ליעיל פחות. מכיוון ש-VPg משתמש בנקודת כניסה חלופית למכונת התרגום של התא, הוא המשיך להניע ייצור של ההורמון גרלין המעורב בתיאבון ובמטבוליזם במודל עכבר של סרטן הלבלב. הזרקות נמוכות-מינון חודשיות סייעו לשמר שריר ושומן, שיפרו צריכת מזון ומטבוליזם והאריכו בשיעור מתון את ההישרדות, ללא רעליות נראית או סימני הפעלה חיסונית כרונית.
התקפה סרטנית מדויקת ואוטואימוניות מרוככת
כדי לבדוק האם שכפול בעל-דיוק באמת חשוב, החוקרים טעינו את וקטור ה-VPg בבניין אונקוליטי מורכב, GSDMDENG, שמיועד ליצור חורים במיטוכונדריה של תאי סרטן ולגרות תגובות חיסוניות ספציפיות לגידול. כאשר אותו מבנה הומצל על saRNA קונבנציונלי של אלפא-וירוס, מוטציות הצטברו בסבבים חוזרים של שכפול וחלשונו את יכולות ההרג הסלקטיבי של תאים סרטניים ואת האפקט הפריימינג האימונולוגי. לעומת זאת, מערכת ה-VPg שמרה על הרצף המיועד, ייצרה הרג חזק של תאי גידול וגרמה לתגובות תאי T עמידות שהאטו או מנעו סרטן לבלב במודלים של עכברים. לבסוף, הם יישמו saRNA מבוסס VPg לאתגר שונה: מחלת השתל-נגד-המאחסן כרונית, שבה תאי חיסון תוקפים את הריאות לאחר השתלת מח עצם. saRNA עם קוד ל־protein C מיועד הפעיל הפחית היווצרות נוגדנים מזיקים, מנע צלקות ריאתיות ושיפר נשימה בעכברים, בעוד מבנה דומה מבוסס אלפא-וירוס עורר חיסון מולד חזק יותר והחריף את התוצאים.
למה זה חשוב עבור תרופות RNA בעתיד
ביחד, העבודה מציגה פלטפורמת RNA קומפקטית, "פלאג-אונד-פליי", שמחברת שלוש תכונות רצויות: היא משכפלת את עצמה בדיוק גבוה, מעוצבת למזער אזעקות חיסוניות ומעקפת צווארי בקבוק שמגבילים תרגום של mRNA סטנדרטי. מאחר שהגן הטיפולי מוחלף בפשטות בגב של נורו-וירוס קבוע, ניתן לבחון חלבונים שונים — מהורמונים ועד ויסותי קרישה וסוכני אונקוליזה — על אותו שלד. למרות שעוד נדרשת עבודה רבה לפני שימוש בבני אדם, גישת ה-saRNA עם VPg מציעה דרך לעבר תרופות RNA המתנהגות יותר כמו עירויי חלבון יציבים: מינון נמוך, משך פעולה ארוך יותר ומתואמות לפעול גם ברקמות חולות שבהן הודעות mRNA רגילות אינן נקראות באופן אמין. 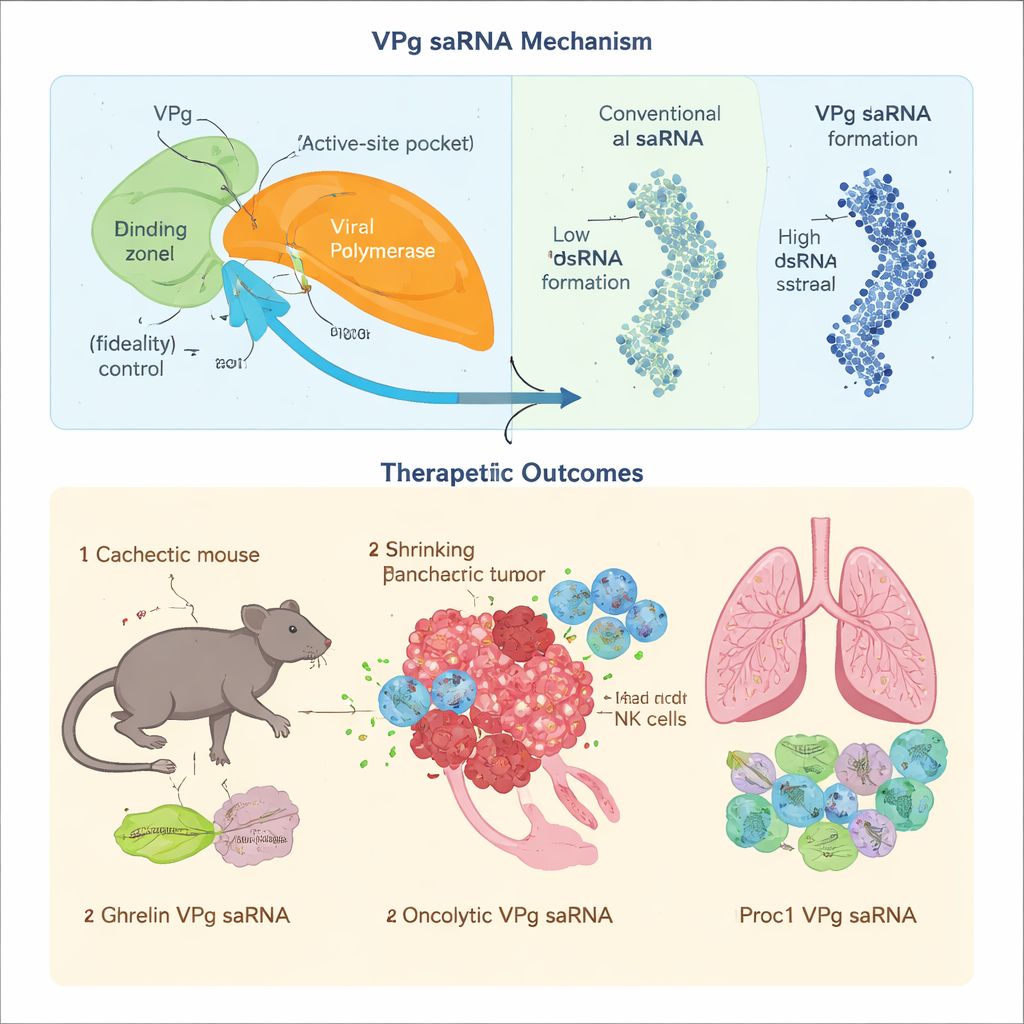
ציטוט: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
מילות מפתח: RNA מתעצם עצמי, תרופות mRNA, VPg מנורו-וירוס, קאקסיה סרטנית, מחלת השתל-נגד-המאחסן