Clear Sky Science · he
התפקיד של רצפים חוזרים בעלי מורכבות נמוכה באינטראקציות RNA–RNA ומסגרת למידה עמוקה לחיזוי דופלקסים
רצפי RNA דביקים שמעצבים את התנהגות התא
בתוך כל תא, מולקולות RNA נתקלות זו בזו ללא הרף, יוצרות שותפויות חולפות שעוזרות לשלוט באילו גנים מופעלים, כיצד מיוצרים חלבונים וכיצד התאים מתפתחים. המחקר הזה מגלה שרבים מהמגעים האלה בין RNA–RNA אינם מקריים: הם מונחים על ידי רצפים קצרים, פשוטים וחוזרים שמדמים סוג של וולקרו מולקולרי. החוקרים גם פיתחו כלי בינה מלאכותית שיכול לזהות היכן זוגות RNA כאלה צפויים להיווצר, ופותח דרכים חדשות לחקור כיצד תאים פועלים בבריאות ובמחלות.
רצפים פשוטים עם השפעות עוצמתיות
לעתים מתארים את ה‑RNA כשליח שנושא מידע גנטי מה‑DNA לחלבונים, אך הוא גם משמש כשלד, כווסת וכמדריך. רבות מהפעילויות האלה תלויות בקשירה של שתי גדילים של RNA זו לזו. על ידי שילוב נתונים ממספר מחקרים ניסיוניים רחבי היקף בתאים אנושיים ועכבריים, המחברים מראים שהאזורים ב‑RNA שמתקשרים בפועל בקשירה כאלה מעושרים במידה רבה במה שהם קוראים לו רצפים חוזרים בעלי מורכבות נמוכה. אלה מקטעים הבנויים ממוטיבים קצרים — למשל רצפים של בסיסי G ו‑C — שחוזרים שוב ושוב. במקום להיחשב כ"זבל" גנומי, מקטעים חוזרניים אלה מתגלים כמקומות עגינה עיקריים שבהם RNA אחד יכול להיצמד לרבים אחרים, וליצור מרכזי אינטראקציה צפופים ברחבי הטרנסקריפטום. 
מרכזי RNA לפיתוח ולויסות
כאשר הצוות חקר אילו גנים נושאים את אתרי המגע העשירים ברצפים חוזרים אלה, הופיעה תבנית בולטת: רבים מהם מקודדים חלבונים השולטים בהתפתחות ובזהות התא, כגון גורמי שעתוק. אפילו בקו־תאי סרטני שאינו מנוון באופן פעיל, ה‑RNAs הקשורים לתוכניות התפתחותיות היו מעורבים במידה ניכרת במגעים מבוססי‑חזרות. המחברים גם בחנו בקפידה RNAים לא מקודדים ארוכים (lncRNAs), מולקולות RNA שאינן מקודדות לחלבונים אך לעתים קרובות מווסתות אותם. לדוגמה, מטרות ה‑lncRNA TINCR ולמחלקה נוספת של lncRNA החשובה ליצירת תאי עצב מוטוריים, Lhx1os, הציגו שפע מיותר של חזרות משלימות. במקרים אלה, חזרות פשוטות על ה‑lncRNA מוצאות התאמה בחזרות משלימות ב‑RNAs שותפים, מה שמאפשר קשירות יציבה שיכולה לעזור לכוונן רמות או תרגום של גנים התפתחותיים מרכזיים.
איפה חלבונים וערכיי עריכה מצטרפים
מגעי RNA המונעים על‑ידי חזרות אלה נדירים שפועלים לבד. המחברים חיפו מפות קשירה של חלבונים על גבי נתוני האינטראקציה שלהם ומצאו שרבים מאתרי המגע הנושאים חזרות גם מזוהים על‑ידי חלבוני‑קשירה של RNA שמעורבים בשליטה על תרגום, בשקיעת RNA וביצירת גרנולות ציטופלזמטיות כגון P‑bodies ו‑stress granules. חלבון אחד בפרט, STAU1, שיכול לעורר השמדה של מטרות ה‑RNA שלו, נקשר לעיתים קרובות לדופלקסים שנוצרים באמצעות רצפים חוזרים בעלי מורכבות נמוכה. דיכוי STAU1 הוביל לרמות גבוהות יותר של RNAים המעורבים בדופלקסים אלה, במיוחד אלה הנושאים חזרות, מה שמרמז שקשירת RNA המוּסרת על‑ידי חזרות יכולה לסמן תמלילים להרס מבוקר. אותם אזורים עשירים בחזרות גם מושכים אנזימי עריכת RNA כגון ADAR1, שמבצעים שינוי כימי בבסיסים ספציפיים בתוך RNA דו‑גדילי, וכך מרמזים שרצפים חוזרים בעלי מורכבות נמוכה מסייעים למקם את אתרי העריכה שמכיוונים את התנהגות ה‑RNA.
להורות לרשת עצבית לקרוא מגעי RNA
תוכניות מחשב סטנדרטיות מנסות לחזות קשירה בין RNA–RNA בעיקר על סמך יציבות תרמודינמית — כמה אנרגיה יידרש כדי ליצור או לשבור דופלקס. למרות התועלת שלהן, המודלים האלה מפספסים לעתים קרובות אינטראקציות אמיתיות הנצפות בתאים, במיוחד בין RNAs ארוכים. כדי לצאת מעבר לכללי האנרגיה הפשוטים, המחברים אימנו מודל למידה עמוקה בשם RIME שמשתמש בהטמעות בסגנון "מודל שפה": ייצוגים נומריים של רצפי RNA שמקודדים דפוסים שנלמדו ממאגרי נתוני חומצות גרעין עצומים. RIME הוצג עם זוגות מקטעי RNA ולמד לסווג האם הם מבצעים אינטראקציה, תוך שימוש בהרבה זוגות אמיתיים מניסויים מבוססי‑פסורלן כדוגמאות חיוביות וזוגות לא אינטראקטיביים שנבנו בקפידה כדוגמות שליליות. 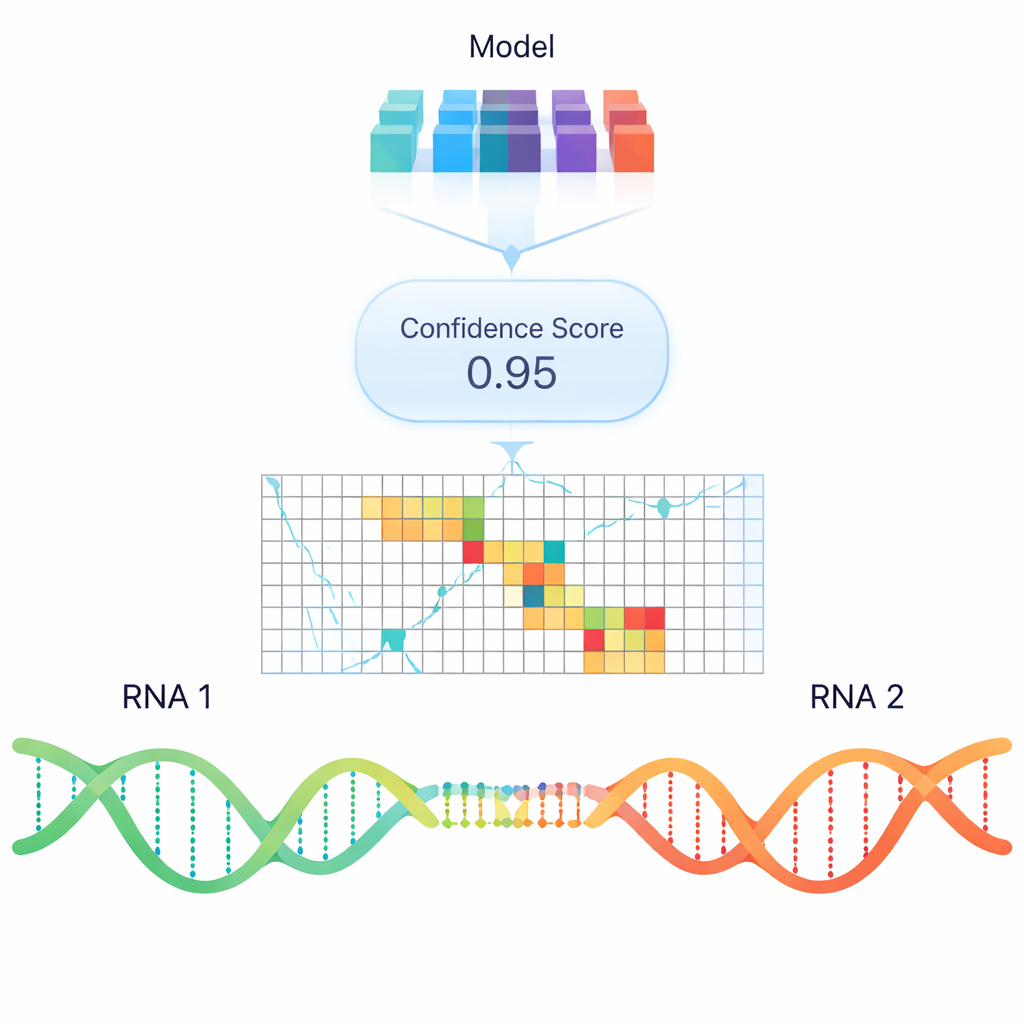
חיזויים חכמים יותר ורמזים ביולוגיים חדשים
כאשר הושווה לכלי מובילים מבוססי תרמודינמיקה ולשיטה נוספת של רשת עצבית, RIME הראה ביצועים טובים יותר בעקביות בהבחנה בין מגעי RNA–RNA אמיתיים לדקוי, במיוחד עבור אינטראקציות ניסיוניות בעלות ודאות גבוהה. הוא לא רק מנבא האם שני RNAs ידבקו זה לזה, אלא גם נוטה להדגיש את האזורים המדויקים המעורבים, והוא לומד באופן טבעי כי רצפים חוזרים בעלי מורכבות נמוכה הם מנבאים חזקים למגע. באופן מרשים, אותו מודל, שאומן רק על אינטראקציות בין RNAs שונים, עובד היטב גם לחיזוי קשרים פנימיים של בסיסים בתוך מולקולת RNA אחת, בהתאמה עם ניסויי מבנה ואלגוריתמי קיפול קלאסיים. עבור ויסותים לא מקודדים כמו TINCR, NORAD ו‑SMaRT, RIME מגלש בהצלחה אתרי אינטראקציה פונקציונליים ידועים ומציע אזורים מועמדים נוספים.
למה זה חשוב
לקורא שאינו מומחה, המסר המרכזי הוא שרצפים קצרים וחוזרים ב‑RNA — שלפני כן ניתן היה להזניחם כרעשים חסרי תכלית — פועלים כנקודות חיבור מרכזיות במפה האלקטרית של אינטראקציות ה‑RNA בתא. הם מסייעים לקבץ RNAs יחד, מזמינים חלבוני ויסות ואנזימי עריכה, ומשתמשים בהם במידה רבה במסלולים ששולטים כיצד תאים מתפתחים ומגיבים ללחץ. מודל RIME החדש נותן לחוקרים כלי עוצמתי לסרוק גנומים אחר שותפויות RNA–RNA אלה, כולל כאלו שעשויות להשתבש במחלות נוירולוגיות ואחרות הקשורות להתרחבות חזרות. במהותו, עבודה זו מראה כי הבנה — וחיזוי — של האופן שבו חזרות פשוטות של RNA נדבקות זו לזו יכולה לחשוף שכבות נסתרות של ויסות גנים.
ציטוט: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
מילות מפתח: אינטראקציות RNA–RNA, רצפים חוזרים בעלי מורכבות נמוכה, RNA לא מקודד ארוך, למידה עמוקה, ויסות גנים