Clear Sky Science · he
הפחתה של תאי אפיתל אלוואולריים בינוניים מודרכת על‑ידי חתימת טרנסקריפטום משפרת פיברוזיס ריאתי בעכברים
מדוע צלקות בריאות חשובות
פיברוזיס ריאתי הוא מחלת ריאות חמורה שבה שקיות האוויר העדינות הופכות בהדרגה לרקמת צלקת נוקשה, מה שהופך כל נשימה למאמץ. הרופאים יודעים שהצטלקות זו מתחילה כאשר תהליכי התיקון הרגילים יוצאים מאיזון, אך לא היה ברור אילו תאים ספציפיים אשם וכיצד להסירם מבלי לפגוע ברקמת ריאה בריאה. מחקר זה בוחן שיטה חדשה ל"קריאת" המסרים המולקולריים בתוך תאי הריאה, שימוש במידע הזה לזיהוי תאים בינוניים מזיקים, והשמדה סלקטיבית שלהם כדי להפחית צלקת בעכברים.
תאים שנתפסו בתהליך תיקון לקוי
לאחר פגיעה בריאה, תאים מיוחדים המייצרים חומצות שטח הנקראים תאי סוג II בדרך כלל מתחלקים ואז מבשילים לתאי סוג I דקיקים שמצפים את שקיות האוויר ומאפשרים לחמצן לעבור לדם. בפיברוזיס, רבים מהתאים הללו נתקעים במצב ביניים או טרנסיציונלי במקום להשלים את המסלול הזה. מחקרים קודמים בריצוף RNA בתא יחיד מצאו את התאים הבינוניים הללו הן בעכברים והן בבני אדם, אך לא היה ברור האם הם רק עדים או הנהגים המרכזיים של המחלה. המחברים התמקדותו בסוג תאי ביניים עכברי הנקרא Krt8+ alveolar differentiation intermediates, ובמקבילים האנושיים שלהם הידועים כ־aberrant basaloid cells, הנמצאים בכמויות גבוהות בריאות פגועות.
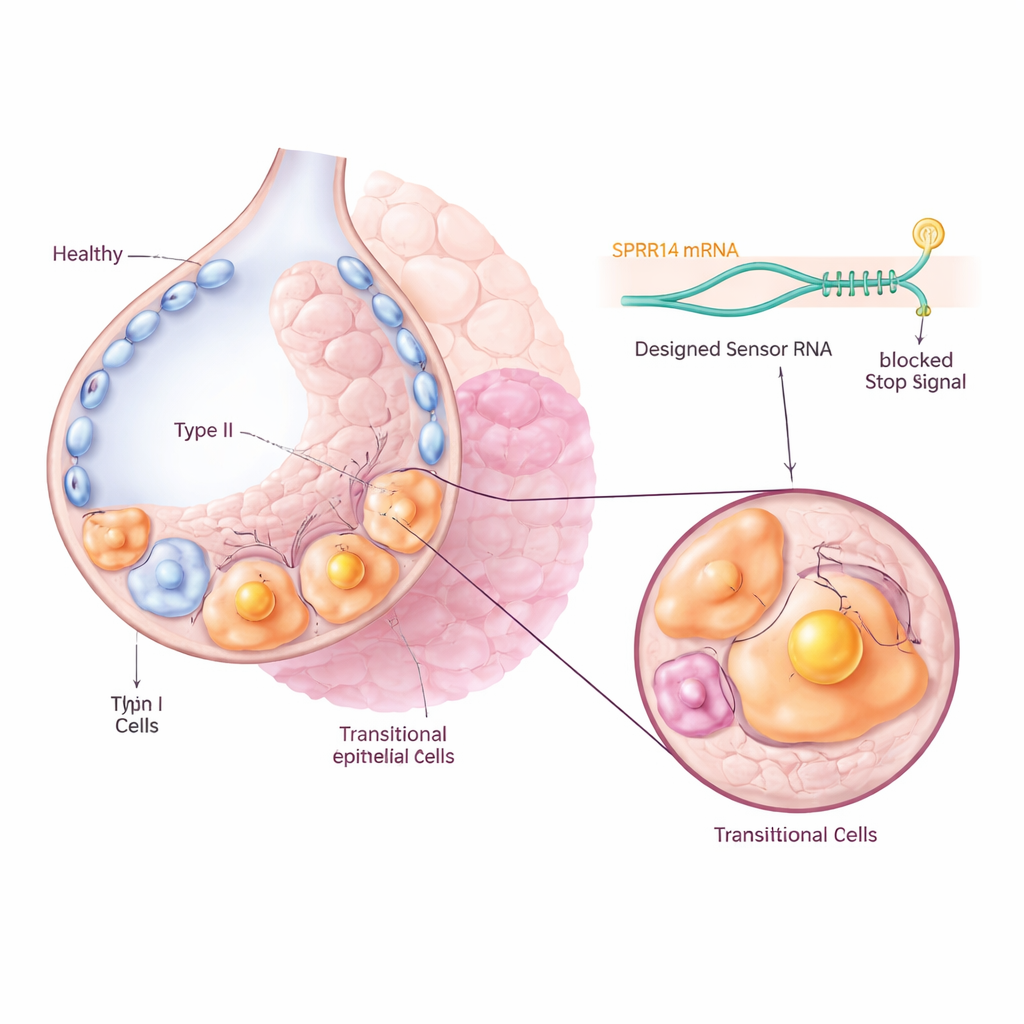
מציאת תג זיהוי מולקולרי ייחודי
כדי ליעד את התאים הבעייתיים מבלי לגעת בשכנים הבריאים, הצוות חיפש תחילה במאגרי ביטוי גנים גדולים סימן שהיה מופעל בעוצמה ובאופן ספציפי באוכלוסיית הביניים. הם זיהו מולקולה בשם SPRR1A כ"תג שם" בולט: היא הועשרה מאוד בתאי Krt8+ הבינוניים בריאות פיברוטיות של עכברים, ובתאי KRT5-/KRT17+ aberrant basaloid של חולים עם פיברוזיס אידיופתי ריאתי, אך נעדרה ברוב התאים בריאים. מיקרוסקופיה של רקמות ריאה גם מעכבר וגם מאדם אישרה כי SPRR1A הופיעה בעיקר באזורים פגועים ומשופצים ולא בשקיות האוויר הבריאות, מה שמרמז שהיא עשויה לשמש כידית מדויקת לזיהוי התאים האשמים.
תכנות תאים עם חיישן RNA
החוקרים השתמשו אז בטכנולוגיה שפותחה לאחרונה בשם CellREADR, שפועלת כחיישן מולקולרי פנימי. הם תכננו רצפי RNA קצרים שיכולים לזווג בסיסים עם RNA של SPRR1A בתא. כאשר החיישן מזהה SPRR1A, הוא מפעיל את ייצורו של חלבון "אפקטור" מצורף, כמו תג זוהר או קולטן שהופך את התא לרגיש לתרופה. בעכברים השתמשו בנגיפים כדי למסור את מבני החיישן–אפקטור לתאי הריאה. רק תאים שמייצרים באופן פעיל SPRR1A הפעילו את האות הזוהר, מה שאפשר לצוות לעקוב ולהפריד תאים טרנסיציונליים ישירות מריאות פיברוטיות. ריצוף תא יחיד הראה שהתאים המסומנים התאימו בצמוד לחתימת הגנים הידועה של תאים בינוניים, ואישר שהחיישן RNA כיוון במדויק לאוכלוסייה המיועדת.
כיבוי התאים הביניים המזיקים
בהמשך הוחלף האפקטור מחלבון זוהר חסר פגע לקבלן רעלן דיפטריה, כך שניתן היה להרוג מבחינה סלקטיבית תאים חיוביים ל‑SPRR1A באמצעות מתן רעלן דיפטריה. על־ידי תזמון הטיפול לשיא שפעם של התאים הביניים לאחר פגיעה כימית בריאה, הצליחו המחברים להסיר בערך שליש מהאוכלוסייה הזו. דילול ממוקד זה הוביל לפחות צלקת ריאה באופן בולט: נצפתה הפחתה בהצטברות קולגן, רמות נמוכות יותר של חלבונים פיברוטיים ומבני שקיות אוויר שנראים תקינים יותר. ניתוחים מפורטים הראו שרוב התאים החיוביים ל‑SPRR1A נשאו סימנים של מצב מותש בדומה להזדקנות, עם תת־קבוצה קטנה בעלת יכולת החלוקה גבוהה, מה שמרמז שהתאים הביניים הללו גם נכשלים לתקן את הרקמה כראוי וגם מסייעים לשמור על התהליך הפיברוטי.
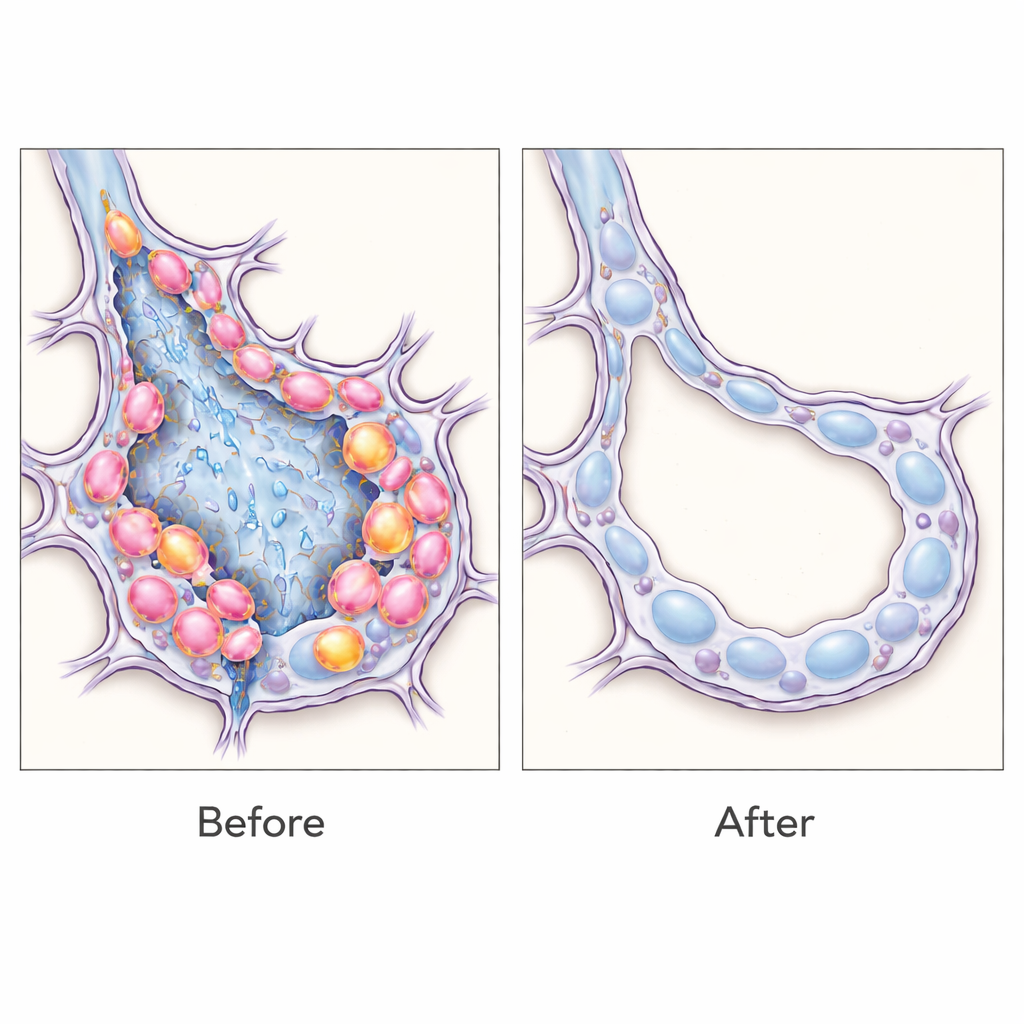
מה זה אומר על טיפולים עתידיים
ממצאים אלה תומכים ברעיון שתאי אפיתל טרנסיציונליים אינם רק סמנים אלא מניעים פעילים של פיברוזיס ריאתי, וכי הסרתם הסלקטיבית יכולה להחזיר את האיזון לעבר מבנה ריאה בריא יותר בעכברים. באופן רחב יותר, העבודה מדגימה אסטרטגיה גמישה: על‑ידי "קריאת" חתימות RNA ספציפיות לתאים, חוקרים יכולים לתייג, לחקור ואפילו להשמיד אוכלוסיות תאים מוגדרות במדויק ברקמה חיה בלי ליצור בכל פעם זני בעלי חיים מותאמים אישית. למרות שעוד דרוש הרבה עבודה לפני שכלי חישה מבוססי RNA כאלה יוכלו להיות מותאמים בבטחה לאנשים, גישה זו פותחת דרך לטיפולים ממוקדי־דיוק שפועלים נגד סוגי התאים המדויקים שמפריעים לריפוי בצלקת ריאות כרונית ובמחלות פיברוטיות אחרות.
ציטוט: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
מילות מפתח: צלקת ריאות, תאי אפיתל אלוואולריים, ריצוף RNA בתא יחיד, טכנולוגיית חישה של RNA, הזדקנות תאית