Clear Sky Science · he
אטלס גרעיני יחיד של האמיגדלה המרכזית חושף דינמיקות כרומטין ותעתוק גנים בהפרעת שימוש באלכוהול בבני אדם
מדוע המחקר הזה משמעותי לחיי היומיום
הפרעת שימוש באלכוהול (AUD) פוגעת במיליונים ובמשפחותיהם, ובכל זאת ידוע לנו באופן מפתיע מעט לגבי מה ששתייה כבדה ממושכת עושה למוח האנושי ברמת התאים הבודדים. המחקר הזה מתמקד באזור קטן אך קריטי — האמיגדלה המרכזית, צומת למחשבה של פחד, לחץ ומוטיבציה — וממפה כיצד אלכוהול מעצב מחדש תאי מוח ומערכות הבקרה הגנטיות שלהם. על ידי שילוב שיטות רצף "תא-בודד" חדישות עם מחקרים גנטיים על סיכון להתמכרות, החוקרים מתחילים להסביר מדוע חלק מהאנשים נוטים יותר ל-AUD ואיך אלכוהול משאיר צלקות מולקולריות מתמשכות במוח.
מבט קרוב על צומת מוח זעיר
האמיגדלה המרכזית מהווה תחנת יציאה מרכזית ברשת הרגשית והלחץ של המוח ומקושרת באופן חזק להרגעת חרדה, לכמיהה ולשימוש כפייתי באלכוהול. בעבודה זו ניתחו החוקרים כ־175,000 גרעיני תאים בודדים שנלקחו לאחר המוות מהאמיגדלה המרכזית של 50 אנשים — 22 עם היסטוריה של הפרעת שימוש באלכוהול ו‑28 ללא AUD. באמצעות טכנולוגיה שקוראת הן פעילות גנים (RNA) והן נגישות כרומטין (מידת ה"פתיחות" או "סגירות" של ה‑DNA) באותו תא, הם בנו אטלאס מפורט של כל סוגי התאים העיקריים באזור זה, כולל מספר סוגי נוירונים ותאי תמיכה כמו אסטרוציטים ומיקרוגליה. הם גילו כי הנוירונים המעכבים — אלו שמרככים או מעצבים את פעילות המוח — שופעים במיוחד באמיגדלה המרכזית ונראים מושפעים במיוחד אצל אנשים עם AUD. 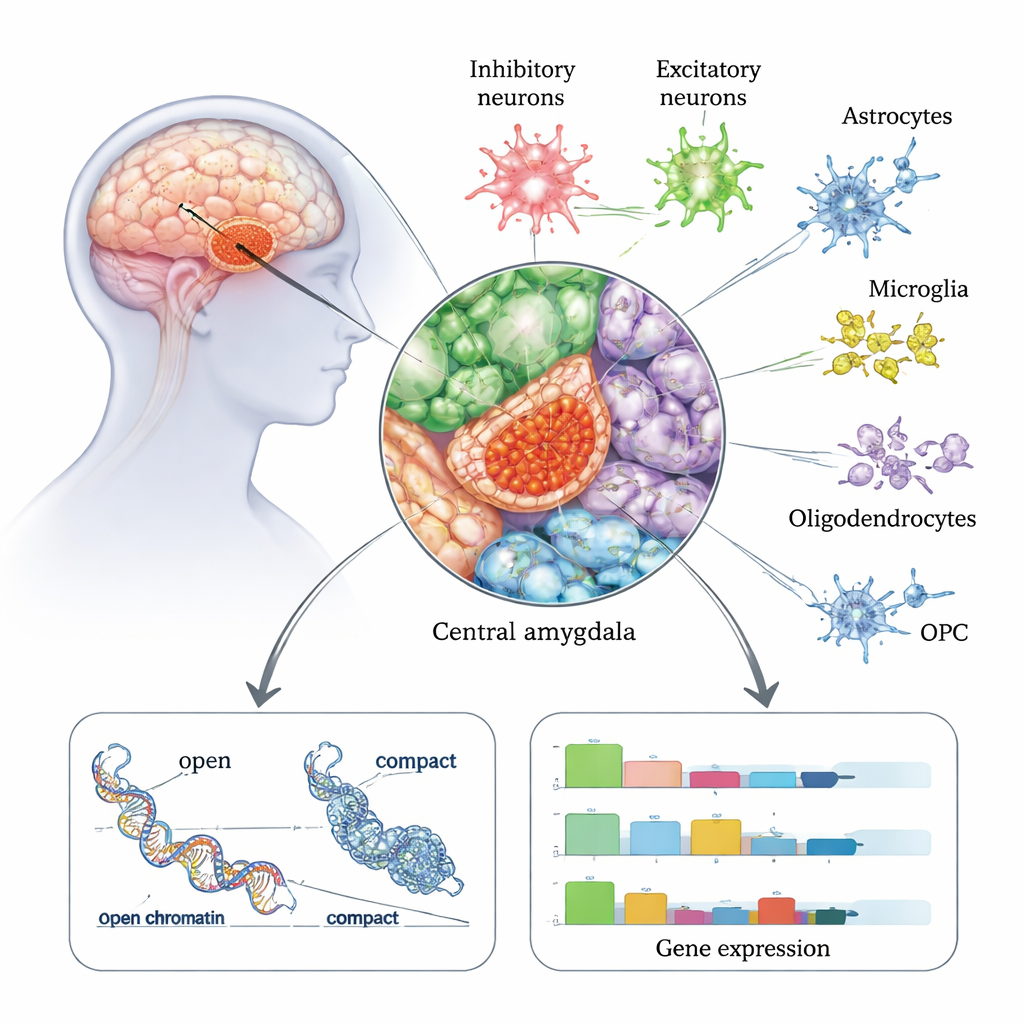
אילו תאים וגנים משתנים בהפרעת שימוש באלכוהול?
הצוות השווה באופן שיטתי את פעילות הגנים באנשים עם ובלי AUD, סוג תא סוג תא. הם גילו יותר מ‑1,800 גנים שהפעילות שלהם השתנתה באוכלוסיות תאים ספציפיות, כשהשינויים הגדולים ביותר התרחשו בנוירונים מעכבים, ואחריהם נוירונים מעוררי פעולה ואסטרוציטים. תת‑סוג של נוירונים מעכבים המסומן על ידי הפפטיד פרואנקפלין (PENK) הראה שינויים חזקים במיוחד. רבים מהגנים המושפעים מעורבים בתקשורת בין תאי מוח, ובמיוחד באיזון בין הסיגנל המעורר גלוטמט והסיגנל המעכב GABA. לדוגמה, הגן GABRA2, שמסייע בהרכבת סוג מרכזי של קולטני GABA, הוגבר בכמה נוירונים מעכבים, בעוד ש‑GRM8, קולט גלוטמט, ו‑NCAM1, מולקולת הדבקה תאית חשובה לסינפסות, השתנו בכיוונים מנוגדים בסוב‑סוגי נוירונים. דפוסים אלה מרמזים כי כוונון העדין של היזון והעיכוב באמיגדלה המרכזית מופרע ב‑AUD.
מתגי הבקרה של המוח: כרומטין ואלמנטים רגולטוריים
גנים אינם פועלים לבדם; הם נשלטים על ידי מקטעי DNA שפועלים כמו מתגים ומעריכי בהירות. בעזרת בחינה של הכרומטין — אופן אריזת ה‑DNA — זיהו החוקרים למעלה מחצי מיליון אלמנטים רגולטוריים מועמדים וקישרו אותם לגנים סמוכים באופן ספציפי לסוג תא. כמעט מחצית מהאלמנטים האלה היו ייחודיים לסוג תא יחיד, מה שמדגיש עד כמה תאי מוח שונים מתמחים. רבים מהאלמנטים הרגולטוריים שהשתנו ב‑AUD נקשרו לגנים המעורבים בטיפול בסידן ובאותות גלוטמט, כמו CALN1, גן הקושר סידן והפעיל בחוזקה בנוירונים. בנוירונים מעכבים, CALN1 הראה גם עלייה בביטוי וגם אשכולות צפופים של לולאות רגולטוריות, מה שמרמז שחשיפה לאלכוהול מעצבת מחדש את הארכיטקטורה המקומית של ה‑DNA ששולטת על גן זה. 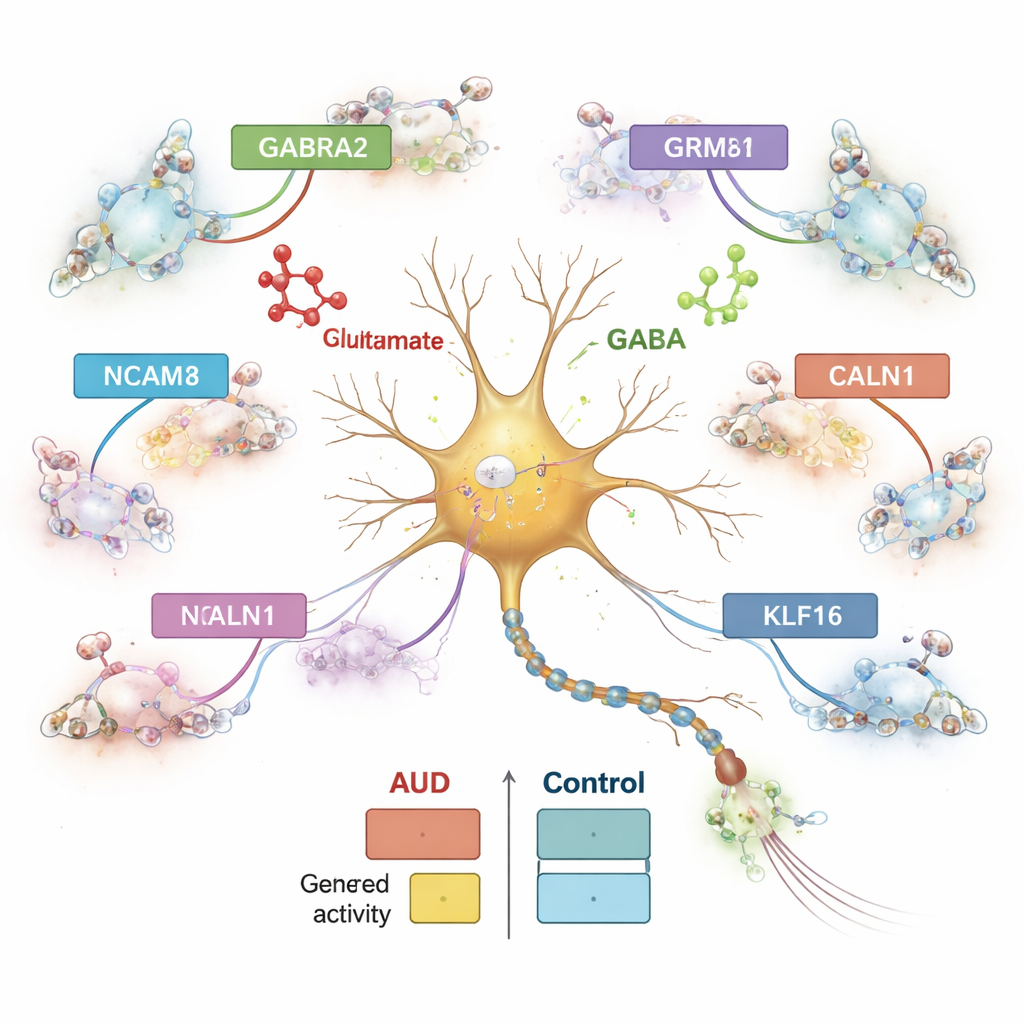
מגנים מסכנים לשינויים מוחיים ממשיים
מחקרים גנטיים זיהו וריאנטים רבים ב‑DNA שמגבירים את הסיכון לפתח בעיות עם אלכוהול, אך לא היה ברור היכן וכיצד הם פועלים במוח. על ידי חפיפת המפות תא‑הבודד שלהם עם מחקרים רחבי־גנום על שימוש בעייתי באלכוהול, מצאו המחברים כי גנים קשורי‑סיכון פעילים ומופרעים באופן בלתי‑פרופורציונלי בנוירונים של האמיגדלה המרכזית, במיוחד בנוירונים המעכבים. הם זיהו יותר מ‑200 וריאנטים סבירים סיבתית שיושבים בתוך אלמנטים רגולטוריים הפתוחים בסוגי תאים ספציפיים. חלקם נמצאו בתוך או בקרבת גנים שכבר קושרו להתמכרות, כגון CACNA1C ו‑DRD2, שמשתתפים בשליטה על יכולת ההרגש של הנוירון ובאותות דופמינרגיים. אחרים, כולל SEMA6D ו‑NF1, עלו כמועמדים חדשים. הצוות גם זיהה משפחת גורמי שעתוק בשם גורמי קרופל‑דמויי (Kruppel‑like factors), ובמיוחד KLF16, שנראים מתאמים שינויים נרחבים בגנים הקשורים לסידן ולגלוטמט, ואישרו חלק מהרשת הרגולטורית הזו במודל עכבר של חשיפה חריפה לאלכוהול.
מה המשמעות להבנה ולטיפול ב‑AUD
במילים פשוטות, המחקר מראה שהפרעת שימוש באלכוהול אינה רק בעיה מוחית מפוזרת אלא הפרעה מאורגנת מאוד, מרוכזת בסוגי תאים מסוימים ובמסלולים מולקולריים בתוך צומת רגשי חשוב. הנוירונים המעכבים של האמיגדלה המרכזית, יחד עם אסטרוציטים ותאי תמיכה אחרים, מראים שינויים מתואמים בפעילות גנים ובמתגי ה‑DNA ששולטים בגנים האלה — במיוחד במערכות שמנהלות אותות גלוטמט, GABA וסידן. על ידי קישור שינויים תאיים אלה לוריאנטים גנטיים של סיכון, העבודה מציעה מפה שמקשרת פגיעות תורשתית לאירועים מולקולריים מוחשיים במוח. עם הזמן, מפות ספציפיות‑תא אלה עשויות להנחות פיתוח טיפולים מדויקים יותר שישיבו את איזון ההתרגשות והעיכוב, במקום לפעול בצורה רחבה על כל המוח.
ציטוט: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
מילות מפתח: הפרעת שימוש באלכוהול, האמיגדלה המרכזית, גנומיקה של תאים בודדים, נוירונים מעכבים, ויסות גנים