Clear Sky Science · he
פעילות DOT1L מגבילה את מהירות ההארכה של השעתוק ומעדיפה עצירת RNAPII כדי להקל על מוטגנזה על ידי AID
איך תאי החיסון שלנו מכווננים עריכות DNA מסוכנות
מערכת החיסון שלנו יוצרת נוגדנים רבי עוצמה על ידי מוטציות מכוונות ב‑DNA שלה — אסטרטגיה מסוכנת שלעיתים עלולה לתרום לסרטן. המחקר הזה שואל שאלה שנראית פשוטה אך לה השלכות רחבות: מה קובע היכן ובאיזו יעילות מתרחשות המוטציות המכוונות האלה? התשובה מתרכזת בחלבון בשם DOT1L, שמכוונן את קצב קריאת הגנים בתאי B ובכך מסייע לכוון את מכונת המוטציה למקומות הנכונים.
הדלקת המוטציה כדי לחדד נוגדנים
כשתאי B נתקלים בזיהום, הם משדרגים את הנוגדנים בשני אופנים. הם מכניסים שינויים זעירים באזור הקושר של הנוגדן כדי להעלות את הקשירה לאיברונים, והם מחליפים את החלק ה"זנב" של הנוגדן כדי לשנות את תגובת מערכת החיסון. שתי השדרוגים מתחילים באנזים שנקרא AID, שמכה ומעוות DNA בגנים שנקראים באופן פעיל. בעוד ש‑AID חיוני לחיסון תקין, הוא עלול גם לפגוע בגנים אחרים, וליצור שבירות מסוכנות שמניעות סרטן דם. עבודות קודמות הראו ש‑AID מעדיף גנים שנקראים בשיעור גבוה ומוסדרים על ידי מתגים חזקים של DNA שנקראים סופר‑אנשלרס, אך זה לא הסביר מדוע רק תת‑קבוצה נבחרת של גנים חשופה באמת.
סמן כרומטין שמצביע על גנים רגישים ל‑AID
המחברים התמקדו בחלבונים הנמצאים בסמיכות ל‑AID בגרעין. באמצעות טכניקת תיוג בסביבה בתאי אדם הם גילו ש‑AID מצטבר ליד DOT1L, אנזים שמוסיף סימון כימי נקודתי על חלבוני היסטון שעליהם עטוף ה‑DNA. סימון זה, על היסטון H3 במיקום K79, שכיח בגנים פעילים. בתאי B של עכבר, גנים ש‑AID ממוטט בתדירות גבוהה — כולל גני הנוגדן ואופ־טארגטים מקושרים לסרטן — נשאו רמות גבוהות במיוחד של התגים האלה שיוצר DOT1L. כאשר החוקרים השביתו את DOT1L בקווי תאי B או חסמו את פעילותו בתרופה, המעבר מסוג הנוגדן (class switching) ירד, וכך גם השבורות ב‑DNA המונעות על ידי AID והחיבורים המסכנים בין גני נוגדן ובין הגן לצמיחה cMyc. משמעותית, נדרשה הפעילות הקטליטית של DOT1L, לא רק נוכחותו: גרסאות מוטנטיות שלא יכלו להניח את התג על ההיסטון נכשלו בשחזור החלפת הנוגדן הנורמלית.
האטת קורא הגנים כדי לתת ל‑AID זמן
מבט ראשון על כך עשוי להיראות מסתורי משום ש‑DOT1L קשור לגנים פעילים, אך הסרתו לא כיבתה פשוט את הגנים. באמצעות שיטה שמצלמת רנ״א חדש, הקבוצה גילתה שתאי B חסרי DOT1L למעשה ייצרו יותר טרנסקריפטים נאסנטיים ברבים מהגנים המסומנים על ידי DOT1L — על אף שראו מעט פחות מהמנוע המרכזי לקריאת גנים, RNA פולימראז II, ישוב על גנים אלה. על ידי שילוב קריאת רנ״א נאסנטית עם מפות של תפוסת הפולימראז, הם הסיקו שבתנאים רגילים התגים של DOT1L פועלים כמו שוברי מהירות עדינים. הם מאיטים את הפולימראז כשהוא מתקדם לאורך הגן ומאריכים הפסקות קצרות ליד ההתחלה ובתוך גופי הגנים המסומנים. בלי DOT1L, הפולימראז רץ מהר יותר וההפסקות קצרות יותר. מאחר ש‑AID זקוק לחלונות קצרים שבהם ה‑DNA חשוף והפולימראז מתעכב, ההאצה הזו מפחיתה במקביל את יכולתו של AID להיצמד ולבצע את תפקידו, גם כאשר השעתוק הכולל עולה.
להפריד בין פעילות גן לסיכון למוטציה
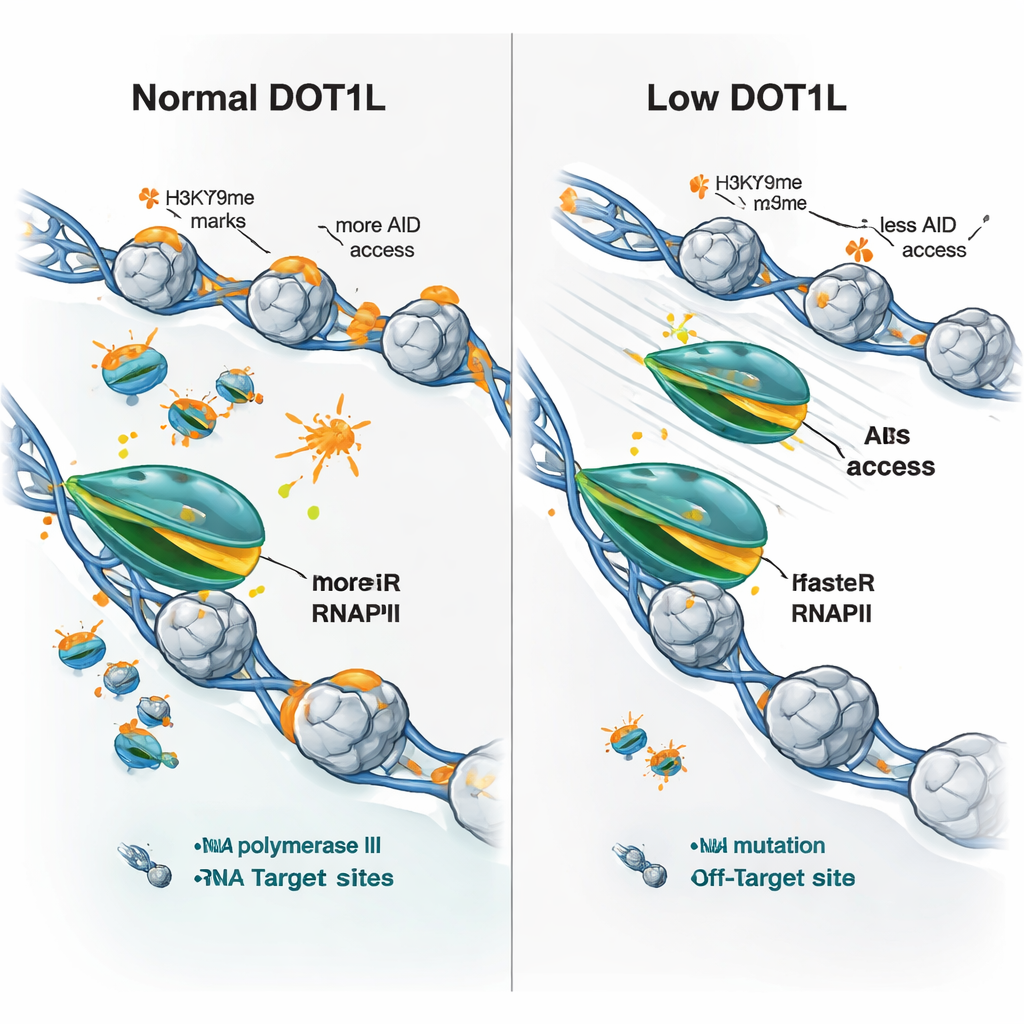
החוקרים שאלו האם שינויים בקצב יכולים להסביר את הדפוס המעורב בשעתוק שנצפה כאשר DOT1L נכחד — חלק מהגנים עולים, אחרים יורדים. הם גילו שכמעט כל הגנים המסומנים על ידי DOT1L שיתפו תכונה אחת בתאי knockout: הארכה מהירה יותר על ידי RNA פולימראז II. אבל התוצאה תלויה במצב ההתחלתי. גנים איטיים ובעלי ביטוי חלש נטו לייצר יותר רנ״א כשהפולימראז הוגבר בקצב, בעוד שגנים ארוכים מאוד ופעילים מאוד עם פולימראז שכבר מהיר לפעמים ייצרו פחות, כנראה כי המעבר המהיר מדי מפריע לעיבוד או להשלמה יעילים. ומהותית, גם בגני הנוגדן וגם באופ‑טארגטים הקלאסיים של AID, אובדן DOT1L הוביל לתנועה מהירה יותר של הפולימראז, פחות עדות ל"תקלות" של הפולימראז, וירידה משמעותית בכדאיות AID להיקשר, גם כאשר הגנים עצמם לא הושתקו.
מדוע זה חשוב לחיסון ולסרטן
במכלול, העבודה מציירת את DOT1L כבודק תנועה עדין למכונה הקוראת גנים בתאי B. על ידי הצבת תגים היסטוניים ספציפיים, DOT1L מאט במעט את RNA פולימראז II ומאריך את ההפסקות שלו, ויוצר סביבה של שעתוק שבה AID יכול לתפקד בעוצמה בגני נוגדן — ולצערנו גם בקבוצת גנים פגיעה מוגבלת אחרת — כדי להחדיר מוטציות. כאשר DOT1L נעדר או מעוכב, הפולימראז עובר במהירות, ומשאיר ל‑AID פחות הזדמנויות לפעול, מה שמחליש את גיוון הנוגדנים ובאותו זמן מוריד את הסיכון לסידורים מזיקים מסוימים. תובנה מכנית זו מסבירה מדוע אובדן DOT1L יכול גם להעלות וגם להוריד ביטוי גנים, וקושרת את השליטה העדינה במהירות השעתוק ישירות למקומות שבהם מערכת החיסון מעזה לכתוב מחדש את ה‑DNA שלה.
ציטוט: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
מילות מפתח: גיוון נוגדנים, אנזים AID, DOT1L, שעתוק גנים, תאי B