Clear Sky Science · he
הבסיס המולקולרי של אנטגוניזם בקולטן האנושי הדימרי לארגינין-ואזופרסין 1A
מדוע קולטן מוחי של הורמון חשוב
הורמונים כמו ואזופרסין ואוקסיטוצין ידועים בעיקר בשל ויסות מאזן המים, לחץ הדם, לידה ויצירת קשרים חברתיים. עם זאת, הדרך שבה הקולטנים שלהם פועלים ברמת האטום נותרה ברובה בלתי נראית. מאמר זה חושף מבני תלת־ממד מפורטים של קולטן מרכזי אחד, קולטן ה‑V1a האנושי של ואזופרסין, המקושר להתנהגות חברתית, לחץ ונגעי מוח שונים. הבנת צורתו ואופן חסימתו על ידי תרופות עשויה לסייע למדענים לעצב טיפולים טובים יותר למצבים כגון אוטיזם, הפרעת דחק פוסט‑טראומטית ומחלת הנטינגטון.
קולטן תאום שמעצב אותות בלב, כליה ומוח
קולטן V1a נמצא על פני השטח של תאים רבים בגוף, במיוחד בכלי דם, בכליות ובאזורים מסוימים במוח. כאשר הורמון ה‑ואזופרסין נקשר אליו, הקולטן מדליק מסלולי איתות פנימיים השולטים בלחץ הדם, מאזן הנוזלים ומעגלי מוח הקשורים לאינטראקציה חברתית, רגש ולחץ. מחקרים גנטיים וקליניים קישרו איתות V1a חריג להפרעות על הספקטרום האוטיסטי, PTSD ומחלת הנטינגטון, מה שהפך אותו למטרה תרופתית אטרקטיבית. כמה תרופות חוסמות V1a (אנטגוניסטים) כבר נמצאות בשימוש או בניסויים קליניים, אך עד כה איש לא ראה את קולטן V1a האנושי ברזולוציה גבוהה, מה שהותיר שאלות מרכזיות לגבי אופן ההרכבה שלו וכיצד בדיוק תרופות אלו מכבות אותו. 
לכידת מבנה הקולטן במצבים שונים של קשירת תרופות
החוקרים השתמשו במיקרוסקופיית אלקטרונים בקריוגניקה (cryo–EM), טכניקה שמקפיאה חלבונים במהירות ומצלמת אותם באמצעות קרן אלקטרונים, כדי להמחיש את קולטן ה‑V1a האנושי. כדי לייצב את החלבון הם מהנדסים צורה מעט מותאמת שעדיין קשורה היטב לתרופות וזיווגו עם מקטע נוגדן קטן (נאנובודי) לסיוע בהדמיה. הם פתרו מבנים של הקולטן בבדידותו ובקשירה לשלושה אנטגוניסטים רפואיים חשובים: atosiban (תרופת פפטיד המשמשת למניעת לידה מוקדמת), ושני מולקולות קטנות החודרות למוח, balovaptan ו‑SRX246, שנבדקו באנשים עם אוטיזם או מחלת הנטינגטון. כל המבנים הגיעו לרזולוציה כמעט אטומית, וחושפים את מיקומן של שבע הסלילים החוצים את הממברנה, הלולאות הגמישות והתרופות הקשורות.
קולטן המעדיף לפעול בזוגות
שלא כמו קולטים קרובים שנראו רק כיחידות בודדות, V1a הופיע כפועלז—דימר—בכל ארבעת מבני ה‑cryo‑EM. שני הקולטנים שוכבים זה לצד זה בממברנה, ומקיימים מגעים הדוקים בעיקר דרך אחד מהסלילים שלהם, בסיוע מגעים פולאריים ושומניים (הידרופוביים). כדי לבדוק אם צימוד זה מתרחש גם בתאים חיים, הצוות חיבר ל‑V1a חלבון פלואורסצנטי בוהק והשתמש בשיטת כיבוי פוטונים יחיד‑מולקולה: אם אזור על פני התא הכיל שני עותקי קולטן, האור שלו ייעלם בשתי קפיצות. בערך שלושת רבעי מהאזורים שנצפו כבו בדיוק בשתי קפיצות, דבר שתומך בחוזקה ברעיון ש‑V1a יוצר באופן טבעי דימרים על פני התא. כאשר המדענים שינו שיירים מרכזיים בממשק כדי להפריע למגעים, הקולטן עבר לכיוון יחידות בודדות והפך לפחות רגיש להורמון ולתרופה, מרמז שהדימר לא רק קישוט מבני אלא בעל חשיבות תפקודית. 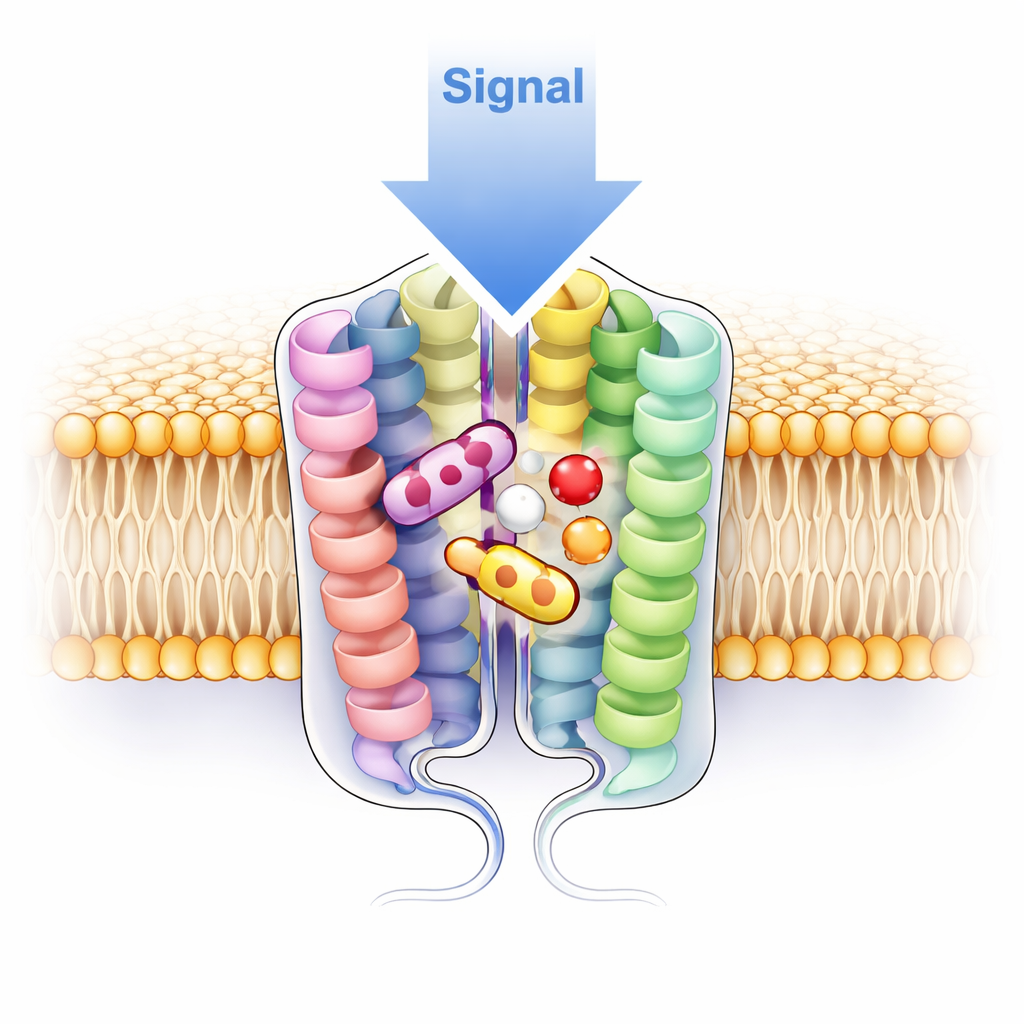
שער גמיש בפתח הקישור להורמון
הצוות גילה אזור "שער" בלתי צפוי שנקרא הלולאה החוץ‑תאית 2 (ECL2), הממוקמת בחלק העליון של כיס הקישור להורמון. במצב החופשי (apo), לולאה זו שוכבת שטוחה על הגרעין כמו מכסה ואינה יוצרת את קשר הדיסולפיד הטיפוסי (קשר גופרתי‑גופרתי) הנצפה בקולטים קרובים רבים. במקום זאת, חלקים מהלולאה קופלים לתוך הכיס ונשמרים בעזרת רשת אינטראקציות עם הסלילים הסובבים, וכיסויים חלקית את חלל הקישור הגדול והדביק. כאשר אחד משלושת האנטגוניסטים נקשר, ECL2 מתנודד מעלה ומחוצה לו, יוצר את קשר הדיסולפיד הקלאסי ויוצר חלל רחב מלא ממס שבו התרופות תופסות מקום. תנועה דרמטית זו מרמזת ש‑V1a עשוי להשתמש ב‑ECL2 כמחסום דינמי להגבלת הפעלה אקראית על ידי מולקולות חיצוניות, ושתרופות יכולות להיות מעוצבות או לכלא את הלולאה במצבה השטוח "הבסיסי" או לנצל את המצב המוגבה והפתוח שלה.
איך שלוש תרופות השותקות את אותו קולטן בדרכים שונות
Atosiban, המדמה בצורתו באופן קרוב את ההורמון הטבעי אוקסיטוצין, מתארך מהחלק העליון של הכיס עד לבסיסו, ומעגן את עצמו באמצעות קומבינציה של קשרי מימן ומגעים הידרופוביים. על ידי שינוי כמה עמדות מפתח בהשוואה לאוקסיטוצין, הוא אינו מצליח להפעיל את שרשרת המעברים הפנימיים הדרושה בדרך כלל להפעלת הקולטן: שיירי "מיקרו‑מפסקים" חיוניים שנעים בזמן האיתות נשארים נעולים במצבי הינוח שלהם, החלל הפנימי שמאפשר את כניסת חלבון ה‑G לעולם לא נפתח, ואתר קשירת המגנזיום החשוב להפעלה מופרע. לעומת זאת, balovaptan ו‑SRX246 הן מולקולות קטנות, בלתי‑פפטידיות, החודרות עמוק אל הכיס אך מיישמות אסטרטגיות שונות. Balovaptan מסתמך על ליבה הידרופובית קשיחה המתאפקת באופן צמוד לתוך חריץ עמוק, בתוספת זנב פולארי גמיש שמגיע לעבר פתח הכיס. SRX246 משתמשת בארכיטקטורה מודולרית, כמו חלקי־בניין, המעוגנת על ידי ליבת β‑לקטאם, עם "אזורים" שונים הממלאים תת‑כיסים ומתרחבים לעבר הלולאות החוץ‑תאיות. בשני המקרים התרופות מייצבות מצורת ינוח שאינה תואמת לקשירת חלבון G. הבדלים עדינים בצורת ובכימיה של הכיס—במיוחד בשתי עמדות על סלילים 5 ו‑7—מסבירים מדוע balovaptan ו‑SRX246 מעדיפות V1a על פני קולטים קרובים מאוד.
השלכות לטיפולים עתידיים
באמצעות מתן תמונות ברזולוציה גבוהה של V1a כדימר, גילוי קונפורמציית לולאה "שטוחה" שלא נראתה קודם במצב חופשי, ופירוט האופן שבו שלושה אנטגוניסטים שונים מאוד מכבים את הקולטן, עבודה זו מספקת למעצבי תרופות מפה מבנית מדויקת למטרת V1a. היא מציעה דרכים לעצב תרופות בדור הבא שיכולות לנצל מאפיינים ספציפיים לדימר או לנעול את הקולטן במצב ינוח עמוק במיוחד, במטרה לטפל בהפרעות מוחיות וקשורות ללחץ באופן ממוקד יותר ובפחות תופעות לוואי.
ציטוט: Zhong, P., Chu, B., Yu, Z. et al. Molecular basis of antagonism of the dimeric human arginine vasopressin receptor 1A. Nat Commun 17, 1622 (2026). https://doi.org/10.1038/s41467-026-68331-5
מילות מפתח: קולטן ואזופרסין V1a, קולטן מקושר לחלבון G, דימריזציה של קולטן, מבנה קריו-EM, עיצוב תרופות לנוירו־פסיכיאטריה