Clear Sky Science · he
עיצוב חישובי של ציקלופרופאנאזים כלליים עם סלקטיביות סטראודיוורסנית
למה מבנים קטנים של שלוש טבעות חשובים לתרופות
ציקלופרופאנים — טבעות פחמן בעלות שלושה אטומים — הם בלוקים קטנים ומתוחים שיכולים לשנות באופן דרמטי את אופן הפעולה של תרופה בגוף. הסידור התלת‑ממדי המדויק של האטומים (הסטרוכימיה) יכול להכריע אם מולקולה תהפוך לתרופה מועילה או למעטפת לא פעילה או אפילו מזיקה. מאמר זה מתאר אסטרטגיה חישובית לעיצוב אנזימים שיכולים באופן מהימן לייצר את כל ארבעת הצורות התלת‑ממדיות האפשריות של הטבעות הללו מאותו חומר פתיחה, ובכך לפתוח דלת לחקירה מהירה ונקייה יותר של מועמדי תרופות.
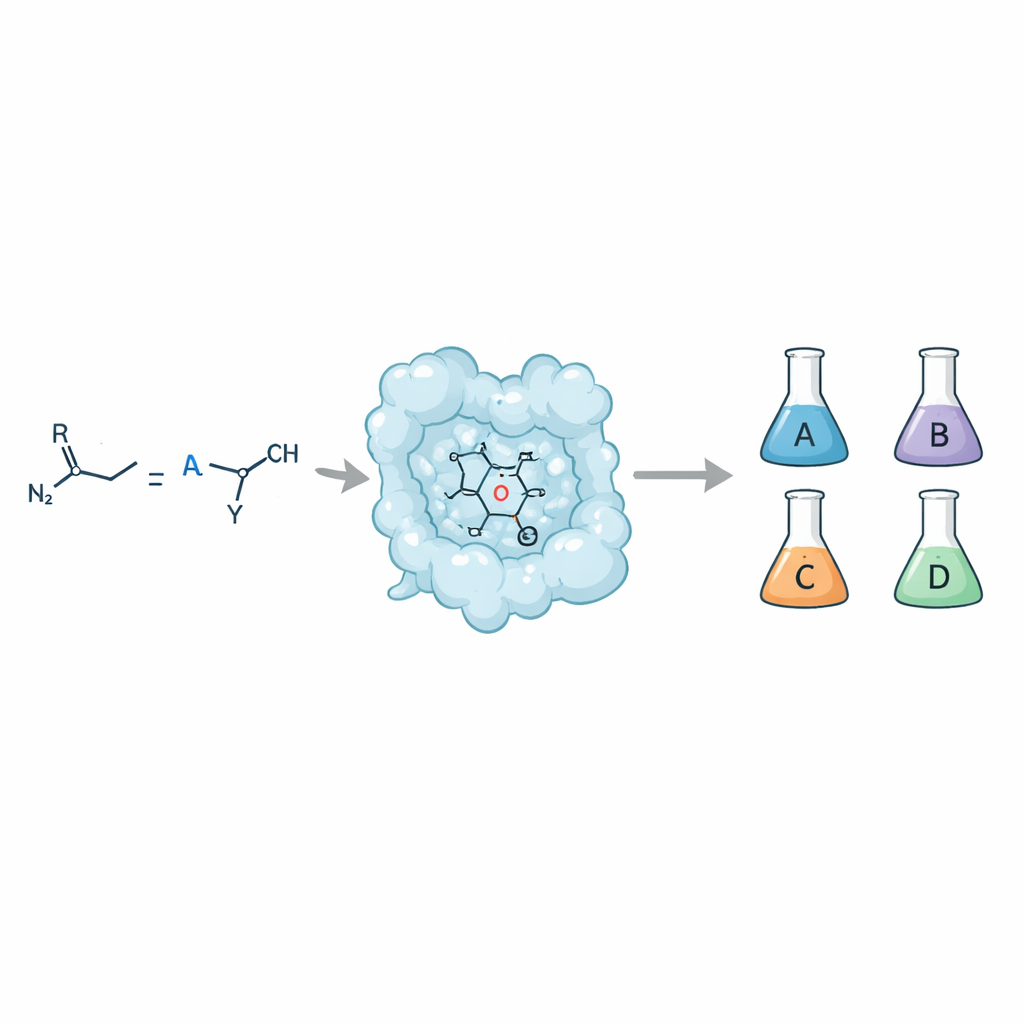
ממתכון אחד לארבע תוצאות שונות
כשקשר כפול פשוט (אולפין) מגיב עם תורם קארבן כגון תרכובת דיאזו, התוצאה יכולה להיות טבעת ציקלופרופאן. אך אותה טבעת יכולה להתקיים בארבע צורות סטראואיזומריות שונות, שכל אחת מהן כוללת את אותם האטומים אך מסודרת בצורה שונה במרחב. כימאים מעוניינים להגיע לכל אחת מהצורות האלה כיוון שהן יכולות לתקשר באופן שונה מאוד עם מטרות ביולוגיות ולהשפיע על תכונות מפתח של תרופה כמו ספיגה, מטבוליזם ובטיחות. קטליזטורים מולקולאריים מסורתיים לעתים קרובות מצליחים לשלוט בכך, אך השגת יכולת זו בעזרת אנזימים — הקטליזטורים של הטבע — היתה קשה, במיוחד כשמטרת המחקר היא גם חד‑סלקטיביות גבוהה וגם סבולת למגוון רחב של סובסטרטים.
עיצוב אנזימים על מסך מחשב
המחברים פיתחו תהליך חישובי מבוסס‑מנגנון ורב‑מצבי כדי לפתור את הבעיה. הם השתמשו תחילה בחישובי כימיה קוונטית למיפוי מצבי המעבר החולפים — המבנים האנרגטיים הגבוהים לאורך מסלול התגובה — ליצירת כל אחד מארבעת הסטריאואיזומרים של הציקלופרופן. דגמים אלה הושמו בתוך אתרי הפעילות של חלבונים שונים המכילים מה, ותוכנת העיצוב Rosetta שימשה להערכת האופן בו כל חלבון מייצב או מDestabilize כל מצב מעבר. באופן קריטי, ציון העיצוב מקצוע מוטב מוטציות שמהללות גם את מצב המעבר הרצוי (עיצוב חיובי) וגם דוחים את המצבים המתחרים (עיצוב שלילי), ובכך מלמדים למעשה את האנזים "להעדיף" מוצר תלת‑ממדי אחד על פני האחרים.
בניית ערכת כלים אנזימטית מלאה
באמצעות גישה זו, הצוות יצר משפחה של אנזימי "כלליים" לציקלופרופנציה. מתוך מיון של מיאוגלובין, הם שינו את אתר הפעילות שלו כדי לקבל וריאנטים שמפיקים ברזולוציה גבוהה את הטרנס‑(1R,2R) ציקלופרופן עם סלקטיביות גבוהה ופעילות טובה על פני יותר מ‑20 אולפינים שונים, כולל סובסטרטים לא מאוקטבים ואלקטרון‑עניים קשים. מיאוגלובין שעוצב קודם לכן סיפק כבר את המוצר המשלים טרנס‑(1S,2S). להשגת שני מוצרי הסיס, המחברים פנו לחלבוני מה אחרים. הם עיבדו את האנזים החיידקי P450cam כדי להשיג וריאנטים שנותנים סלקטיבית את הסיס‑(1S,2R), ומינפו את האנזים האנושי אינדולאמין 2,3‑דיאוקסיגנאז‑1 (IDO1) — שלא שימש קודם לכן בכימיית קארבן — כדי להעדיף את הסיס‑(1R,2S). בסה"כ, ארבעת הביוקטליזטורים הללו יכולים לייצר כל סטריאואיזומר של אותה קבוצת מוצרי ציקלופרופן, לעתים עם שליטה של עד 99% הן בדיאסטריאומר והן באננטיומר.
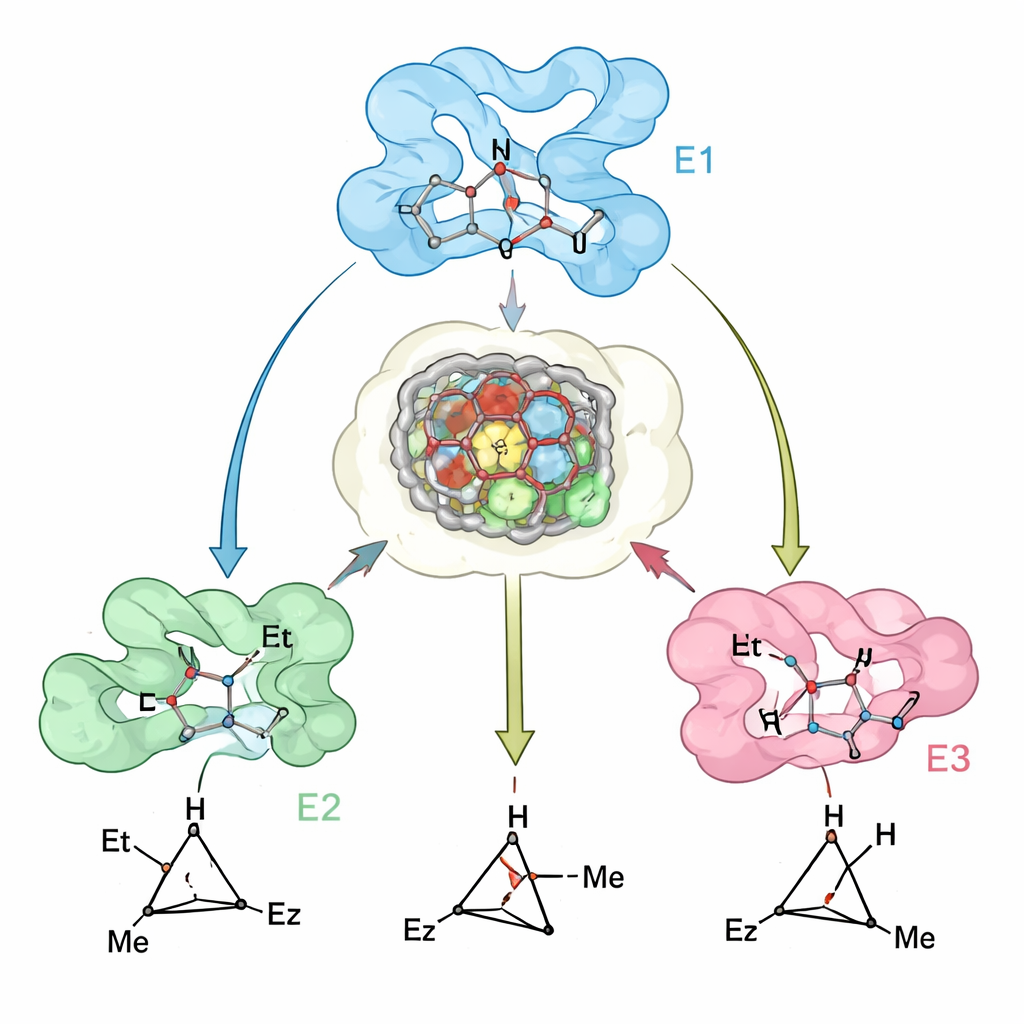
כיצד העיצוב משקף את המציאות
כדי לבדוק עד כמה המודלים החישוביים שלהם משקפים אנזימים אמיתיים, החוקרים פתרו מבני גביש של וריאנט מיאוגלובין מרכזי והשוו אותם למבנים שחזו. ההתאמה היתה קרובה, ונתונים ניסויים הדגישו תכונה עדינה אך חשובה: אתר הפעילות של החלבון מאורגן מראש כדי לקבל את מצב המעבר המועדף, בעוד שזזים קטנים בלולאות ובהליקסים סמוכים גורמים לקישור של מצב המעבר ה"שגוי" להיות בעל עלות אנרגטית גבוהה. היכן שהתחזיות היו פחות מדויקות — למשל עבור כמה סובסטרטים גדולים — אי‑ההתאמות יכולות להיות מיוחסות לתזוזות של השלד (backbone) שלא נתפסו במלואן במודלים, ומה שמצביע על דרכים ברורות לשיפור שיטות העיצוב בעתיד.
מה המשמעות עבור תרופות וקטליזטורים עתידיים
על‑ידי שילוב מיפוי מצבי מעבר מבוסס פיזיקה עם עיצוב חכם של חלבונים, עבודה זו מדגימה שניתן לתכנת מראש תוצאות סטרוכימיות של תגובות מוכללות על ידי אנזימים, במקום לגלות אותן רק באמצעות אבולוציה בהתנסות וטעיה. ערכת הציקלופרופאנאזים שהתפתחה מספקת לכימאים דרך מעשית להכין מערכי שלמות של סטריאואיזומרים של ציקלופרופן ממגוון רחב של אולפינים, ובכך מפשטת מאוד את מחקרי המבנה‑פעילות בגילוי תרופות ובסינתזת מוצרי טבע. אסטרטגיה זו צפויה להיות ניתנת להתאמה לסוגי אנזימים וקבוצות תגובה אחרות, מה שמזרז את יצירת הביוקטליזטורים שנוגעים בדיוק תלת‑ממדי במולקולות מורכבות.
ציטוט: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
מילות מפתח: ביוקטליזה, ציקלופרופנציה, עיצוב אנזימים, סטרוכימיה, חלבוני המה