Clear Sky Science · he
גורצראול 3-פוספט אצילטרנספרז מחמירה את רעילות α-סינוקלאין על־ידי הגברת פירוק שומנים חמצוני
מדוע השומנים במוח חשובים למחלת פרקינסון
מחלת פרקינסון מתוארת בדרך כלל כבעיה בחלבון הנקרא אלפא‑סינוקלאין, שמתצבר וגורם נזק לתאי מוח ששולטים על תנועה. המאמר הזה מראה ששומני המוח — ובעיקר האופן שבו הם מיוצרים ומושמדים — משחקים תפקיד חזק ומפתיע בקביעת מידת רעילותו של אלפא‑סינוקלאין. על‑ידי גילוי אנזים ליצירת שומנים שמחמיר פגיעה בתאי עצב, העבודה מצביעה על מסלול חדש שניתן לטפל בו תרופתית ויכול להשלים מאמצים קיימים להתמודדות עם פרקינסון במקורו.
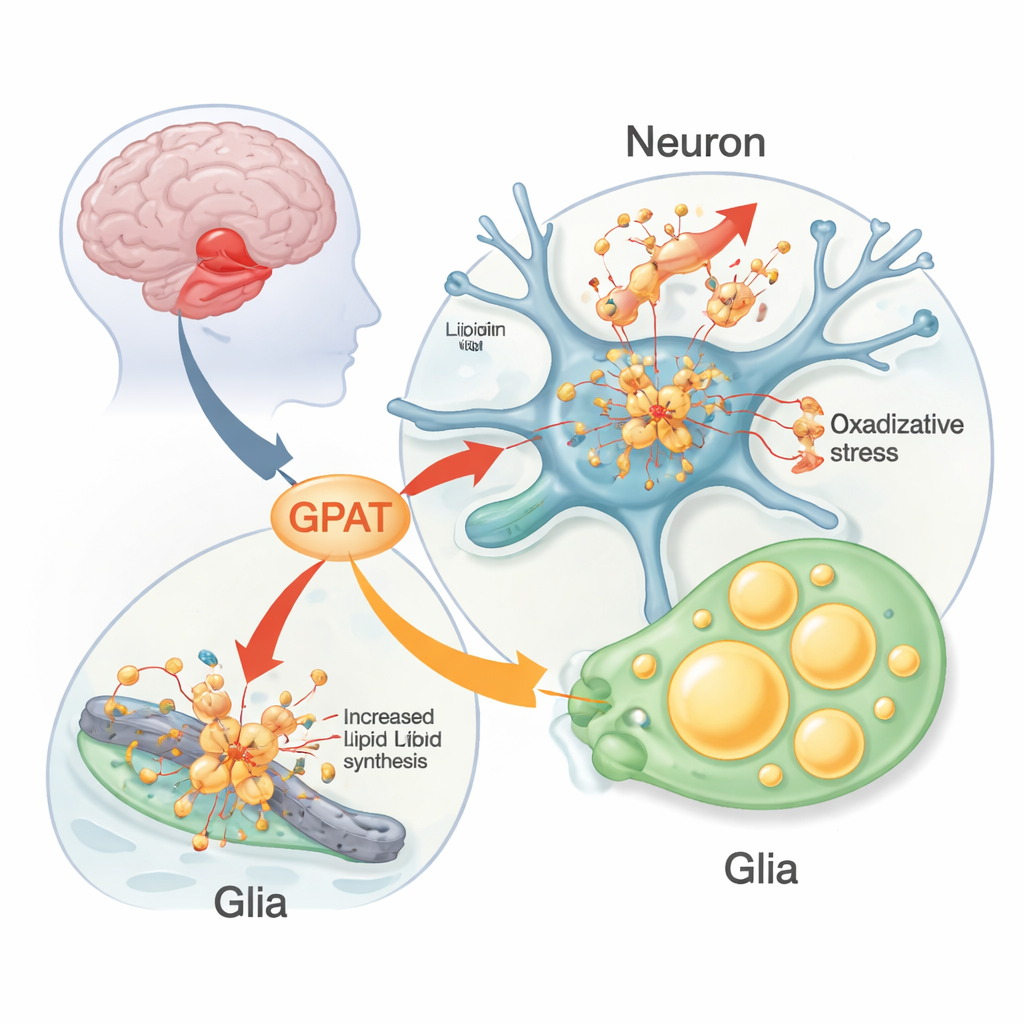
חלבון שמתנהג בצורה לקויה בפרקינסון
אנשים עם פרקינסון מאבדים בהדרגה תאי עצב שמייצרים דופמין באזור מוחי עמוק שמ_COORDINATES תנועה. בתוך התאים המתים הללו, מדענים מוצאים לעתים קרובות משקעים צפופים הנקראים גופי לווי, שהם עמוסים בחלבון אלפא‑סינוקלאין. במשפחות נדירות מוטציות או עותקים נוספים של גן האלפא‑סינוקלאין גורמים ישירות לפרקינסון, אבל וריאנטים גנטיים נפוצים בגן זה מעלים רק במידה מתונה את הסיכון. זה מרמז שגנים ומסלולים אחרים משפיעים על מידת הנזק של אלפא‑סינוקלאין. עדויות גוברות מצביעות על ליפידים — שומנים ומולקולות דמויי שומן שמרכיבות ממברנות תא ומאגרים אנרגיה — כשותפים מרכזיים גם בהצטברות האלפא‑סינוקלאין וגם במוות התאי.
גילוי אנזים שומני חזק במודלים של זבובי פרי
החוקרים השתמשו בזבובים מהונדסים שמייצרים אלפא‑סינוקלאין אנושי במערכת העצבים שלהם כמערכת ניסוי חיה. זבובים אלה מפתחים תופעות דמויות פרקינסון: אובדן תאי דופמין, קושי בטיפוס, ושיבוש קצבי פעילות יומיומיים. הצוות שינה בצורה שיטתית גרסאות זבוב של גנים אנושיים שקשורים לסיכון לפרקינסון כדי לראות אילו מהן משנות את השפעת האלפא‑סינוקלאין. אחד בלט: גן שנקרא mino, שמקודד לצורה מיטוכונדריאלית של האנזים glycerol 3‑phosphate acyltransferase (GPAT). GPAT יושב בנקודת הכניסה לבניית פוספוליפידים וטריגליצרידים — הליפידים שמרכיבים ממברנות וטיפות שומן. כשהצוות הפחית את פעילות mino בתאים עצביים, זבובי האלפא‑סינוקלאין שמרו על יותר מתאי הדופמין שלהם ונעו בצורה טובה יותר לזמן ארוך יותר; הגברת mino הביאה להשפעה ההפוכה והמיטיבה.
שומנים פגומים, מיטוכונדריות בסטרס וטיפות שומן בגליה
בהעמקה נוספת, המדענים מצאו כי GPAT השפיע על כמות הנזק החמצוני שהצטבר בליפידים של המוח. בזבובי אלפא‑סינוקלאין שמוחזקים בטמפרטורה גבוהה יותר (מה שמחמיר תכונות מחלה), פירוק שומנים חמצוני — ״חלודה״ כימית של שומנים — עלה בממברנות המוח. הקטנת mino צימצמה נזק זה, בעוד שהעברתו לרמות גבוהות הגביר אותו; ללא אלפא‑סינוקלאין, שינויי mino כמעט ולא השפיעו. סמנים למוות תאי באזור הראייה שיקפו דפוס זהה. הצוות גם תיאר הצטברות בולטת של טיפות שומן — כדורי אגירת שומן זעירים — לא בתאים עצמם אלא בתאי גליה שכנים. טיפות אלה התרחבו עם הגיל בזבובי אלפא‑סינוקלאין והיו נתונות לשליטה על‑ידי אנזימים שבונים או מפרקים טריגליצרידים, מה שמדגיש שותפות מטבולית פעילה בין נוירונים וגליה במצב סטרס.
חישמול מטבולי והצטברות אלפא‑סינוקלאין
מדידות מטבוליטים ממוחות הזבובים הראו שהבעת אלפא‑סינוקלאין קשורה לצוואר בקבוק במחזור המייצר אנרגיה של התא: ציטרט ואיזו‑ציטרט, שני מתווכים של מעגל חומצות הטריקרבוקסיל (TCA), הצטברו בעוצמה בעוד שהשלבים שאחריהם השתנו במידה מתונה יותר. גם רמות לקטט עלו, בהתאם להגברה של גליקוליזה. במקביל, פרופיל ליפידים מפורט הצביע על שינויים באיזון הפוספוליפידים הממברנליים והרכב חומצות השומן שלהם, כשהם מטים לכיוון סוגים הרגישים יותר לנזק חמצוני. כשצמצמו מספר אנזימי GPAT — mino במיטוכונדריה ואנזימים קרובים על הרשתית האנדופלזמית — אלפא‑סינוקלאין עדיין הצטבר, אבל הנטייה שלו ליצור אוליגומרים בדרגה גבוהה (קשירות חלבונים מרובות) ירדה, והמיטוכונדריות הראו פחות סימנים של מתח חימצוני ו״הזדקנות״.
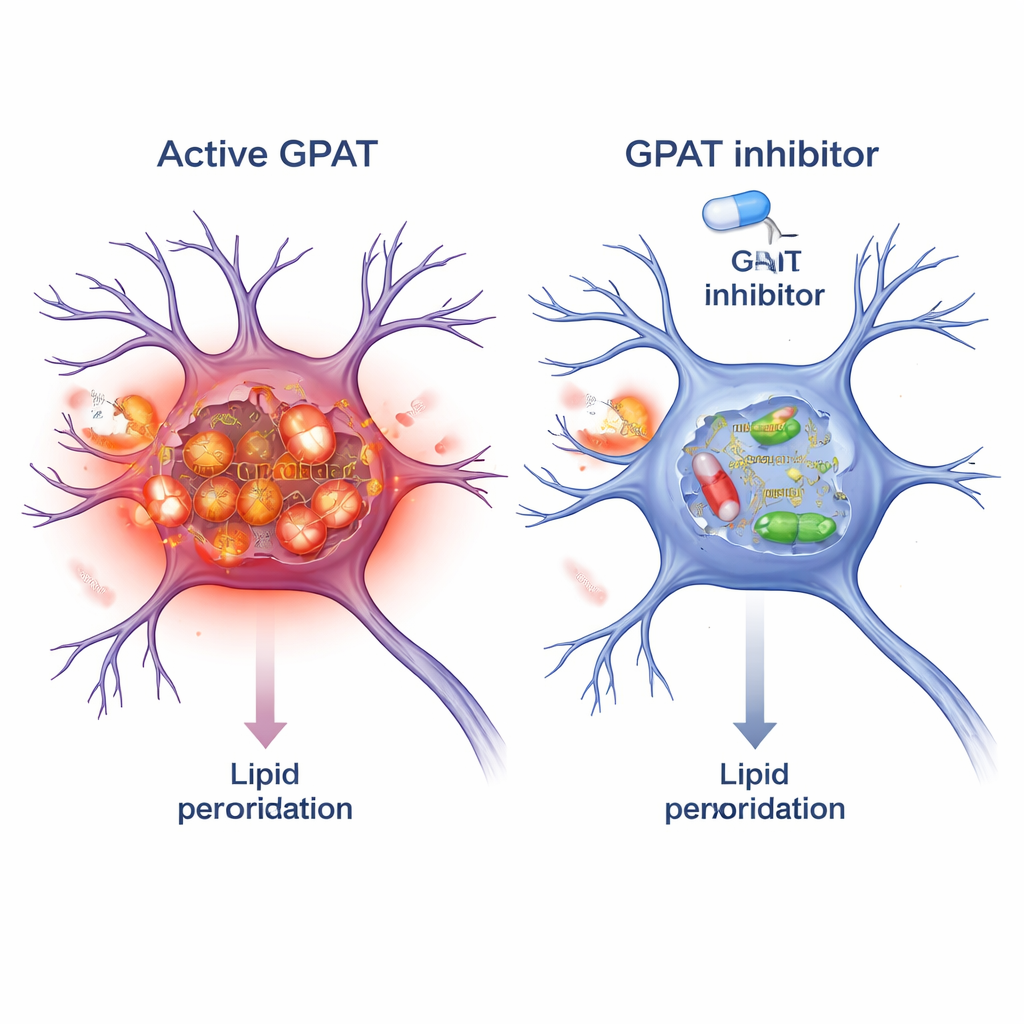
חסימת GPAT כאסטרטגיה מגן
מכיוון ש‑GPAT הוא אנזים, ניתן לכוון אותו באמצעות מולקולות קטנות. החוקרים בחנו את FSG67, מעכב GPAT קיים שפותח במקור להשמנת יתר וסוכרת. בזבובי אלפא‑סינוקלאין, הוספת FSG67 למזון שוחזרה את היתרונות של דיכוי גנטי של GPAT: תנועה משופרת, הישרדות טובה יותר של תאי דופמין, פחות אוליגומרים מזיקים של אלפא‑סינוקלאין, ופחות מתח חמצוני במיטוכונדריה. כדי לבדוק אם המושג מתקיים גם בחולייתנים, טיפלו בתרבית תאי מוח של עכבר בסיבים מוצקים של אלפא‑סינוקלאין שהכינו מראש, שמזרזים הצטברות של אגיגטים רעילים. טיפול משולב עם FSG67 צימצם את הצטברות אלפא‑סינוקלאין מזורחן, והוריד מספר מדדים עצמאיים של פירוק שומנים חמצוני בתוך תאים אלה.
מה משמעות הדבר עבור אנשים עם פרקינסון
במילים פשוטות, עבודה זו מראה שאופן הטיפול של המוח בשומנים יכול להעלות או להוריד את רעילות האלפא‑סינוקלאין. כש‑GPAT פעיל מאוד, נבנים לתוך ממברנות וטיפות אגירה ליפידים פגיעים יותר, שקל יותר לחמצנם; סביבה שומנית זו נוטה לעודד צורות מזיקות של אלפא‑סינוקלאין וללחוץ על המיטוכונדריות, תחנות הכוח של התא. הקטנת פעילות GPAT — גנטית או בעזרת תרופה — מזיזה את האיזון לעבר פחות ״חלודה״ של ליפידים, פחות אסיפות חלבון רעילות,and תאים בריאים יותר. בעוד שממצאים אלה מוקדמים ומקורם בזבובים ובתאי עכבר בתרבית, הם מצביעים על מטבוליזם הליפידים, ובפרט על GPAT, ככיוון מבטיח חדש לטיפולים בפרקינסון שיכול להשלים אסטרטגיות שמכוונות ישירות את אלפא‑סינוקלאין.
ציטוט: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
מילות מפתח: מחלת פרקינסון, אלפא-סינוקלאין, פירוק שומנים חמצוני, מעכב GPAT, ניוֹרונְדֶגֶנֶרציה