Clear Sky Science · he
מבנה קומפלקס SHOC2-KRAS-PP1C חושף קובעי איזוֹם-ספציפיים של RAS ותובנות על עיכוב עצמת ההרכבה על-ידי מעכבי RAS
איך תאים מחליטים מתי לגדול
התאים שלנו נשענים על מערכת חיווט פנימית כדי להחליט מתי לגדול, להתחלק או להישאר שקטים. בלב מערכת זו נמצאים חלבוני RAS, מתגים מולקולריים זעירים שמתפקדים לעתים שגויה בסרטן. מחקר זה חוקר לעומק כיצד קבוצה מסוימת של חלבונים — SHOC2, RAS ו‑PP1C — מצטרפת כדי להפעיל מתג מרכזי של גדילה, וכיצד ניתן לכוונן תרופות מודרניות נגד סרטן כדי לחסום תהליך זה ביעילות רבה יותר ולמנוע מגידולים להתחמק מהטיפול.
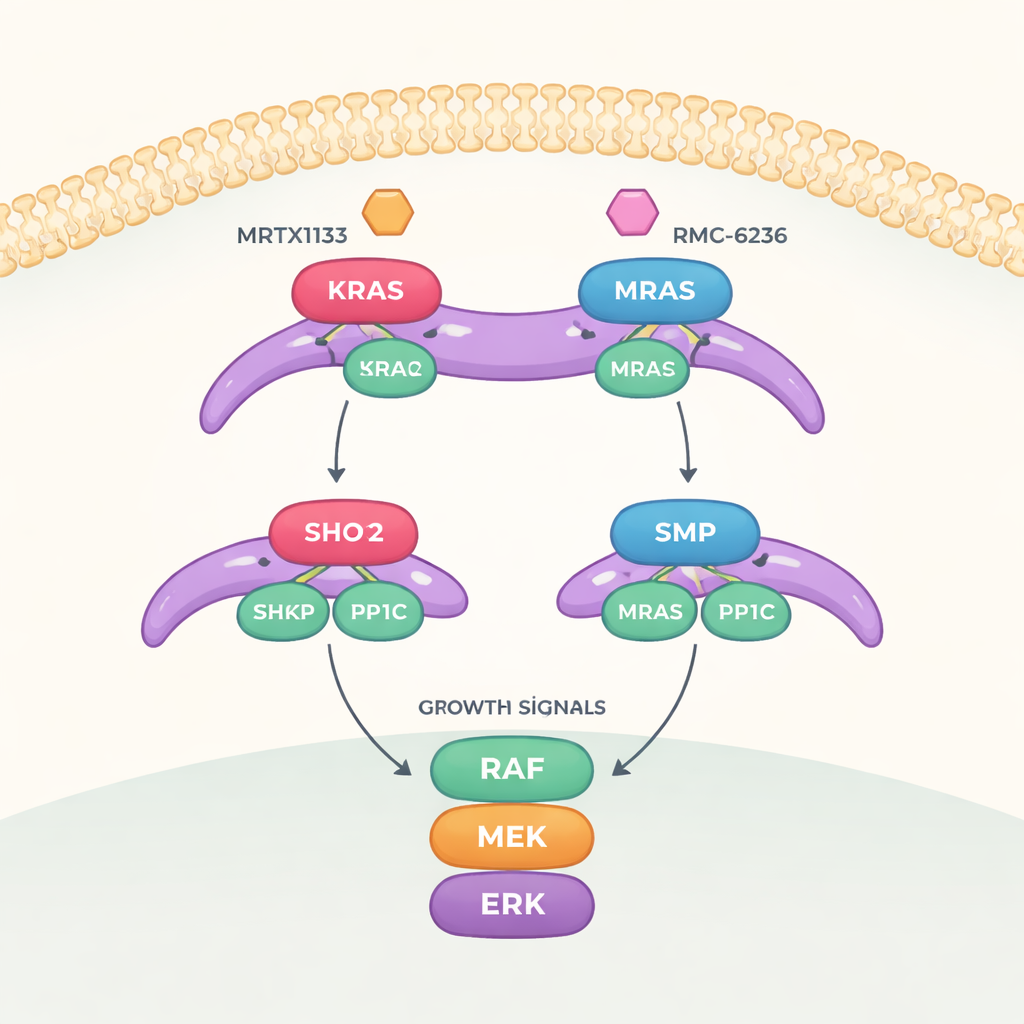
מתג גדילה עם שלושה רכיבים קריטיים
העבודה מתמקדת במסלול איתות שנקרא נתיב MAPK, שמעביר מסרים של גדילה ממעטפת התא אל הגרעין. על מנת להפעיל נתיב זה במלואו, חלבון נוסף בשם RAF חייב לעבור ממצב "כבוי" למצב "מופעל". המתג הזה נשלט על ידי קומפלקס תלת‑חלקי המורכב מ‑SHOC2 (תבנית המחזיקה את הרכיבים יחד), PP1C (אנזים המוסר תג פוספט) ו‑RAS פעיל. כשהם מורכבים, השלושה מסירים סימן פוספט ספציפי מ‑RAF, ומשחררים אותו להפעיל את קסקדת הגדילה שממשיכה מטה.
מדוע שותף בעל זיקה נמוכה עדיין חשוב בסרטן
קיימים כמה סוגי חלבוני RAS. MRAS יוצר קומפלקס בעל זיקה גבוהה מאוד עם SHOC2 ו‑PP1C, בעוד הנהגים המוכר יותר של סרטן — KRAS, HRAS ו‑NRAS — יוצרים גרסאות פחות חזקות של אותו קומפלקס. למפתיע, תאים סרטניים המונעים על‑ידי מוטציות ב‑KRAS, HRAS או NRAS תלויים מאוד ב‑SHOC2, אף על פי שהקומפלקסים שלהם פחות יציבים. מערכי סריקות גנטיות רחבי היקף מראים שרבים מהגידולים עם מוטציות מסוימות ב‑RAS — במיוחד במיקומים מפתח כמו Q61 ו‑G13 — רגישים מאוד לאובדן SHOC2, כלומר ההרכבה הזו חיונית להישרדותם.
חשיפת צורת קומפלקס KRAS
עד כה מדענים ראו רק מבנה ברזולוציה גבוהה של הקומפלקס החזק המבוסס על MRAS. הגרסה החלשה של KRAS התמוטטה בקלות מדי כדי ללכוד אותה. במחקר הזה השתמשו החוקרים במוטציות הקשורות למחלה שמחזקות בעדינות את המגעים בין הרכיבים כדי לייצב את קומפלקס SHOC2–KRAS–PP1C מספיק זמן לצילום במיקרוסקופ אלקטרונים קראיו. הם גילו שהארכיטקטורה הכללית תואמת בקירוב את קומפלקס MRAS, אך ל‑KRAS חסרים כמה תכונות מבניות קטנות ש‑MRAS משתמש בהן כדי להיאחז ב‑SHOC2 וב‑PP1C ביתר כוח. כתוצאה מכך, הרכבה של KRAS טומנת פחות שטח מגע ומייצרת פחות קשרים, מה שמסביר מדוע היא באופן פנימי פחות יציבה, אף שהיא נותרת חשובה מאוד בגידולים שבהם KRAS פעיל בצורה מופרזת.
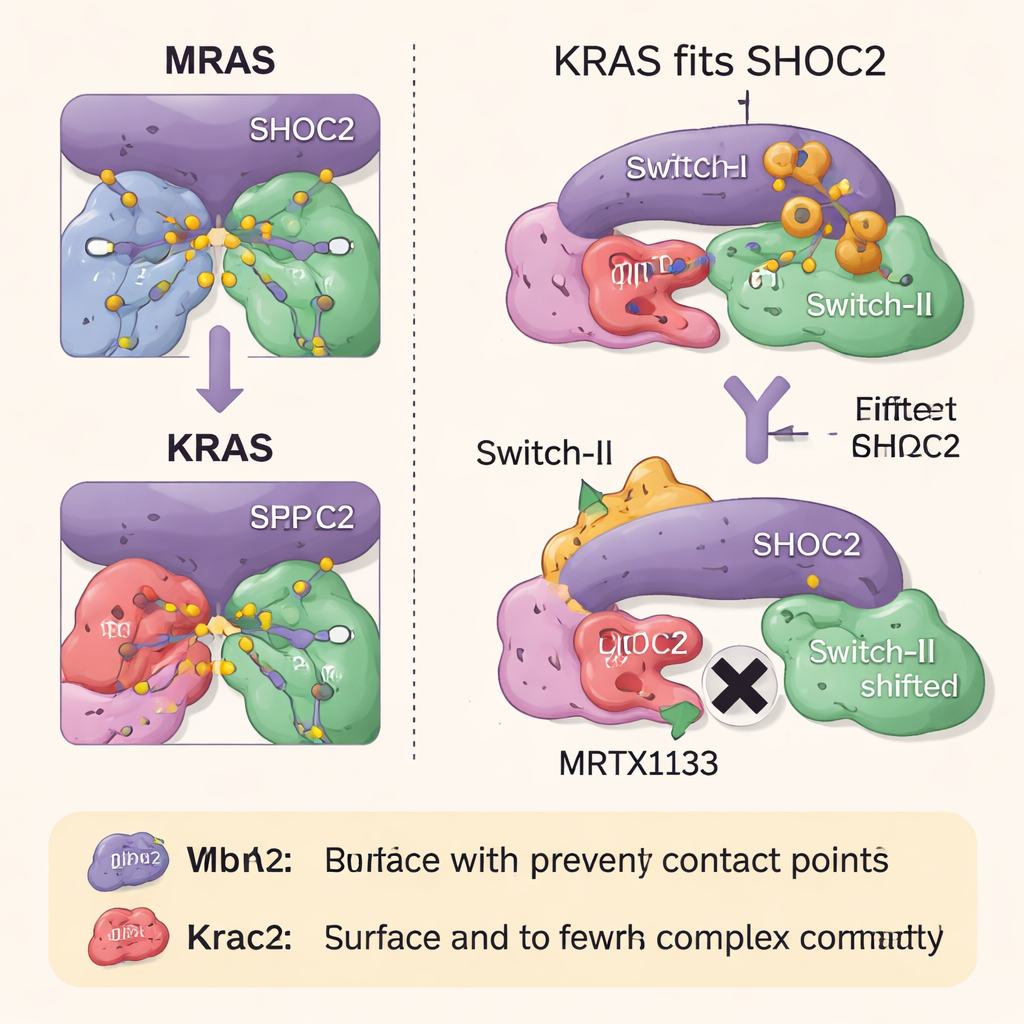
כיצד תרופות נגד RAS חוסמות את הרכבת הקומפלקס
הצוות חקר אחר כך כיצד שתי קטגוריות של תרופות המכוונות RAS משפיעות על קומפלקס תלת‑החלקי הזה. MRTX1133, שתוכננה לקשור כיס ליד אזור גמיש של KRAS המכונה Switch‑II, נועלת אזור זה בצורה שמתנגשת עם משטח SHOC2. הדבר מונע בצורה חזקה הרכבת קומפלקסים חדשים של SHOC2–KRAS–PP1C, אם כי היא פחות יעילה בפירוק קומפלקסים שכבר התקיימו. תרופה שנייה, RMC‑6236, פועלת יחד עם חלבון מסייע (ציקלופילין A) וחוסמת גם היא את אותם משטחים ב‑KRAS הנדרשים לקשירת SHOC2. עם זאת, אף אחת מהתרופות אינה קושרת באופן טבעי את MRAS, כך שהקומפלקס בעל הזיקה הגבוהה ל‑MRAS נשאר שלם ויכול לסייע להחזיר את מסלול הגדילה לפעולה כאשר KRAS מעוכב.
כיוון מטרה כפולה כדי למנוע עמידות
כדי לבדוק האם אפשר לבצע כיוון כפול, החוקרים מהנדסים גרסה של MRAS שבה כיס Switch‑II שונה כך שמעלה MRTX1133 יוכל כעת לקשור אותה. המוטנט הזה עדיין יצר קומפלקס חזק עם SHOC2 ו‑PP1C, אך התרופה כעת חסמה את הרכבתו והפחיתה את יכולתו להפעיל את RAF בניסויים מבחנה. יחד עם נתונים על תרכובות הקשורות ל‑SHOC2, התוצאות האלה מראות שניתן מעשית לעצב תרופות שיכבו הן את הקומפלקס המבוסס‑KRAS והן את זה המבוסס‑MRAS. לאדם מן השורה, המסר המרכזי הוא שתאים סרטניים משתמשים במספר מתגים קרובים הקשורים זה לזה כדי לשמור על זרימת אותות הגדילה, במיוחד כאשר מתג אחד מושתק על‑ידי תרופה. על‑ידי הבנת הצורות והקשרים המדויקים בתוך הרכבי החלבון האלה, החוקרים יכולים לתכנן כעת טיפולים שפוגעים בשני הנתיבים החלופיים בבת אחת, מה שמקשה על סרטן מונע‑RAS להתאים ולהתנגד לטיפול.
ציטוט: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
מילות מפתח: איתות RAS, מעכבי KRAS, נתיב MAPK, קומפלקסי חלבונים, התנגדות לתרופות