Clear Sky Science · he
מנגנון עמידות SARS-CoV-2 לתרופות אנטיווירליות מבוססות אנלוגים של נוקלאוטידים
איך הווירוס חכם יותר מתרופות מרכזיות
וירוס הקורונה שייך לקבוצה נדירה של וירוסי RNA שיכולים לבדוק את החומר הגנטי שלהם, מה שהופך אותו ליעיל במיוחד בהתנגדות לחלק מהתרופות האנטיווירליות הטובות שלנו. מחקר זה חופר לפרטים ברמת האטום של איך SARS‑CoV‑2 מזהה ומסיר קטגוריה נפוצה של תרופות שנקראות אנלוגים של נוקלאוטידים, ומסביר מדוע תרופות שעובדות טוב נגד וירוסים אחרים לעיתים קרובות מפגינות ביצועים פחותים בזיהומי קורונווירוס.
משיכת חבל על RNA הוויראלי
SARS‑CoV‑2 משכפל את הגנום ה‑RNA שלו באורך כ־30,000 תווים באמצעות מכונה מולקולרית גדולה הנקראת קומפלקס השכפול‑הטרנסקריפציה. במרכזו נמצאת ה‑RNA‑תלויה ב‑RNA פולימראז (RdRp), המזינה גדילי RNA חדשים, ויחידה נפרדת, האקסונוקלאז (ExoN), המבצעת בדיקת שגיאות וגיזום תיקונים. גלולות אנטיווירליות רבות, כולל תרופות שפותחו במקור להפטיטיס C, מחקות את אבני הבניין של ה‑RNA באופן מספיק קרוב כדי שה‑RdRp יכניס אותן לשרשרת, אך עם שינויים עדינים שמעצרים את השכפול או יוצרים שגיאות. לרוע המזל, לקורונווירוסים יש את ה‑ExoN, שיכול לזהות את החיקויים האלה לאחר שהם בשרשרת ה‑RNA ולחתוך אותם החוצה, וכך להציל את השכפול הוויראלי.
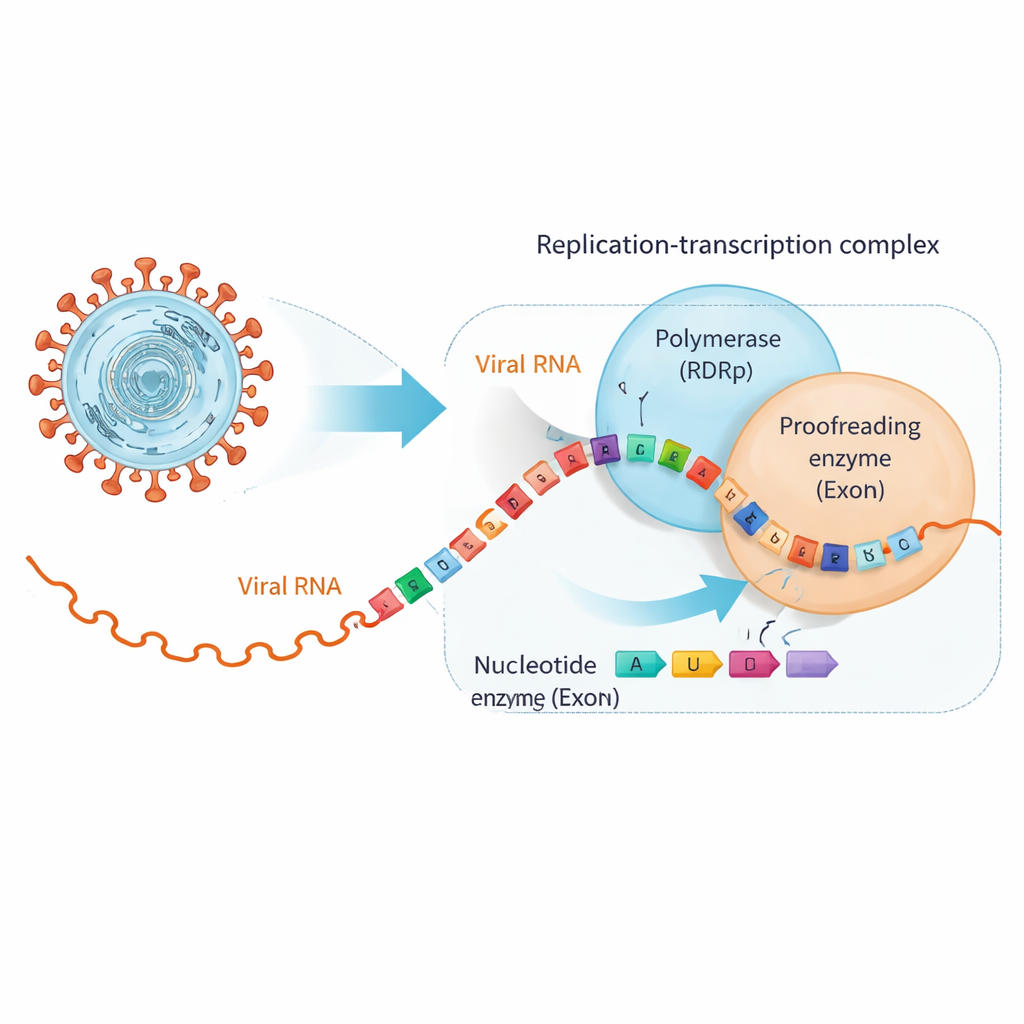
כאשר תרופות מועילות משנות את שותפות ה‑RNA
החוקרים התמקדו בשתי תרופות אנטיווירליות קליניות חשובות, בֶּמניפוסבּוּר ומְסוֹפוֹסבוּר, שתיהן תוכננו לפעול כבוני RNA פגומים. הם הראו תחילה כי פולימראז הווירוס מכניס בקלות את האנלוגים האלה בקצה גדיל ה‑RNA ואז ברוב המקרים מפסיק להאריך את השרשרת, כפי שמיועד. עם זאת, ניסויי קשירה חשפו תפנית: ברגע שאנלוג יושב בקצה ה‑RNA, ה‑RNA כבר לא מתחבר באופן חזק לפולימראז אלא מתחבר חזק יותר ל‑ExoN. למעשה, ה‑RNA המשונן בתרופה דוחף החוצה ממכונת ההעתקה ונמסר לבדוק השגיאות, שלוקח את ההזדמנות לגזור את הנוקלאוטיד הבעייתי ולאפשר לשכפול להימשך.
בדיקת שגיאות שמואטת אך לא נעצרת
ניסויי קורס‑זמן ביוכימיים הראו כי ה‑ExoN כן מסיר את הבמניפוסבּוּר והמסופוסבּוּר מ‑RNA, אך לאט יותר מאשר כשהוא מסיר נוקלאוטידים תקינים. בתגובות ללא תאים, שני האנלוגים חסמו בחוזקה המשך סינתזת RNA — אך כאשר נוסף ExoN פעיל, חלק משמעותי משרשראות ה‑RNA התקועות ניצלו והורחבו. מוטנט של ExoN מושבת לא הצליח לעשות זאת, מה שאישר כי הפעילות המבוּקרת של בדיקת השגיאות אחראית לביטול חלק ניכר מאפקט התרופות. הנוכחות של הפולימראז לצד ה‑ExoN האיצה למעשה את הסרת האנלוגים, מה שמרמז ששני האנזימים הוויראליים פועלים בשיתוף כדי לפנות מכשולים ולשמר את השכפול.
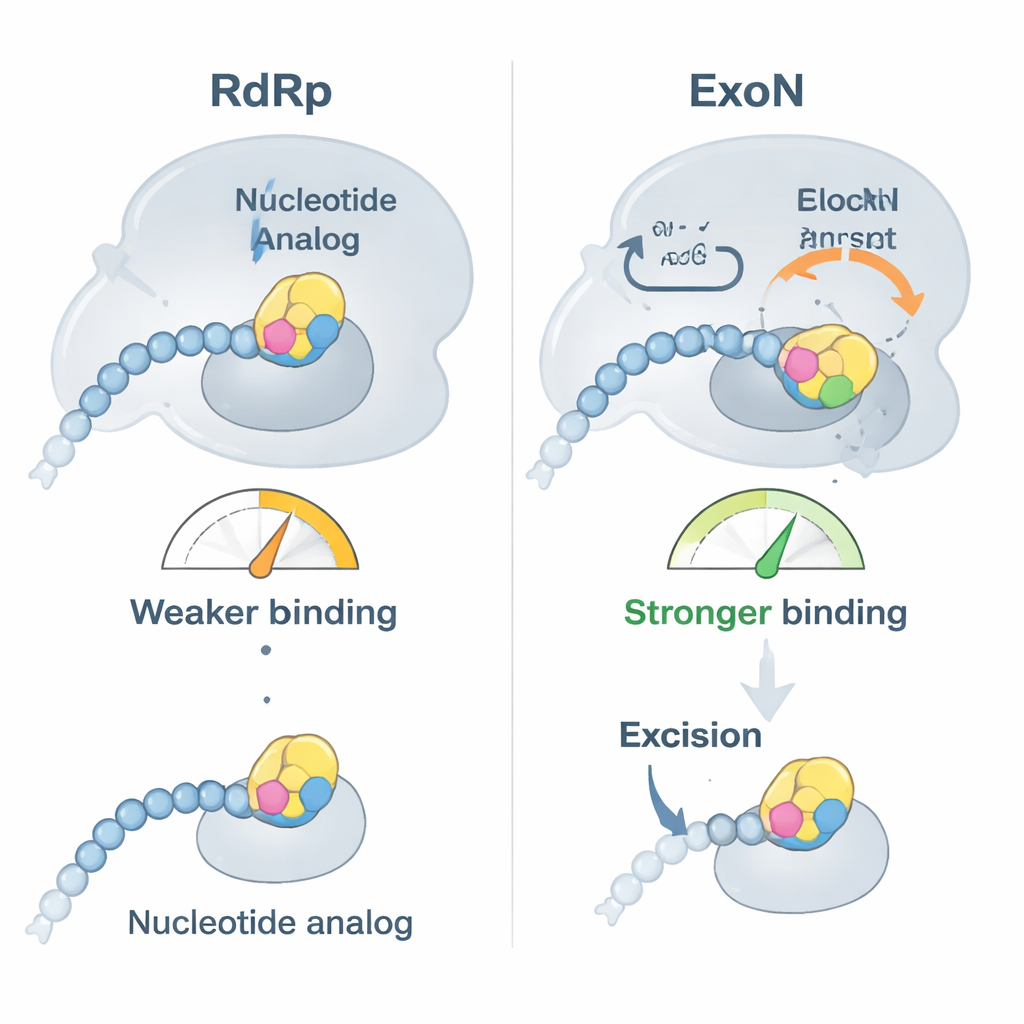
צפייה בבודק השגיאות ברזולוציה אטומית
כדי להבין כיצד ה‑ExoN מזהה ומגיב לתרופות אלה, הצוות השתמש במיקרוסקופ אלקטרונים קפוא ברזולוציה גבוהה כדי לפתור מבנים של קומפלקס ה‑ExoN קשור לגדילי RNA שמסתיימים בבמניפוסבּוּר או במסופוסבּוּר. מבנים אלה, חדים דיים כדי לראות קבוצות כימיות בודדות, חשפו כי הטבעת הסוכרית המותאמת בכל תרופה נכנסת לכיס הידרופובי שנוצר על‑ידי לולאה קצרה של חלבון ה‑ExoN. התאמה הדוקה נוספת זו מסבירה את הקשירה החזקה יותר של RNA המכיל תרופות ל‑ExoN. אך יש גם תופעת לוואי בלתי צפויה: על‑ידי מתיחת אותה לולאה, התרופות מפריעות לסידור המדויק של לולאת קטליזה סמוכה שמחזיקה שייר היסטידין מפתח במקומו. כאשר ההיסטידין נוטה הרחק מאתר החיתוך, המרכז הפעיל של ה‑ExoN נעשה חלקית מושבת, מה שמאט אך אינו מונע לחלוטין את חיתוך האנלוג.
מתג פנימי שמכוונן את בדיקת השגיאות הוויראלית
מוטציות בחומצות אמינו בודדות בתוך הלולאה הרגישה אישרו את חשיבותה. שינויים בארבעה שיירים משומרים הפחיתו במידה ניכרת את יכולת ה‑ExoN לחתוך גם קצות RNA סטנדרטיים וגם קצות שמסתיימים בתרופה, ושינו גם את הנוקלאוטיד הסופי שה‑ExoN מעדיף להסיר. זה מזהה את הלולאה כמווסת אלוסטרי — מתג מכני משולב שמרגיש איזה סוג נוקלאוטיד נמצא בקצה ה‑RNA ומכווין את פעילות האנזים. המבנים מראים גם כי ה‑ExoN מזהה בסיסים שונים (A, U, C או G) באמצעות קשרי מימן גמישים, אך מתקשה במיוחד לאכלס בסיסים דמויי גואנין, דבר רלוונטי משום שבמניפוסבּוּר מחקה גואנוזין.
מסקנות עבור התרופות העתידיות נגד COVID‑19
ללא מומחיות מיוחדת, המסר המרכזי הוא ש‑SARS‑CoV‑2 נושא "בודק איות" מתוחכם שיכול לשלוף תרופות מסוימות מהגנום שלו לאחר שהן עשו את שלהן ועצרו את השכפול. במניפוסבּוּר והמסופוסבּוּר כן מחלישים את מכונת ההעתקה של הווירוס, אך במקביל הם מכוונים את ה‑RNA אל בודק השגיאות שיכול לבטל חלקית את האפקט שלהם. על‑ידי גילוי בדיוק כיצד בודק השגיאות הוויראלי אוחז בתרופות אלה, וכיצד לולאה רגולטורית זעירה מזיזה את האנזים בין מצבים פעילים לפחות פעילים, עבודה זו מציעה מפת דרכים לעיצוב נוקלאוטידים אנטיווירליים חדשים שיכולים או להיקשר בצורה גרועה יותר ל‑ExoN, או לנעול אותו בקונפורמציה לא פעילה, או לנצל את הקושי שלו בהתמודדות עם מבנים דמויי גואנין. מולקולות מדור הבא כאלה עשויות להיות קשות בהרבה למחיקה על‑ידי הווירוס, ולשפר את יכולתנו לטפל ב‑COVID‑19 ובוונגעות קורונווירוס עתידיות.
ציטוט: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
מילות מפתח: SARS-CoV-2, עמידות לאנטי‑ויראליים, אנלוגים של נוקלאוטידים, בדיקת שגיאות ב‑RNA, שכפול קורונווירוס