Clear Sky Science · he
הבסיס המולקולרי לעיכוב מתילציה של DNA חדשה על ידי TCL1A
כיצד התאים מחליטים מה לשמור בזיכרון
לכל תא בגופך יש כמעט את אותו ה‑DNA, ועדיין תאי מוח, תאי דם ותאי עור מתנהגים בצורה שונה מאוד. אחת הדרכים שבהן תאים "זוכרים" את זהותם היא באמצעות תגיות כימיות המוסיפות ל‑DNA, תהליך המכונה מתילציה של DNA. המחקר הזה מגלה, ברזולוציה אטומית, כיצד חלבון קטן בשם TCL1A יכול לכבות את האנזימים שמוסיפים את סימני המתיל האלה. מכיוון ששינויי מתילציה של DNA ו‑TCL1A קשורים לסרטן והפרעות רבייה, הבנת הדחיקה המולקולרית הזו עשויה בסופו של דבר להניע פיתוח טיפולים חדשים.
מכונת תגי ה‑DNA של התא
מתילציה של DNA פועלת כמו סימון בעיפרון בשוליי הגנום, ועוזרת להשתיק גנים מסוימים ולייצב את הגנום במהלך ההתפתחות. שני אנזימים, DNMT3A ו‑DNMT3B, הם ה"כותבים" המרכזיים שמוסיפים מתילים חדשים במהלך ההתפתחות המוקדמת וכשגזעים מתמיינים. אם אנזימים אלה מוטנטים או לא מפוקחים כראוי, תבניות סימני ה‑DNA עלולות להתפרק ולתרום לתסמונות התפתחותיות וללוקמיות. TCL1A הוא חלבון הנודע בעיקר בשל תפקידו בסרטני תאי חיסון, בהם הוא לעתים קרובות מופרז. מחקרים קודמים רמזו ש‑TCL1A יכול להיקשר ל‑DNMT3A ו‑DNMT3B ולהחליש את פעילותם, אך לא היה ברור כיצד בדיוק הוא משיג את החסימה הזו.
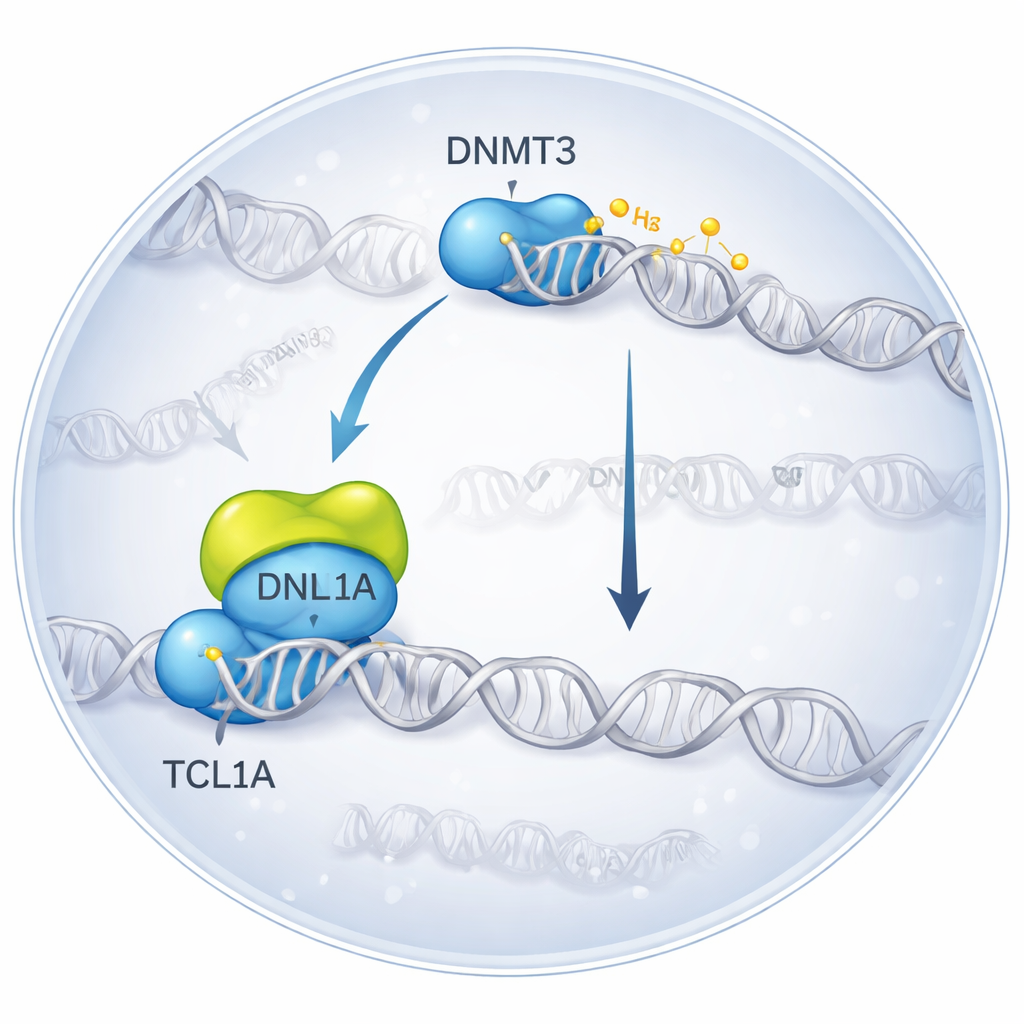
הקפאת מפגש מולקולרי בתלת‑ממד
החוקרים השתמשו במיקרוסקופיה קרי‑אלקטרונית, טכניקה שמדמה מולקולות שהוקפצו במהירות, כדי להמחיש את הקומפלקס שנוצר כאשר DNMT3A נקשר ל‑TCL1A. הם מצאו ששתי מולקולות DNMT3A מתיישבות בזוגות, ובכל צד דימר של TCL1A נצמד אל החלק הקטליטי של DNMT3A — אותו אזור שבדרך כלל מתקשר לחלבוני סיוע ול‑DNA. משטח הקישור הזה חופף לנקודה שבה בדרך כלל מצרף שותף אחר, DNMT3L, כדי להגביר את פעילות DNMT3A. בבדיקות ביוכימיות, הוספת TCL1A צמצמה באופן חד את יכולתם של DNMT3A ו‑DNMT3B לבצע מתילציה של DNA, אפילו בנוכחות DNMT3L, מה שאישר שהקומפלקס המבני תואם למצב מעוכב בחוזקה.
שינוי צורה שמתקע את האנזים
במבט מעמיק יותר, הצוות ראה שקישור TCL1A אינו פשוט יושב מעל אתר הפעילות כמו מכסה. במקום זאת, הוא מעורר שינוי עדין אך נרחב בצורת DNMT3A. שני אזורים גמישים של האנזים, הידועים כלולאת ההכרה במטרה (target‑recognition loop) והלולאה הקטליטית, מתנודדים הרחק מהמקומות שלהם כאשר DNMT3A קשור ל‑DNA. בצורה הפעילה, הלולאות האלה מתחבקות אל ה‑DNA ויוצרות כיס למולקולת דלק קטנה הנקראת SAM, שמעניקה את קבוצת המתיל. בנוכחות TCL1A, הלולאה הקטליטית מתקפלת אל תוך כיס ה‑SAM וחוסמת אותו, ובו בזמן מקשה על הגעת ה‑DNA אל האנזים. מדידות קישור אישרו ש‑DNMT3A ששותף עם TCL1A כבר לא יכול לאחוז ב‑DNA או ב‑SAM באופן שניתן למדוד.
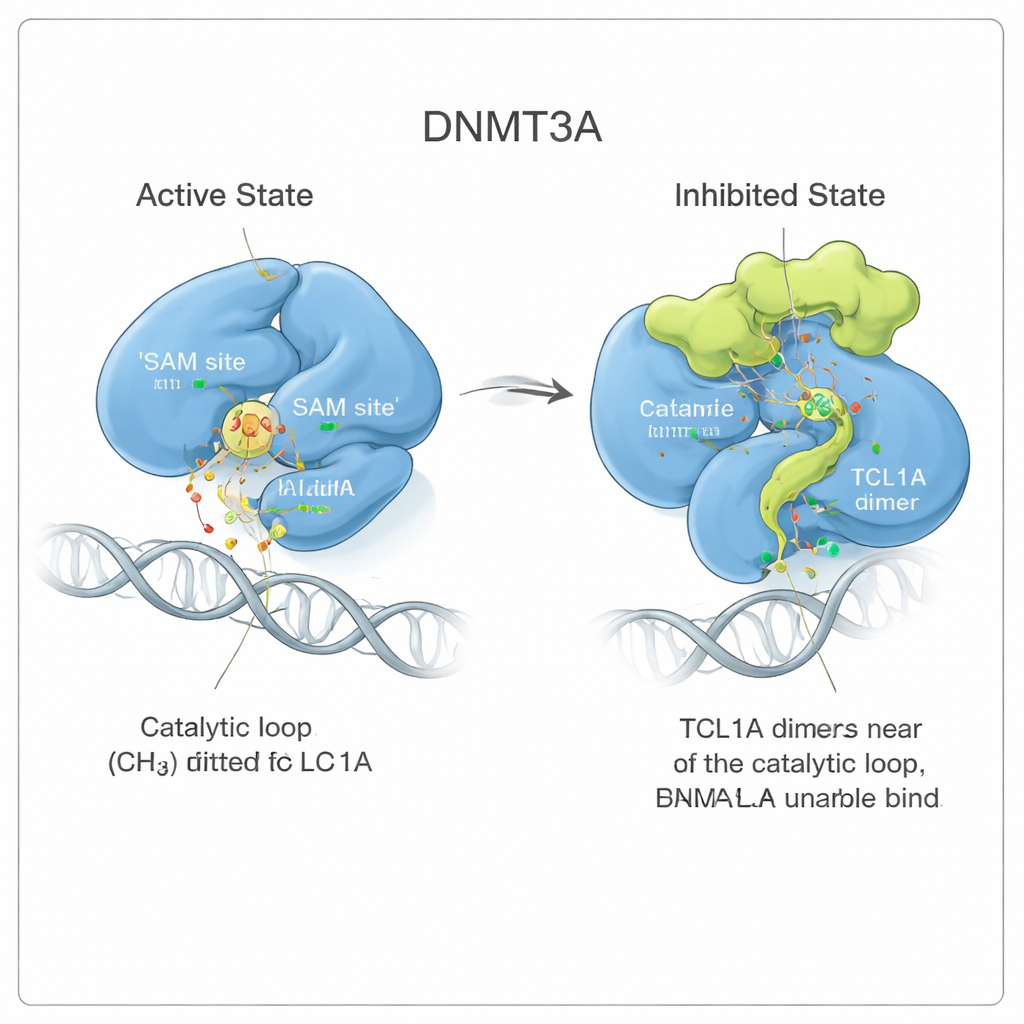
צפייה בחסימה דינמית בתנועה
כדי להבין עד כמה הקונפורמציה המעוכבת הזאת יציבה, המחברים הריצו סימולציות דינמיקה מולקולרית ארוכות, במידת מה תמונות תנועה פיזיקליות של המולקולות בסביבה ממוססת. כאשר DNMT3A היה קשור למפעיל שלו DNMT3L, הלולאה הקטליטית נשארה במקום הפעיל שלה. בנוכחות TCL1A, אותה לולאה הפכה לניידת הרבה יותר, מתנודדת אך תופסת שוב ושוב את כיס ה‑SAM כמו אצות ימיות השוצפות ועדיין מסתירות ניקוז. התנועה הקבועה הזו הקטינה את הנפח הזמין ל‑SAM יותר מעשרה־מונים, ותמכה במודל שבו TCL1A מנצל את הגמישות הטבעית של DNMT3A כדי לכפות צורת בלימה דינמית במקום חסימה נוקשה.
השלכות לתאים מתפתחים ולמחלה
הצוות לאחר מכן בדק מה החסימה המולקולרית הזו משמעותית עבור תאים אמיתיים. הם תכנתו תאי גזע עובריים של עכבר לייצר TCL1A אנושי בשלב שבו התאים בדרך כלל מגדילים את מתילציית ה‑DNA כשהם מתחילים להתמיין. מיפוי מתילציה ברמת הגנום הראה שתאים שמייצרים TCL1A בכמות גבוהה לא רכשו את רמת המתילציה הגבוהה הרגילה, בדומה במידה רבה לתאים שבהם שני הגנים Dnmt3a ו‑Dnmt3b הושבתו. גרסה מוטנטית של TCL1A שקושרת את האנזימים היטב פחות לא השפיעה כמעט כלל, מה שמדגיש שהאינטראקציה הפיזית היא המפתח. ממצאים אלה מקשרים בין המנגנון המבני לשינויים אפיגנטיים רחבי היקף בגנום.
מה משמעות הדבר לבריאות
במבט כולל, העבודה חושפת כיצד TCL1A יכול לפעול כבלם חזק על האנזימים שמניחים סימני מתילציה חדשים על ה‑DNA. על ידי עגינה בממשק קריטי, TCL1A משנה את מיקומן של לולאות גמישות ב‑DNMT3A וב‑DNMT3B כך שהן כבר אינן יכולות לקשור את תבנית ה‑DNA או את דלקן הכימי, מה שמוביל לאובדן גלובלי של סימני מתילציה בתאים. בהתפתחות נורמלית, ויסות עדין מסוג זה עשוי לסייע לאזן מתי והיכן מוסיפים מתילציה. כאשר TCL1A ממוקם במקומות הלא נכונים או מיוצר בכמות מוגזמת, כפי שקורה בסוגי סרטן דם מסוימים ובהפרעות רבייה נדירות, אותו מנגנון עלול לסטות את תוכנית האפיגנטיקה של התא. הבנת האינטראקציה ברזולוציה אטומית פותחת פתח לעיצוב מולקולות שידמות או ינגדו את השפעות TCL1A, ועשויות לשחזר דפוסי מתילציה בריאים.
ציטוט: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
מילות מפתח: מתילציה של DNA, DNMT3A, TCL1A, אפיגנטיקה, סרטן