Clear Sky Science · he
צמצום RAD23A מאריך חיים וממתן פתולוגיה בדגם עכבר של פתולוגיית החלבון TDP-43
מדוע המחקר הזה חשוב למשפחות ולחולים
צורות רבות של דמנציה ומחלות תאי מוטוריות, כולל טרשת צד-גבית ניוון שרירים (ALS) ודמנציה פרונטוטמפורלית (FTD), מערבות חלבונים בתאי המוח שמתעתקים בצורה לא נכונה, מתקבצים ומרעילים בהדרגה נוירונים. אחד החשודים המרכזיים הוא חלבון בשם TDP-43, שלרוב מסייע בניהול RNA אך נעשה רעיל כאשר הוא מצטבר. המחקר שואל שאלה מבשרת תקווה: האם ניתן לחזק תאי מוח על ידי הורדת רמתו של חלבון אחר, RAD23A, שמסייע בקביעת אופן הטיפול בחלבונים פגומים? החוקרים מראים בעכברים כי הורדת RAD23A יכולה להאריך חיים, לשפר תנועה ולהפחית נזק מוחי בדגם שמניע מחלה על ידי TDP-43, ומציגה כיוון חדש אפשרי לטיפול.
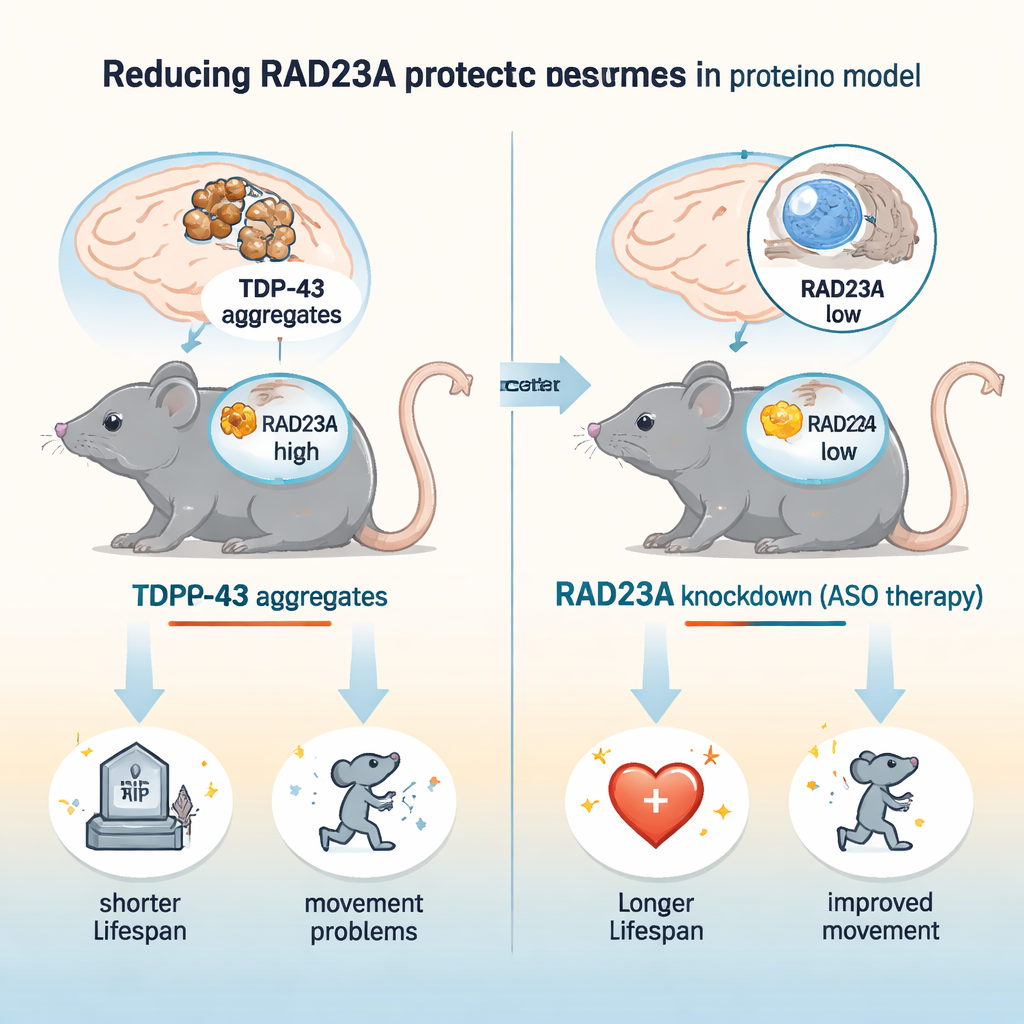
פקק תנועת חלבונים בתאים חולים
מחלות נוירודגנרטיביות מאופיינות לעתים על ידי ערימות של חלבונים מתעתקים שמכונת ההשלכה של התא אינה מצליחה לפנות. ב-ALS ו-FTD, TDP-43 יוצא מהגרעין, יוצר גושים דביקים ומסומן בכבדות באוביקוויטין, סמן שבדרך כלל מכוון חלבונים לפרוטאזום — המפרק המרכזי של התא. RAD23A הוא אחד ממספר חלבונים ממייני"ש ("שאטלים") שמסוגלים לשאת מטענים מסומנים באוביקוויטין אל הפרוטאזום. יחד עם זאת, עבודות קודמות בתולעים ובנוירונים בתרבית רמזו כי אובדן חלבונים דמויי RAD23 עשוי דווקא להגן מפני נזק המופעל על ידי TDP-43 — פרדוקס שהמחקר הנוכחי ביקש לחקור במוח יונק חי.
השבתת RAD23A בדגם עכבר של TDP-43
החוקרים השתמשו בדגם עכבר מבוסס היטב, המכונה TAR4/4, שמייצר באופן יתר חלבון TDP-43 אנושי בניוירונים ומפתח בעיות תנועה, עקמומיות של עמוד השדרה, רעד ומוות מוקדם — סימפטומים המשקפים תכונות מרכזיות של ALS/FTD. הם הורידו את RAD23A בשתי שיטות: על ידי הזרקת אוליגונוקלאוטידים אנטיסנס (ASOs) לגורים חדשים שהורידו את רמת ה-Rad23a RNA, ועל ידי הרביה של עכברים שנושאים השבתה גנטית מלאה של Rad23a. טיפול ASO יחיד קיצץ את רמות RAD23A במוח ובחוט השדרה בכ-75%. אצל עכברי ה-TDP-43, השתקת RAD23A האריכה את תוחלת החיים בכמעט 50% ועיכבה את הופעת וחומרת בעיות ההליכה, הרעד, העקמומיות של עמוד השדרה ואחיזת הגפיים האחוריות. מעניין כי אובדן גנטי מלא של RAD23A לא הוסיף תועלת נוספת, מה שמרמז כי הפחתה חלקית היא האופטימלית ושיעבוד מוחלט לטווח הארוך עלול להפעיל תגובות פיצוי.
פחות דלקת, טיפול חלבונים נקי יותר וגנום רגוע יותר
בדיקה מיקרוסקופית של הקורטקס המוטורי הראתה שעכברי ה-TDP-43 איבדו נוירונים ופיתחו הפעלה חזקה של אסטרוציטים ומיקרוגליה — תאי תמיכה וחיסון של המוח. הורדת RAD23A שימרה את מספר הנוירונים והפחיתה סמני דלקת ומוות תאי. ניתוחים ביוכימיים חשפו כי ייצור יתר של TDP-43 הציף את התאים בחלבונים מסומנים באוביקוויטין שאינם נספגים בממיסים (detergent-insoluble) ומשך יחידות פרוטאזום לתוך ההצטברויות הללו, מה שהחליש את יכולת התא לפנות חלבונים פגומים. הפחתת RAD23A הקטינה את העומס הכולל של חלבונים מואביקוויטנים, שמרה יותר פרוטאזומים בבריכה המסיסה והפעילה, והשיבה כמה סוגי פעילות פרוטאזום לקראת הנורמה. באותו זמן, השתקת RAD23A הקטינה גם את הצורות הכוללות והממורכזות של TDP-43, כולל שבר של 25 קילודלטון הרעיל במיוחד, והזיזה את TDP-43 מתוך הציטופלסמה בחזרה לכיוון הגרעין. ריצוף RNA ברמת הגנום הראה שאלפי שינויים בביטוי גנים שהופעלו על ידי TDP-43 הופחנו חלקית כאשר RAD23A הופחת, בייחוד גנים המעורבים בתפקוד נוירוני, ייצור אנרגיה מיטוכונדריאלי ונתיבים לניקוי הצטברויות כגון אגרפאג'י (aggrephagy).
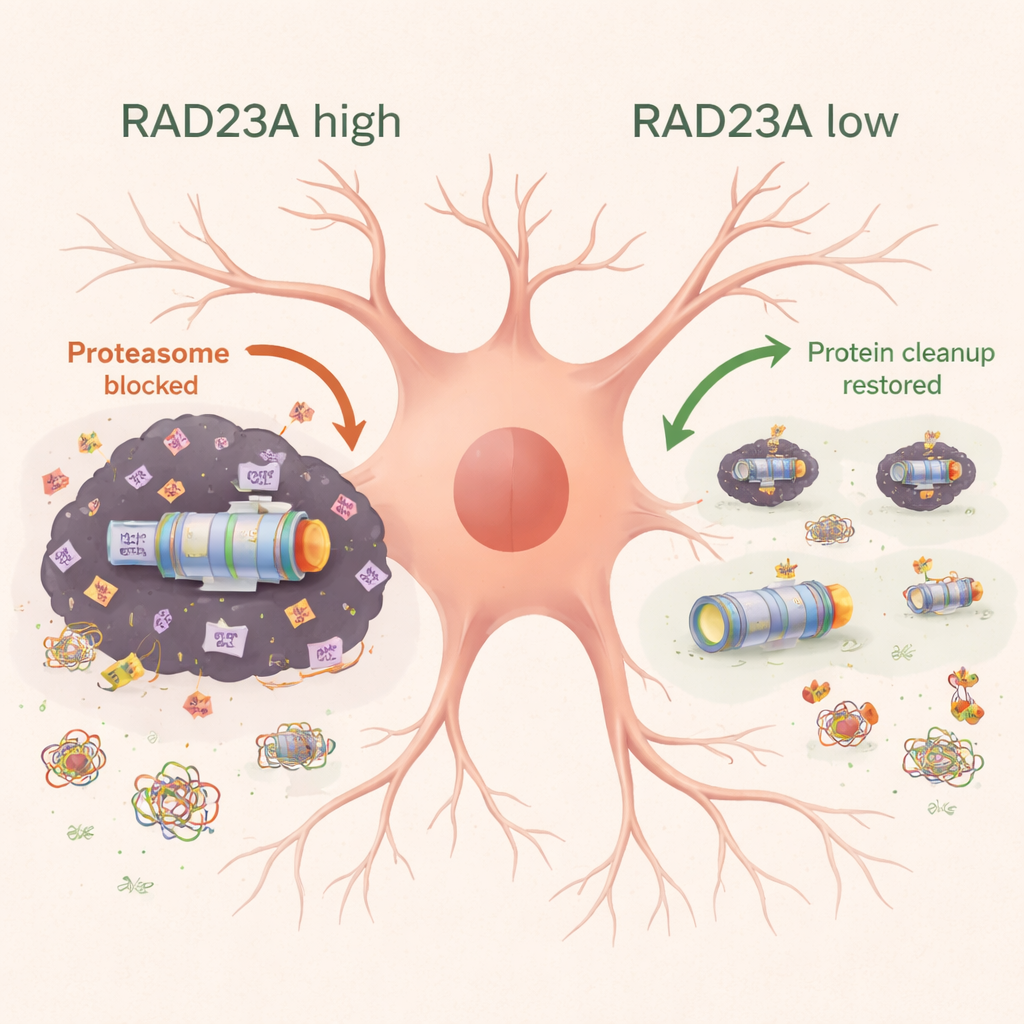
חידוש ה"פרוטאום הבלתי מסיס" החבוי
כדי לבחון ביתר פירוט את ההצטברויות העקשניות שמתנגדות לממיסים רגילים, השתמשה הקבוצה בספקטרומטריית מסה עם איזוטופים כבדים כדי למפות חלבונים שבולעו בחלק הבלתי מסיס של קורטקס העכבר. ביטוי של TDP-43 אנושי משך מרכיבי פרוטאזום, חלבוני שלד וצמתי תובלה ומכשור תאי נוסף. כשהורידו את RAD23A, הרכבו הכולל של הפרוטאום הבלתי מסיס השתנה: פחות חלבוני פרוטאזום ותובלה נתפסו בהצטברויות, בעוד שחלק מחלבוני הריבוזום וחלבוני הלחץ עלו בהצטברויות. ראוי לציין שהעיצוב הזה לא השתקף פשוט בשינויים ברמות RNA, מה שמרמז כי RAD23A משפיע בעיקר על אופן חלוקת החלבונים הקיימים בין מצבים מסיסים ומצטברים, ולא על כמות הייצור של כל חלבון.
מה זה עלול להצביע לגבי טיפולים עתידיים
ביחד, ממצאים אלה מציירים את RAD23A כתוונטור רב-עוצמה של בקרת איכות חלבונים בנוירונים תחת לחץ. בהורדה חלקית של RAD23A בדגם עכבר הנגרם על ידי TDP-43, המחברים הצליחו להפחית גושי חלבון רעילים, לשחזר את פעילות מערכת ההשלכה של חלבונים, להשקיט שינויים מזיקים בביטוי גנים, להגביל דלקת מוחית ולהאריך חיים ותפקוד מוטורי. מכיוון שהצטברות לא תקינה של TDP-43 רחבה הן בצורות תורשתיות והן בספורדיות של ALS, FTD והפרעות קשורות, מיקוד RAD23A בעזרת תרופות אנטיסנס תואמות-אדם עשוי להציע דרך להגן על נוירונים ללא חסימת TDP-43 עצמו, חלבון חיוני. למרות שנותרו הרבה בדיקות נוספות בדגמים אחרים ובבני אדם, עבודה זו מזהה את RAD23A כידית מבטיחה חדשה על נתיב משותף של נוירודגנרציה.
ציטוט: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
מילות מפתח: TDP-43, ALS, הצטברות חלבונים, פרוטאזום, טיפול אנטיסנס