Clear Sky Science · he
הבהרת השפעת אצטילציה בקצה ה‑N: מחלבון לפיזיולוגיה
איך תגיות כימיות זעירות יכולות לשנות את התנהגות החלבון
כל תא בגופך מלא בחלבונים שצריכים להתקפל כראוי, להגיע למקום הנכון, להתאסף למכונות מולקולריות ולהיות מוסרים כאשר הם פגומים. מאמר סקירה זה בוחן שינוי כימי עדין אך נפוץ מאוד בקצה אחד של חלבונים רבים — שנקרא אצטילציה בקצה ה‑N — ומראה כיצד «כובע» קטן זה מסייע לשלוט בכל דבר, מהגדילה התאית ומתגובות ללחץ ועד להתפתחות הלב ולתפקוד המוח.
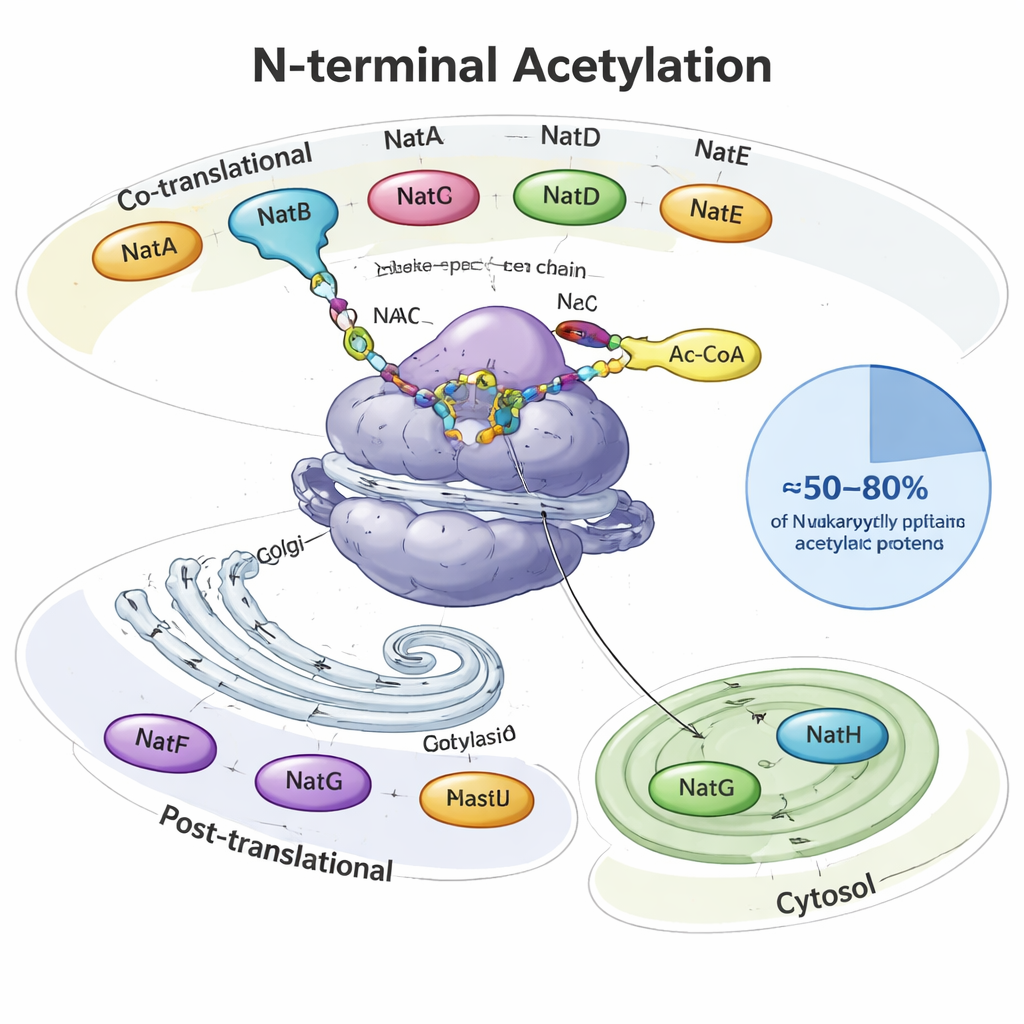
הכובע החלבוני שרובנו מעולם לא שמענו עליו
כאשר חלבון נוצק, הוא יוצא ממפעל החלבונים של התא — הריבוזום — כמו חוט שגדל. בתחילתו בדיוק — הקצה ה‑N — רבים מהחלבונים באאוקריוטים מקבלים קבוצת אצטיל, כובע זעיר של שתי פחמימות. אנזימים מתמחים הנקראים N‑terminal acetyltransferases (NATים) מבצעים את העבודה הזו, כשהם משתמשים במולקולה מטבולית משותפת (acetyl‑CoA) כמחזר. בשמרים, בצמחים ובבעלי חיים יש שמונה סוגי NAT עיקריים (NatA–NatH) שמחלקים את העבודה. חלקם פועלים בזמן שהחלבון עדיין מיוצר, אחרים עובדים לאחר מכן וממוקמים במקומות ייחודיים כמו מערכת הגולג'י או הפלסטידים של צמחים. יחד הם משנים בערך מחצי עד ארבע חמישיות מכלל החלבונים התאית, כשכל NAT מזהה רצפי התחלה מועדפים של שתי עד ארבע חומצות אמינו.
רבים מהאנזימים, כל אחד עם המומחיות שלו
NatA, NatB ו‑NatC הם העומסים הכבדים, פועלים ישירות בריבוזום ומכסים קטעים גדולים של «אצטילום הקצה‑N». NatA לבדה יכולה לשנות כ‑40% מהחלבונים האנושיים, בדרך כלל אלה שהמתיאונין הראשון שלהם נחתך. NatB ו‑NatC פועלים על חלבונים ששומרים על המתיאונין ההתחלתי שלהם, אך שונים בהעדפת חומצות האמינו השכנות. NATים אחרים בררניים יותר: NatD מתמקד בכמה היסטונים ספציפיים שאורזים את ה‑DNA, NatF מזהה חלבונים ממברנליים בגולג'י, NatG פועל בתוך הפלסטידים של צמחים, ו‑NatH (NAA80) משלים תהליך הבשלות המיוחד בשני שלבים על אקטין, מרכיב מרכזי של שלד התא. המאמר מאחד ממצאים מבניים וביוכימיים שמראים כיצד תתי היחידות הסייעות מעגנות אנזימים אלה לריבוזומים או ממברנות ומדייקות אילו חלבונים הם מבקשים.
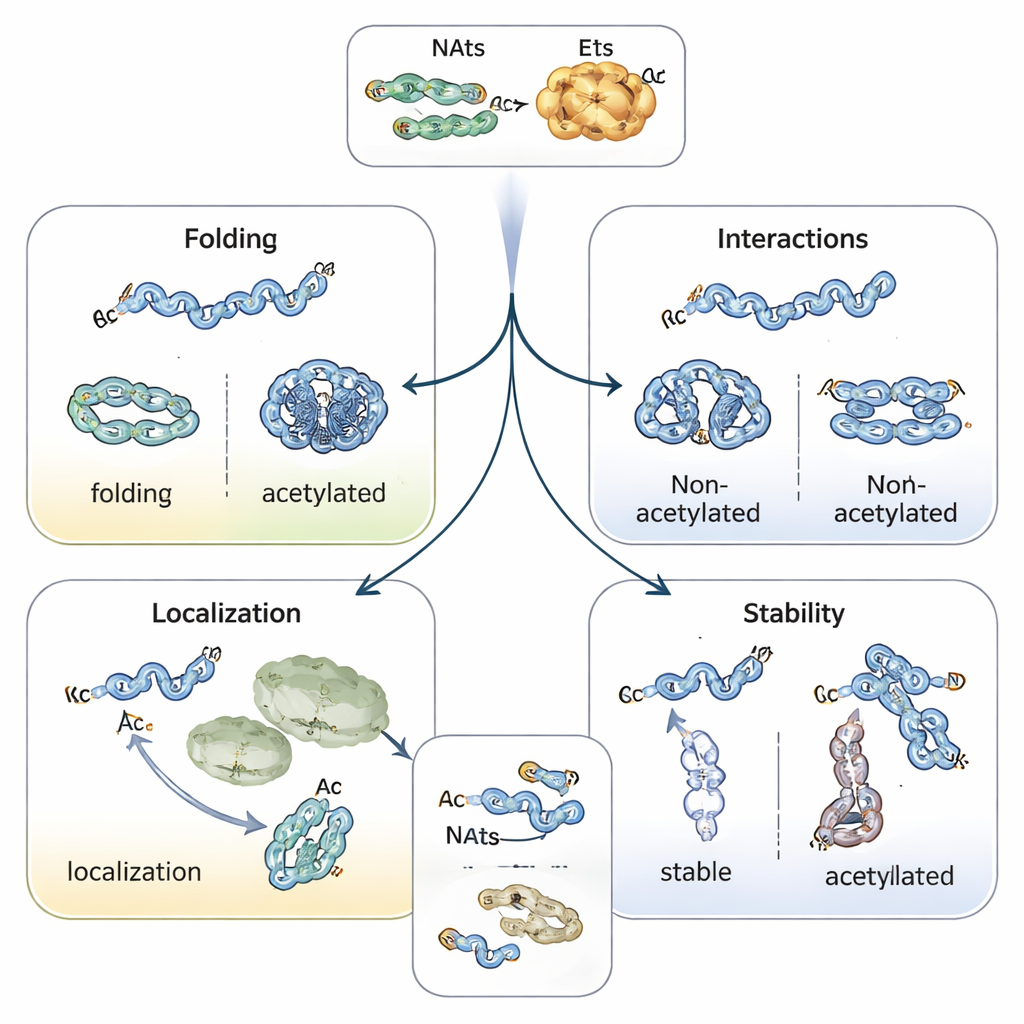
מנחים את קיפול החלבון, מיקומו ומשך חייו
הוספת כובע אצטיל משנה את הטבע הכימי של תחילת החלבון, לעתים מייצבת מבנים הֵלִיקִליים ומשפיעה על אופן קיפול החלבון. לדוגמה, החלבון המקושר לפרקינסון אלפא‑סינוקלאין נוטה להצטבר פחות ולאמץ צורה בטוחה יותר כאשר קצהו ה‑N אצטילט. טרופומיוזין, שותפו של אקטין, נקשר ומווסת את הסיבים של אקטין בצורה טובה יותר כאשר הוא מאצטל נכון. בצמחים ובחיות, אצטילציה בקצה ה‑N יכולה לשמש כסימן כתובת, המסייע לחלבונים למצוא כלורופלסטים, ליזוזומים או את הגולג'י. אולי השפעה הבולטת ביותר היא בתפקידו בקביעת אורך חיי החלבון: קצה N חשוף יכול להתקרא כ«אות לפירוק» על ידי אנזימים המתייגים באוביקוויטין, בעוד שאצטילציה יכולה להסתיר את האות ולייצב את החלבון — או, במקרים מסוימים, ליצור תו מותנה שמוכר רק כאשר החלבון מקופל לא כראוי או אינו מורכב נכון.
מפיזיולוגיה תאית להתפתחות ומחלה
מאחר שאצטילציה בקצה ה‑N נוגעת בכמות כה גדולה של חלבונים, פגיעה ב‑NATים גוררת השלכות רחבות על אורגניזמים שלמים. הוצאת NatA, NatB או NatC במינים מודליים לעיתים גורמת לפגמים התפתחותיים חמורים, לשינויים בתגובות ללחץ או אף למוות, בעוד שאנזימים מתמחים יותר כמו NatF ו‑NatH מציגים בעיות צרות יותר כמו שקיעת סידן במוח או אובדן שמיעה. בבני אדם, מוטציות מולדת בכמה גני NAT הן בסיס לתסמונות נדירות של התפתחות עצבית עם לקות אינטלקטואלית, מומים בלב או חולשת שרירים. אותה מכונה תדיר פעילות יתר בממקרים של סרטן, שם רמות NAT מוגברות מקושרות לפרוגנוזה ירודה ועלולות לקדם גדילת גידול, גרורתיות והתנגדות לטיפולים. שינויים באצטילציה בקצה ה‑N גם משפיעים על חלבונים הנוטים להצטברות כמו אלפא‑סינוקלאין והנטינגטין, וקושרים את המודיפיקציה למנגנונים של מחלות ניווניות עצביות.
כיוונים עתידיים ותקווה רפואית
המחברים מסכמים שבעוד שאנו כבר מכירים את רוב האנזימים המרכזיים שמוסיפים את כובעי ה‑N האלה, אנו עדיין מבינים רק חלק קטן מהמטרות החלבוניות הספציפיות וכללי הבקרה שלהם. נושא מרכזי הוא שאצטילציה בתחילת החלבון לעתים קרובות מShield אותו מהשמדה מוקדמת, ובאותו הזמן יוצרת אותות תלויי‑קונטקסט לבקרת איכות. זיהוי אילו ליגאזות אוביקוויטין קוראות אילו דפוסי קצה‑N וגילוי האם קיים אנזים שיכול להסיר כובעים אלה הם שאלות פתוחות מרכזיות. כיוון ש‑NATים יושבים בצלב דרכים של יציבות חלבונית, ויסות גנים ותגובות ללחץ תאי, מעכבי NAT סלקטיביים — ואולי כלים עתידיים שיכוונו אצטילציה בקצה ה‑N של חלבונים הקשורים למחלה — מתעדים ככיוונים מבטיחים לטיפולים חדשים בסרטן, במחלות לב ובניוון עצבי.
ציטוט: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
מילות מפתח: שינוי חלבוני, אצטילציה בקצה ה‑N, בקרת איכות חלבונים, מחלות ניווניות עצביות, ביולוגיה של סרטן