Clear Sky Science · he
CRISPR-AuNP: אופטימיזציה פיזיקוכימית של פלטפורמת ננו-חלקיקים זהב לעריכה גנטית לא-ויראלית, חסכונית ומודולרית בתאי גזע המטופויטיים
להביא את עריכת הגנים ליותר מטופלים
כלי עריכת גנים כמו CRISPR כבר שינו את חייהם של אנשים עם מחלות דם תורשתיות, אך הטיפולים עדיין יקרים, דורשים מיומנות טכנית רבה ונמצאים בעיקר במספר מרכזים מתמחים. מאמר זה מתאר שיטה חדשה להעברת CRISPR לתאי גזע מייצרי דם באמצעות חלקיקים זעירים מבוססי זהב שניתן להכין על בניין מעבדה תוך מספר שעות בלבד. המטרה היא להפוך שיטות עריכה גנטית עוצמתיות לפשוטות יותר, זולות יותר וקלים יותר לפריסה במקומות רבים בעולם.
למה חשובים תאי גזע של הדם
תאי גזע ומקורות יוצרים של מערכות הדם שוכנים במח העצם וממלאים באופן תמידי את כל סוגי התאים בדם. אם ניתן לתקן באופן בטוח מוטציות גורמות-מחלה בתאים אלה, טיפול חד-פעמי עשוי להעניק ריפוי לכל החיים למחלות כגון אנמיה חרמשית וחסרים חיסוניים מסוימים. כיום הדרך השכיחה ביותר להעביר CRISPR לתאים אלה מתבססת על אלקטרופורציה — תהליך המשתמש בפולסים חשמליים לפתיחת נקבים בממברנת התא. למרות שמדובר בכלי עוצמתי, האלקטרופורציה פוגעת בתאים, דורשת ציוד יקר וחומרים מיוחדים, ואינה קלה להיקף או לייצוא להגדרות עם משאבים מצומצמים. וקטורים ויראליים בטוחים מתאימים היטב לרבות מהתרפיות הגנטיות, אך הם פחות מתאימים להעברת CRISPR כי הם ממשיכים לייצר את כלי העריכה לפרקי זמן ארוכים מדי, מה שמגביר את הסיכון לשינויים לא-ממוקדים.
בניית נשא משל זהב זעיר
החוקרים שאפו לשפר מערכת ננו-חלקיקי זהב שתוארה קודם לכן ונשאה רכיבי CRISPR על פני השטח שלה. בעיצובים קודמים, ה-RNA המנחה את חלבון החיתוך של CRISPR עוגן ישירות על הליבת הזהב ואז הוצמד אליו חלבון Cas9. זה עבד סבירות עבור סוג אחד של אנזים CRISPR אך תפקד גרוע עם Cas9, שהוא מרכזי באסטרטגיות טיפוליות רבות. בבחינה מעמיקה של התנהגות Cas9 ו-RNA המנחה בתנאים חומציים המשמשים במהלך הרכבת החלקיקים, הצוות גילה כי דופלקס ה-RNA המנחה נהיה לא יציב על פני הזהב, מה שהוביל לכך שמעט או אין Cas9 פעיל שהוצמד לחלקיק. מיקרוסקופיה קונפוקלית גם רמזה כי הציפוי הפולימרי שנועד לסייע לחלקיקים לברוח ממחלקות תאיות התקלף לפני שהספיק לבצע את תפקידו.
עיצוב מחדש של הפלטפורמה בשלבים
כדי להתגבר על הבעיות הללו, המדענים בנו את המערכת מחדש משלוש שלבים. ראשית, במקום לעגן RNA חשוף לזהב ואז להוסיף חלבון, הם יצרו תחילה קומפלקסים של ריבונוקלאופרוטאין CRISPR (חלבון ועוד ה-RNA המנחה) לפני הבאתם במגע עם משטח הזהב. הם זיהו תנאי חומציות קלה שאיפשר לקומפלקסים אלה להיקשר לחלקיקים בעוד חלבון החיתוך נשאר פעיל. לאחר מכן הם עטפו את החלקיקים המועמסים בפולימרים מהונדסים באופן מיוחד ששילבו שרשראות בעלות מטען חיובי — הנחוצות לבריחה ממחלקות תאיות — עם מקטעי פוליאתילן גליקול גמישים הידרופיליים שמונעים הצטברות. באמצעות מדידות של גודל, מטען פני השטח ותכולת חלבון הם הראו שניתן לטעון בעקביות עשרות קומפלקסי CRISPR לכל חלקיק תוך שמירה על יציבות בתמיסה.
שבירת הגנות התא
אפילו עם טעינה משופרת, חלקיקי הדור השני עדיין התקשו במכשול מרכזי: הוצאת ה-CRISPR ממחלקות התא הפנימיות אל חלק התא שבו נמצא ה-DNA. לכן הצוות כיוונן בצורה שיטתית את הכימיה של שכבת הפולימר ואת היחס בין קבוצות החיוביות על הפולימר לקבוצות השליליות בקומפלקס ה-CRISPR. הם גילו שהוספת מספר גדול יותר של שרשראות פוליאתילן גליקול קצרות ומספר מבוקר של מעגנים המכילים גופרית שיפרה הן את יציבות החלקיקים והן את היכולת להפר את ממברנות האנדוזום מבלי להזיק לתאים. בעיצוב הסופי, הדור השלישי, הם יצרו תחילה קומפלקסים קומפקטיים של CRISPR ופולימר, ואז קישרו אותם לגרעיני זהב מרוכזים. מיקרוסקופיה אלקטרונית הראתה מעטפת דקה של CRISPR ופולימר סביב כל כדור זהב, וצילום בתאי גזע חיים אישר שהמטען יכול לברוח אל פנים התא ולהגיע לגרעין.
תוצאות העריכה עם כלים שונים של CRISPR
כדי לבחון עד כמה החלקיקים המותאמים עובדים, החוקרים כיוונו לגן בשם בטא-2-מיקרוגלובולין, המייצר חלבון הנמצא על פני כמעט כל תאי הדם וניתן למדודו בקלות על-ידי ציטומטריית זרימה. באמצעות פלטפורמת הזהב הדור השלישי הם הגיעו ליותר מ-10% שיבושים מדויקים של גן זה בתאי גזע ומקורות דם ראשוניים אנושיים — רמות שנחשבות משמעותיות עבור יישומים טיפוליים רבים — תוך שמירה על הישרדות גבוהה של התאים. אף על פי שהיעילות הזו נמוכה מזו שניתן להשיג באלקטרופורציה, מערכת הזהב לא דרשה ציוד מיוחד וגרמה למתח מזערי בתאים. חשוב מהבית, אותה פלטפורמה ניתנת לשימוש עם חלבוני CRISPR שונים, כולל Cas9, Cas12a ואנזים חדש יותר הנקרא Cas12a-M29-1, עם רמות עריכה דומות וללא רעילות ניתנת לזיהוי, מה שמבליט את אופייתה המודולרית של העיצוב.
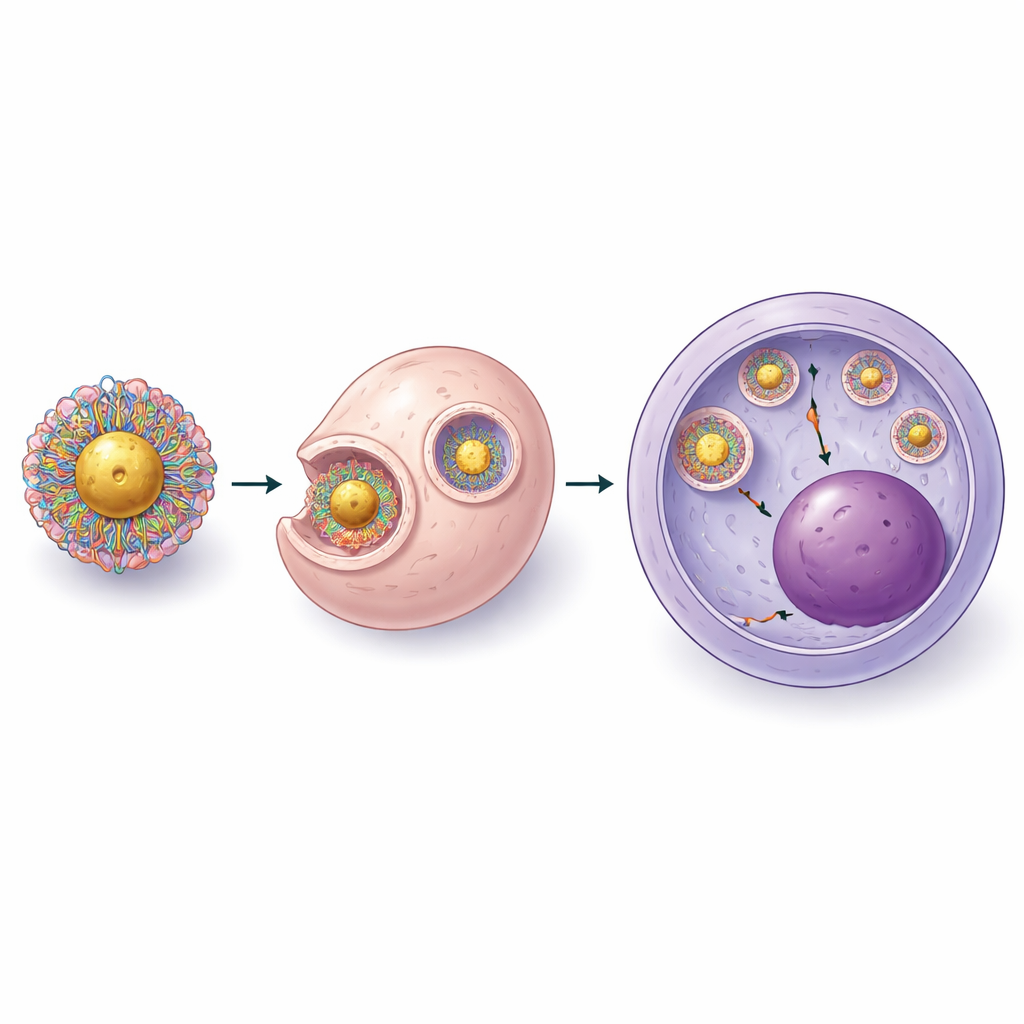
מה זה עשוי להעניק לטיפולים עתידיים
באופן פשוט, עבודה זו מראה שאפשר לבנות נשא קטן ומהונדס בקפידה מבוסס זהב שיכול להעביר כלי CRISPR לתאי גזע רגישים של הדם ללא חשמל או וירוסים, באמצעות חומרים זמינים במחיר של פחות משבעים דולר לכל מיליון תאים. בעוד נדרשות שיפורים נוספים כדי להתאים ליעילות של השיטות הקליניות הטובות ביותר כיום, במיוחד למחלות שמצריכות שיעורים גבוהים מאוד של תאים מתוקנים, פלטפורמה הנרכבת על הספסל מפחיתה מחסומים מעשיים לביצוע עריכות גנטיות מתוחכמות. עם המשך שיפור ובדיקות בטיחות, ננו-חלקיקים כאלה עשויים לעזור להפיץ את היתרונות של תרפיות מבוססות CRISPR מעבר למרכזים מתמחים, ולהפוך טיפולים מרפאים לנגישים יותר למטופלים ברחבי העולם.
ציטוט: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
מילות מפתח: עריכת גנים CRISPR, ננו-חלקיקים זהב, תאי גזע המטופואטיים, העברה לא-ויראלית, ננו-רפואה