Clear Sky Science · he
התמודדות עם קופרטוזיס: משינוי מטבולי לניצול טיפולי בסרטן
כשמתכת מועילה פונה נגד הסרטן
נחושת ידועה בעיקר כחומר בחוטים חשמליים ובצנרת, אך היא זורמת גם בתאי הגוף שלנו בצורה דיסקרטית, מסייעת לאנזימים לייצר אנרגיה ולהגן מפגיעה. מאמר סקירה זה בוחן תפנית מפתיעה: בתנאים המתאימים, עודף נחושת יכול לדחוף תאי סרטן לסוג מיוחד של מוות. הבנת התהליך—"קופרטוזיס"—עשויה לפתוח דרכים חדשות לטיפול בגידולים ששרדו טיפולים סטנדרטיים.
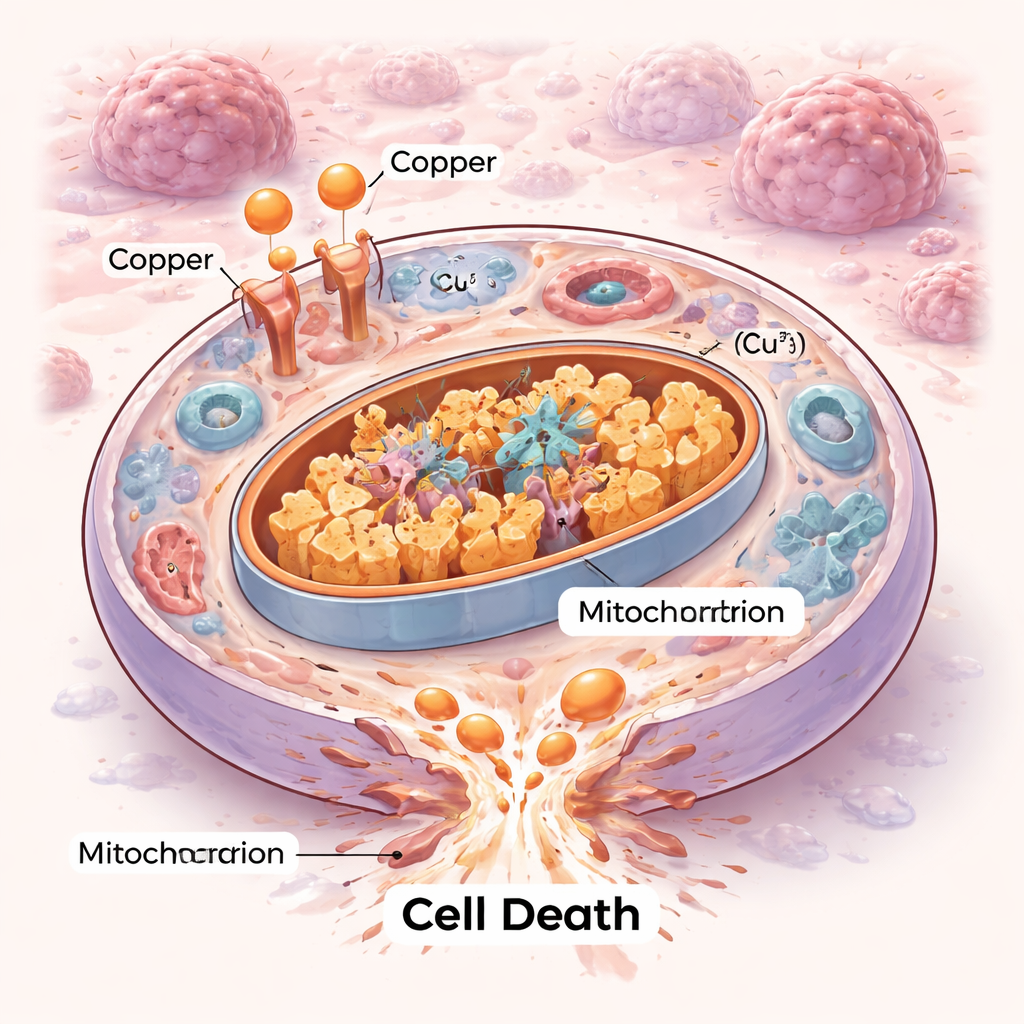
דרך חדשה שבה תאים יכולים למות
תאים לא כולם מתים באותו האופן. במשך עשורים מדענים מיפו תכניות הרס עצמי מסודרות כמו אפופטוזה וצורות חדשות כגון פרוטופטוזיס (ferroptosis). הקופרטוזיס מוסיפה פרק חדש. כאן, עודף נחושת מציף את תחנות הכוח של התא—המיטוכונדריה—ומקשר לאנזימים מטאבוליים ספציפיים שאמורים לשרוף דלק. הקישור גורם לאותם אנזימים להיגרם לצבריונים ולחוסר יציבות של רכיבי ברזל–גפרור שהמיטוכונדריה זקוקה להם. התוצאה היא סוג של פקק תעבורה פנימי והתמוטטות מכנית שהאחד התא אינו מצליח לתקן, ומסתיימת במוות הנגרם מלחץ פרוטאוטוקסי במקום מסלולי התאבדות קלאסיים.
כיצד תאי סרטן שומרים על נחושת ואנרגיה
מאחר שנחושת גם חיונית וגם מסוכנת, תאים מתפעלים רשת לוגיסטית מתוחכמת להובלתה בבטחה. מעבירים ייעודיים מכניסים נחושת לתא, חלבוני צ'פרון מוליכים אותה למיטוכונדריה וליעדים אחרים, ומולקולות אחסון כמו מטלוטיונאינים וגלוטתיון סופגות כל עודף. גידולים לעתים קרובות משנים מחדש מערכת זו. חלק מגדילים את היבואנים או הצ'פרונים כדי להזין את הביקוש האנרגטי הגבוה שלהם; אחרים מעלים יצואנים או חלבוני אחסון כדי להימנע מעודף נחושת. בו בזמן, סרטנים רבים מעבירים את המטבוליזם שלהם—מתחלפים בין שריפת סוכרים על פני התא לבין נשימה מיטוכונדריאלית עמוקה יותר. הסקירה מסבירה שהקופרטוזיס פוגע בחומרה רבה יותר בתאים שעדיין תלויים במיטוכונדריה, מה שהופך גידולים עם פרופיל מטבולי זה לפגיעים במיוחד.
מתגי מאסטר שמכוונים רגישות לנחושת
"מחליטים" תאיים מרכזיים משפיעים על האפשרות שהקופרטוזיס תתרחש. לדוגמה, הדומע הגידולי p53 נוטה לדחוף תאים הרחק מתסיסת סוכר מהירה לעבר שימוש מסודר יותר בדלק במיטוכונדריה. בכך, ובשינוי הטיפול באנזימי קשירת נחושת, p53 יכול להפוך סרטן לפגיע יותר למוות המושרש בנחושת—בעוד שצורות מוטנטיות של p53 לעתים עושות את ההפך. לעומת זאת, גורם ההיפוקסיה HIF‑1α, המופעל בליבות גידול עניות בחמצן, מסייע לתאים להימלט מקופרטוזיס על ידי דיכוי אנזימים מיטוכונדריאליים מרכזיים והגברת מגן הקשור לנחושת. מסלולים אחרים, כגון Wnt/β‑catenin ו‑AKT, מקדמים עמידות על ידי הגברת יצוא נחושת או שינוי כימי של חלבונים קריטיים כך שבניו כבר לא יגיבו לעודף נחושת. יחד, רשתות אלו פועלות כמו תרמוסטטים, מגבירות או מורידות את רגישות הגידול לטיפולים מבוססי נחושת.
נחושת, המערכת החיסונית והעברת תרופות חכמה יותר
תפקיד הנחושת אינו מוגבל להריגת תאים סרטניים ישירות; היא גם מעצבת את הנוף החיסוני סביב הגידולים. מתח נחושת מבוקר יכול להפוך תאים סרטניים גוססים ל"גלויים" יותר, לשחרור אותות סכנה המגייסים ומפעילים תאי T, תאי דנדריט ומקרופאגים. נחושת יכולה גם להשפיע על רמות נקודות עצירה חיסוניות כמו PD‑L1, שהגידולים משתמשים בהן כדי לכבות תאי T אנטי‑סרטן, מה שמרמז על אפשרויות לשלב תרופות הממוקדות נחושת עם אימונותרפיות מודרניות. מאחר שנחושת חופשית עלולה להזיק לרקמות בריאות, חוקרים מפתחים כלים מדויקים—יונופורים קטני מולקולה שמוליכים נחושת סלקטיבית לתאי סרטן, ופלטפורמות ננודרמה המכילות נחושת או תרופות מונעות נחושת בתוך חלקיקים ממוקדים או הידרוג'לים. טכנולוגיות אלה שואפות להעלות את רמות הנחושת לרמות קטלניות בתוך הגידולים תוך שמירה על שאר הגוף בטווח בטוח.
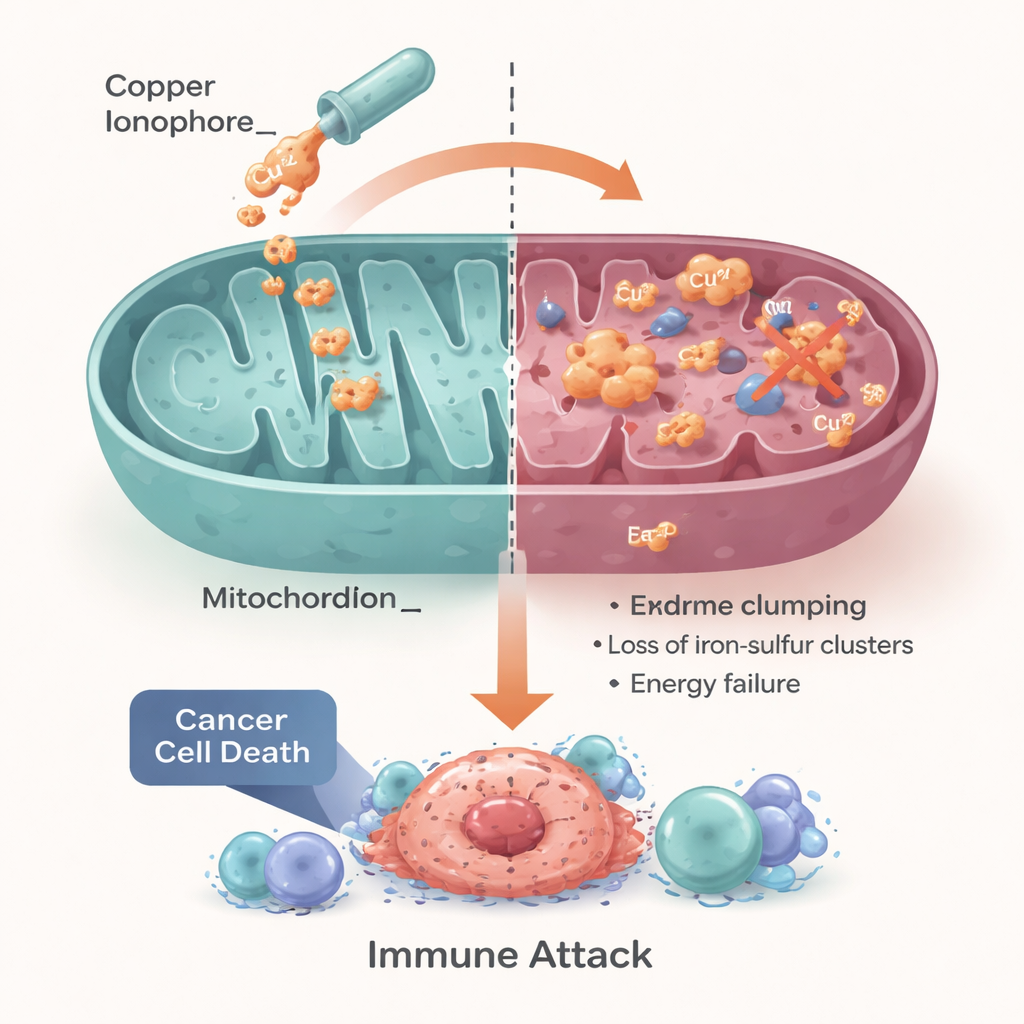
להפוך חולשה תאית לטיפול
המחברים מסכמים שקופרטוזיס הופכת צורך תאי בסיסי—ניהול זהיר של נחושת ואנרגיה—לעקב אכילס פוטנציאלי של הסרטן. גידולים עם טיפול נחושת מופרע או תלות מופרזת במטבוליזם מיטוכונדריאלי עשויים להיות רגישים במיוחד לאסטרטגיות מבוססות נחושת, כולל תרופות בעלות שימוש מחודש כמו דיסולפיראם ואלסקלומול, וכן ננו־חלקיקים מדור הבא. עם זאת, הם מדגישים שהצליחה תלויה בהתאמת החולים המתאימים לגישה הנכונה, באמצעות סימנים ביולוגיים שמתארים מעבירים של נחושת, פעילות מיטוכונדריאלית ומצב חיסוני וחמצוני של הגידול. אם מחסומים אלה יוסרו, ניצול הקופרטוזיס יכול להעניק לאונקולוגים מנוף חדש מונע מתכת לטיפול בגידולים שיש להם כיום מעט אפשרויות טובות.
ציטוט: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
מילות מפתח: קופרטוזיס, מטבוליזם הנחושת, טיפול בסרטן, מטבוליזם של גידול, אימונותרפיה בסרטן