Clear Sky Science · he
כוח מגנטו‑מכני דינמי בליזוזומים מעורר הפעלה מתמשכת של מאקרופאגים לחיסון נגד גידולים
שימוש בכוחות עדינים כדי להעיר את המערכת החיסונית
סרטן לעתים קרובות שורד על ידי השתקת מנגנוני ההגנה של הגוף. המחקר הזה בוחן דרך לא צפויה להעיר אותם מחדש: על‑ידי משיכת מרכיבים זעירים בתוך תאי החיסון בעזרת ננו‑חלקיקים מונעי מגנט. במקום להסתמך רק על תרופות, החוקרים משתמשים בכוחות מכניים מכוונים בתוך התאים כדי לתכנת מחדש תאי חיסון הנקראים מאקרופאגים למלחמה ממושכת בגידולים.
מדוע גידולים מוצקים קשים לטיפול
אימונותרפיות מודרניות לסרטן, כמו נוגדנים החוסמי‑נקודות בדיקה ותאי חיסון מהונדסים, שינו את הטיפול בחלק מסוגי סרטן הדם. עם זאת, עבור רבים הסובלים מגידולים מוצקים כמו סרטן הריאה, שיטות אלה מסייעות רק למיעוט. סיבה מרכזית לכך היא הסביבה המיקרית של הגידול. גידולים מוקפים בנישה מגינה מלאה בתאים ואיתותים שמדכאים את החיסון. מאקרופאגים, שיכולים לתקוף גידולים (מצב דמוי M1) או לתמוך בהם (מצב דמוי M2), לעתים נדחפים למצב M2 התומך בגידול. הפיכה של התכנות ה"רע" הזה באופן יציב הייתה מאתגרת באמצעות תרופות ביוכימיות קונבנציונליות בלבד.
הפיכת ננו‑חלקיקים למנועים מכניים זעירים
הצוות תכנן ננו‑מנועים מגנטיים—חלקיקים בקנה‑מידה ננומטרי של תחמוצת ברזל מומסת באבץ ומצופים בפולימר בעל מטען חיובי—שנבלעים בקלות על‑ידי מאקרופאגים ומצטברים בליזוזומים, מרכזי המיחזור והאותות של התא. לאחר כניסתם, שדה מגנטי מסתובב חיצוני גורם לחלקיקים להתיישר לשרשראות בצורת מוט ולהסתובב, מערבל את הנוזל הצמיג בתוך הליזוזומים ויוצר מערבולות זעירות. סימולציות ממוחשבות וניסויי ממברנות מדגם הראו כי בעזרת כוונון תדירות הסיבוב ניתן להגדיר את מאמץ הגזירה על ממברנת הליזוזום לנקודת איזון: חזקה דיו כדי לגרום לדליפה רגעית של הממברנה, אך לא חזקה עד כדי הרס קבוע.
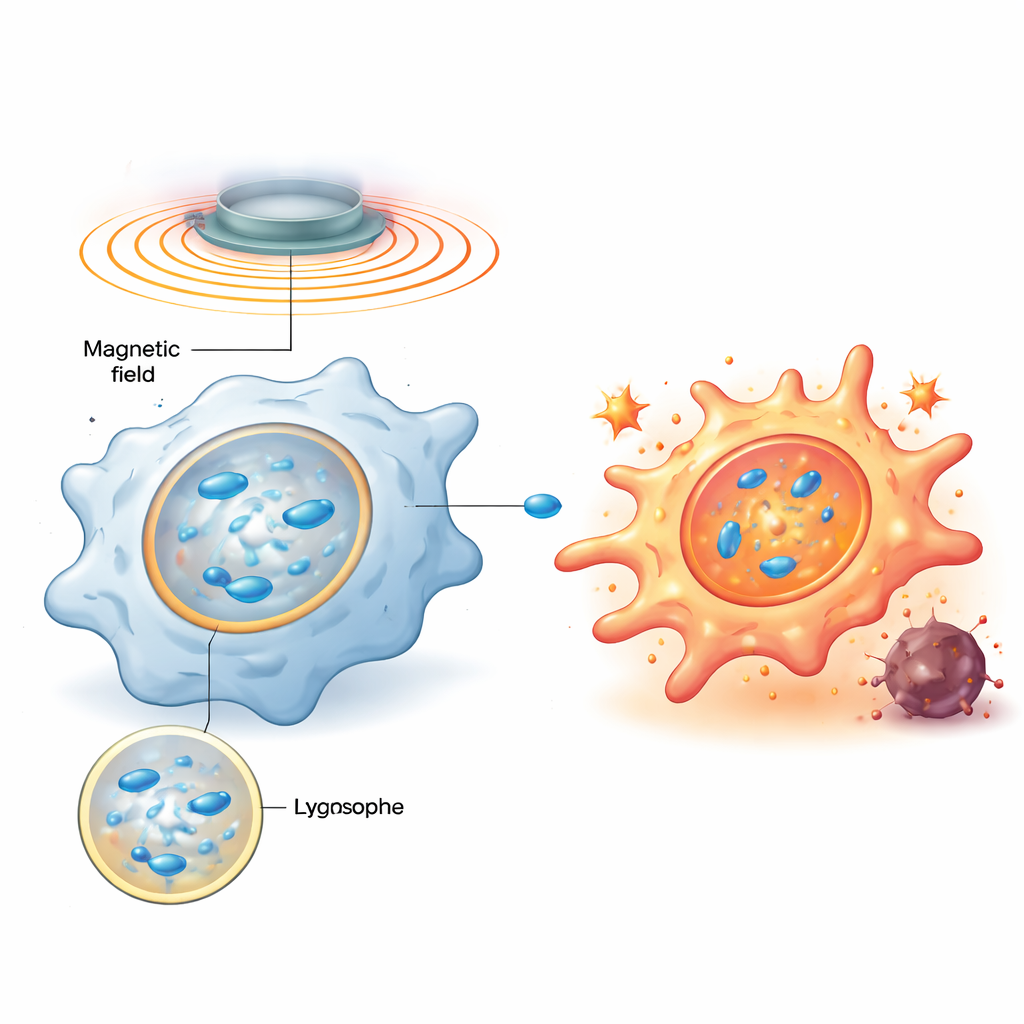
דחיפה מכנית מפעילה אזעקה ביוכימית
כאשר ממברנת הליזוזום מופרעת לרגע, חלבון קושר‑סוכרים בשם גלקטין‑9 נוטל אל הנקודות הפגועות, ופועל כחיישן ללחץ המכניקלי הזה. המחקר מראה שפעולה זו מפעילה בתורה אנזים מרכזי החושף את מצב האנרגיה של התא, AMPK, שאז מגביר את מסלול האיתות NF‑κB—ידוע בהנעת תגובות דלקתיות ואנטימיקרוביאליות. יחד, האותות האלה משנים את המטבוליזם של המאקרופאגים ממצב שקט וחסכוני דלק לגליקוליזה מהירה, דפוס המקושר להתנהגות עוינת דמוי M1. חשוב שגם כשהשדה המגנטי מכובה, הליזוזום מתקן את עצמו והאותות נחלשים; כאשר השדה חוזר מאוחר יותר, אותו מסלול מופעל מחדש. מחזוריות תכנותית זו של הדלקה וכיבוי מאפשרת לחוקרים "להקיש" על אותו מתג מכני שוב ושוב מבלי להרוג את התאים.
חינוך מחודש של מאקרופאגים ללחום בגידולים
בתרביות תאים, חדירת הליזוזומים המושרת מגנטית—תהליך שכונו MagLMP—החזירה מאקרופאגים שנדחפו למצב תומך‑גידול דמוי M2 חזרה למצב פרו‑דלקתי דמוי M1. תאים שעודכנו כך ייצרו יותר ציטוקינים דלקתיים ושמרו על הפרופיל דמוי M1 למשך ימים, אפילו בתמיסות גידול שמקובל שדוחפות אותם לכיוון M2. במודלים עכבריים של גידול, הכנסת ננו‑מנועים מגנטיים אל תוך הגידולים ויישום מחזורים יומיים של השדה המסתובב האטו את גדילת מספר סוגי סרטן. כאשר מאקרופאגים הושמטו לניסוי, התועלת נעלמה ברובה, מה שמראה שתאים אלה הם מרכזיים להצלחת הטיפול. רצף RNA חד‑תאי מרקמת הגידול חשף ש‑MagLMP הגדיל את החלק היחסי של מאקרופאגים דמויי M1, הגביר נויטרופילים אנטי‑גידוליים ותאי CD8 אפקטוריים, ובעת ובעונה אחת העלה ביטוי גנים הקשורים ל‑NF‑κB ולגליקוליזה בתוך המאקרופאגים.
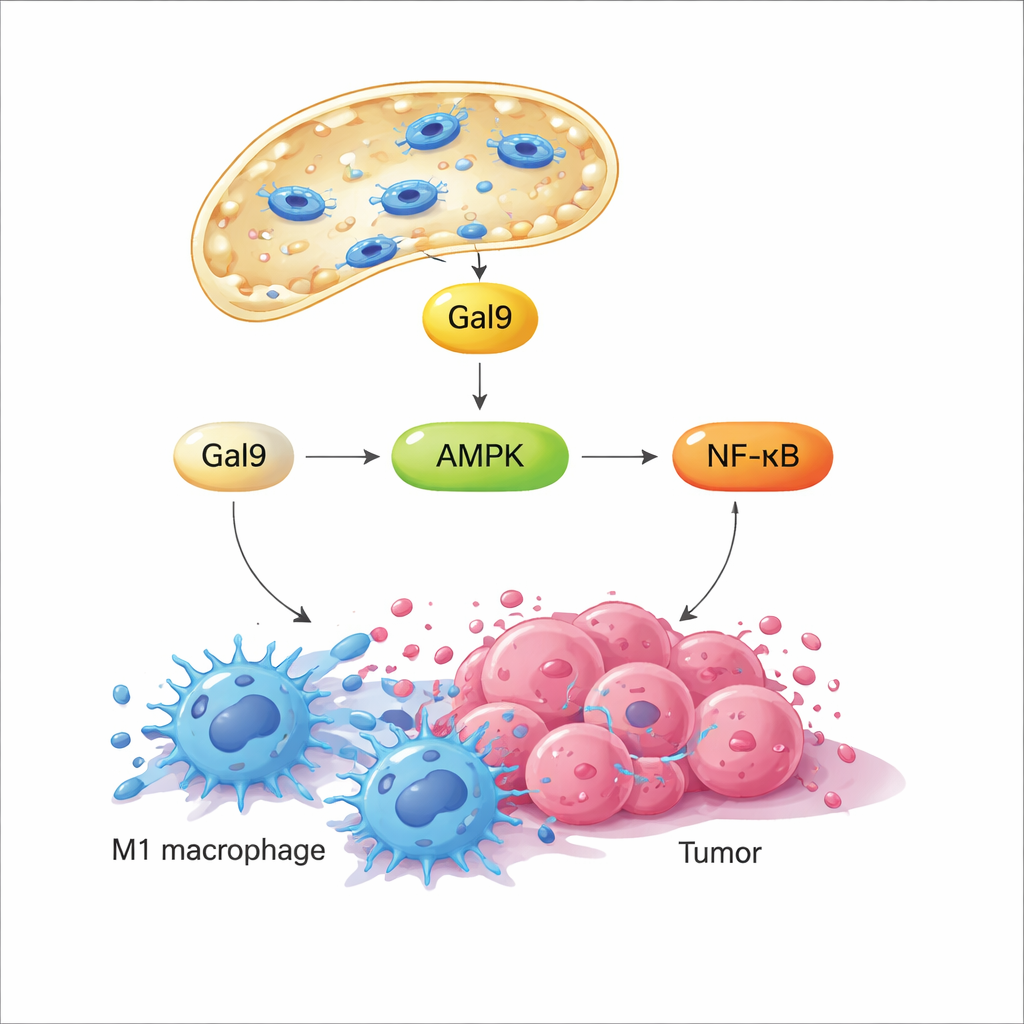
משליטה מקומית לטיפול מערכתית
החוקרים שאלו לאחר מכן האם גישה זו יכולה לפעול כמו טיפול בעולם האמיתי, המינתר דרך מחזור הדם. הם הזריקו את הננו‑מנועים תוך‑שורית ושתמשו במגנט חיצוני פשוט כדי לרכזם בתוך הגידולים, והפגינו קליטה יעילה על‑ידי מאקרופאגים במצע הגידולי. טיפול MagLMP לאחר מכן שוב הזיז את המאקרופאגים לכיוון מצב דמוי M1 ועיכב את הגדילה. במודל עכבר של סרטן ריאה בשלבים מוקדמים שגדל בתוך הריאה עצמה, שילוב של הנחיית מגנטית עם MagLMP מחזורי הוביל להארכת חיי בעלי‑משמעות: כ‑שליש מהעכברים המטופלים חיו למעלה מ‑300 ימים, בהשוואה לשבועות בלבד בחיות הביקורת. שילוב של MagLMP עם מעכב נקודת‑בדיקה PD‑1 חיזק עוד יותר את השליטה בגידול במודלים קשים לטיפול.
דרך חדשה לשלוט בחיסון מבפנים החוצה
העבודה הזו מראה כי כוחות מכניים זעירים ומבוקרים היטב בתוך אברון ספציפי ניתנים לניצול כדי לנווט את ההתנהגות החיסונית בחיות חיות. על‑ידי "דקירה" חוזרת והפיכה של הליזוזומים, MagLMP מפעיל ציר גלקטין‑9–AMPK–NF‑κB שמתכנת מחדש מאקרופאגים ללוחמים עמידים נגד הגידול מבלי להזיק בתרחב לתאים. עבור לא‑מומחים, הרעיון המרכזי הוא שרמזים פיזיקליים—המופעלים על‑ידי ננו‑מנועים מונעי מגנט—יכולים לפעול כמו חייגן על מערכת החיסון, ומציעים מחלקה חדשה של כלים שיכולה להשלים תרופות באימונותרפיות עתידיות לסרטן.
ציטוט: Li, Y., Zheng, M., Zhu, Z. et al. Dynamic magneto-mechanical force in lysosomes induces durable macrophage repolarization for antitumor immunity. Cell Res 36, 197–218 (2026). https://doi.org/10.1038/s41422-025-01217-1
מילות מפתח: אימונותרפיה לסרטן, רפרוגרמינג של מאקרופאגים, ננו‑חלקיקים מגנטיים, מכנוטרנסדוקציה, אותות מליזוזום