Clear Sky Science · he
ווריאנטים מאבדים‑תפקוד ב‑ODAD1 משבשים עיגון ODA ומעוררים עיצוב מחדש של השלד הציטוסקלטלי באקטין בדי חלקית בתסמונת דיסקינזיה של ריסים ראשונית
כשהמברשות המיקרוסקופיות של הגוף מתקלקלות
כל נשימה שלך תלויה בצבאות של מבנים זעירים בדמיון שיער הנקראים ריסים, שמטאטאים ריר, חיידקים ואבק מדרכי הנשימה. אצל אנשים עם מצב תורשתי נדיר הנקרא דיסקינזיה של ריסים ראשונית, או PCD, המברשות המיקרוסקופיות האלה אינן פועלות כראוי, מה שמוביל לשיעולים עיקשים, זיהומי ריאות ולפעמים להיפוך מיקום האיברים בגוף. מחקר זה חושף כיצד שינויים מזיקים בגן יחיד, ODAD1, לא רק משביתים את המנועים הפנימיים של הריסים אלא גם, באופן בלתי צפוי, משנים את שלד התמיכה של התאים שמכילים אותם — וחושפים נקודת תורפה חדשה שעשויה להיות ניתנת לטיפול תרופתי.
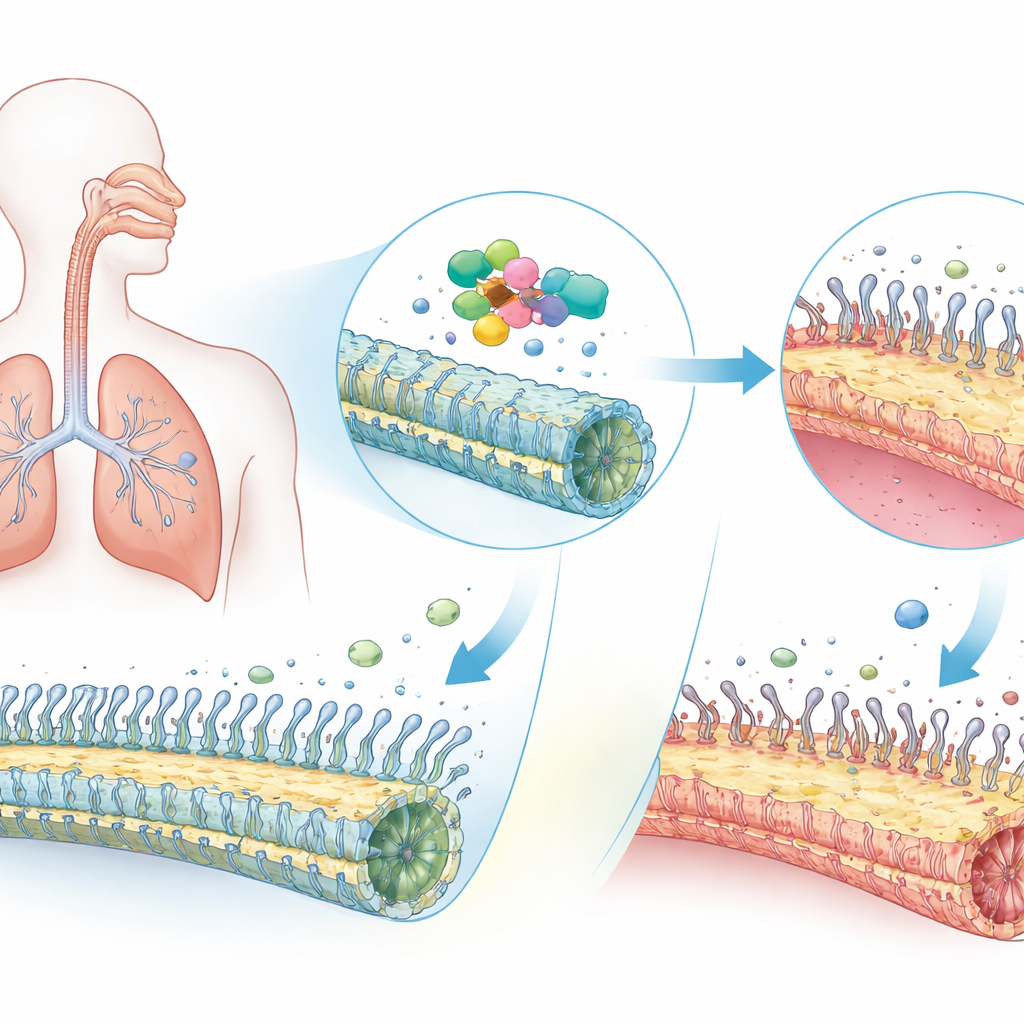
מחלה ריאתית נדירה עם השלכות משמעותיות
PCD משפיעה על בערך אחד ממספר אלפים אנשים ברחבי העולם ולעתים קרובות מופיעה בילדות. מכיוון שהריסים המצפים את האף והריאות אינם יכולים להכות באופן יעיל, ריר ומיקרובים כלואים ונשארים, מה שמניע בעיות סינוס כרוניות, זיהומי אוזניים ונזק ריאתי מתקדם. רבים מהחולים גם מציגים "סיטוס אינברסוס", שבו הלב ושאר האיברים מסתדרים בהיפוך שמאל‑ימין — סימן לכך שהריסים נכשלו בכיוון של תוכנית הגוף בעובר. רופאים ידעו זמן מה שמנגנונים פגומים בעשרות גנים שונים יכולים לגרום ל‑PCD. ODAD1 הוא אחד מהגנים הללו ועוזר לעגן את המנועים המולקולריים שמניעים את התנועת השוט של כל ריס. אך המדענים לא הבינו במלואם כיצד ליקויים ב‑ODAD1 מתבטאים בתוך רקמת דרכי הנשימה האנושית.
מיפוי גן פגום בתאי מטופלים
החוקרים חקרו תשעה פרטים משבע משפחות חאן‑סיניות שהציגו סימנים קלאסיים של PCD: בעיות נשימה בנעורים, שיעול רטוב לכל החיים, זיהומי ריאות תכופים ורמות ניטריק אוקסיד נמוכות באופן יוצא דופן באוויר הנשוף — סימן קליני של המחלה. בדיקות גנטיות חשפו ארבע גרסאות מזיקות של גן ODAD1, כולל אחת שמעולם לא תועדה קודם. כל הגרסאות הפגומות צמצמו קשות או הבטלו את חלבון ODAD1 התקין בתאי אפיתל האף. כאשר הצוות צילם ריסים ממדגם המטופלים במהירות גבוהה, הם ראו שהתנועה החלקה והגלית הרגילה הוחלפה בריצוד חלש ואי‑מאורגן. תרביות מעבדה שגודלו מתאים אלה, שמשחזרות שכבה דקה מצופה ריסים בממשק אוויר‑נוזל, הראו את אותה תנועה איטית וחסרת תיאום.
בתוך המיקרו‑מכונות השבורות
כדי לראות מה היה פגום פיזית, המדענים השתמשו בטכניקות הדמיה עוצמתיות. מיקרוסקופיה אלקטרונית סטנדרטית ומיקרוסקופיה קריו‑אלקטרונית מתקדמת גילו כי יחידות המנוע החיצוניות ואת אתרי העיגון שלהן חסרו לחלוטין בריסי המטופלים. במקרים מסוימים גם מבנים מרכזיים אחרים בגרעין הריס הוזזו או היו מעוותים. פגמים אלה מסבירים מדוע הריסים אינם יכולים ליצור כוח מספיק להזיז את הריר. עם זאת, הנזק עבר את גבולות הריסים עצמם. השטח האפי־תאי בתרביות שמקורן במטופלים הכיל הרבה פחות תאים מרובי‑ריסים, והתאים שנותרו היו מרווחים באופן מוזר ומוגדלים, כאשר הריסים שלהם פונים בכיוונים מעורבים. בהפתעה, מספר ה"גופים הבזאליים" הפנימיים בכל תא — הזרעים שממנו צומחים הריסים — היה תקין, מה שמרמז שהבעיה נעוצה באירגון התאים על פני הרקמה ולא בכמות הריסים שהם ניסו לבנות.
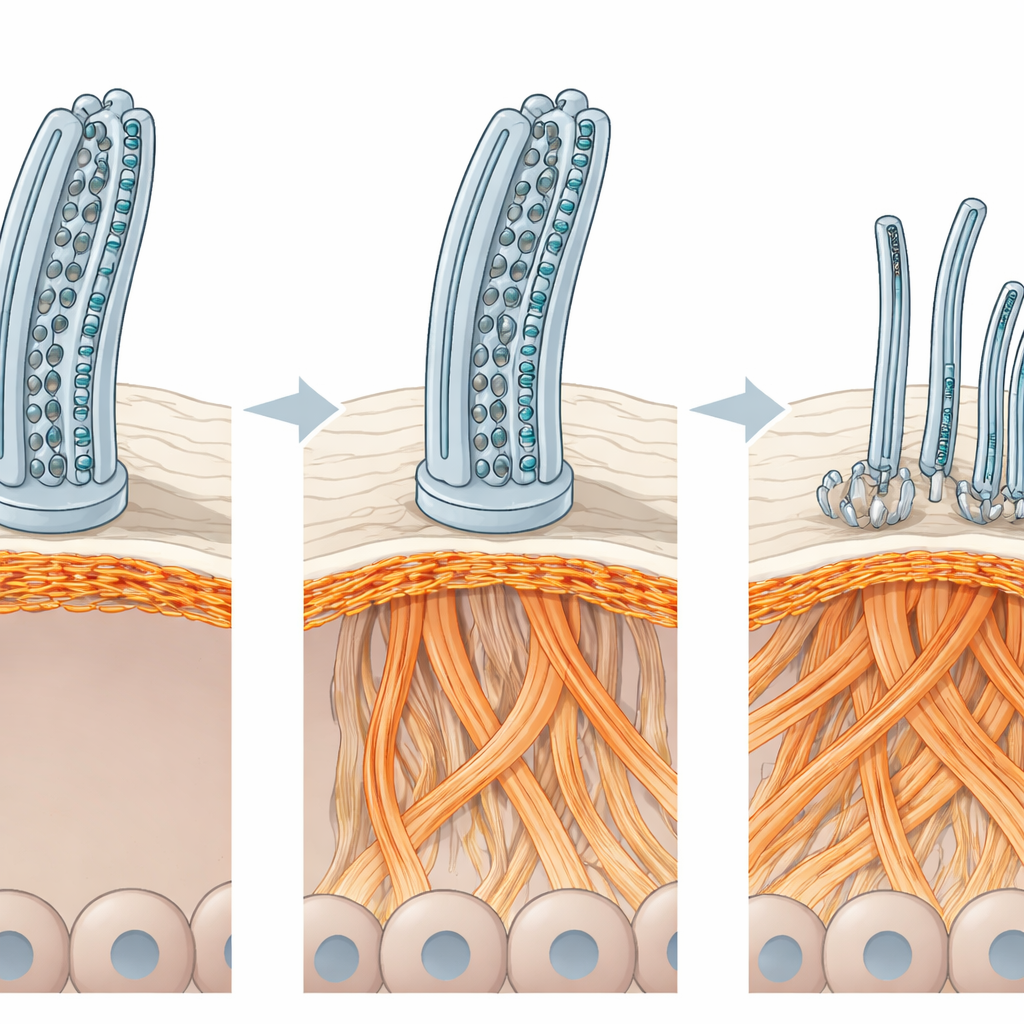
השלד הפנימי של התא עובר חיבור מחדש
כדי לדייק מה מפר את הארגון הזה, הצוות מדד אלפי חלבונים בתרביות דרכי הנשימה שמקורן במטופלים. בעוד שחלבונים רבים הקשורים לריסים היו מופחתים, כמה חלבונים המקושרים לאקטין — הסיבים הרב‑תכליתיים שמרכיבים חלק ניכר מהשלד הפנימי של התא — היו בשפע רב יותר. הדמיה של קטעי אקטין אישרה עיצוב מחדש דרמטי של השלד: קבוצות אקטין מעובות בחלק העליון של תאים מרובי‑ריסים, רשתות דחוסות בגבולות תאים, וכתמים מצטברים בשכבות העמוקות יותר של הרקמה. שינויים אלה לא היו ספציפיים לרקע הגנטי של המטופלים; יצירת השבתת ODAD1 בתאים בריאים הניבה את אותו חיבור מחדש של האקטין ואובדן תאים מרובי‑ריסים. כאשר החוקרים הפריעו בעדינות להרכבת האקטין בעזרת תרופה מולקולרית קטנה, מספר התאים מרובי‑הריסים ופריסת המשטח שלהם התאוששו חלקית, והריסים הפכו לשכיחים ומאורגנים יותר — אף על פי שעדיין לא יכלו להכות כרגיל ללא תפקידו של ODAD1 בעיגון המנוע.
להחזיר את החלק החסר ולהביט קדימה
לבסוף, החוקרים בדקו האם החלפת ODAD1 יכולה להחיות את תנועת הריסים. הם גידלו אורגינואידים של דרכי הנשימה בסידור "אפיקל‑אוּט" — כדוריות חלולות ממיקרו‑רקמת דרכי נשימה עם ריסים הפונים החוצה — מתאים ממטופלים והשתמשו בווקטור לנטיו‑ויראלי כדי להעביר עותק עובד של ODAD1. החלבון המוכנס התמקם נכון בתוך הריסים, השיב את אתרי העיגון החסרים של המנוע והחזיר את פעימת הריסים למהירות ולתבנית קרובות לנורמליות. יחד, תוצאות אלו מראות כי אובדן ODAD1 פוגע בדרכי הנשימה בשני מישורים: הוא משבית ישירות את מערכת המנוע של הריסים ובלבד משנה בעקיפין את שלד האקטין שמעצב את פני השטח המצופה ריסים. עבור החולים, התובנה הכפולה הזו מרמזת על עתיד טיפולי בכיוון כפול — תרפיות גנטיות לתיקון פגימת המנוע הראשית ואסטרטגיות בטוחות לשינוי האקטין שיעזרו לשקם שטיח בריא של ריסים שיכול שוב לשמור על ניקיון הריאות.
ציטוט: Huo, C., Luo, T., Yang, S. et al. Loss-of-function variants in ODAD1 disrupt ODA docking and induce actin cytoskeletal remodeling in primary ciliary dyskinesia. Cell Discov 12, 25 (2026). https://doi.org/10.1038/s41421-026-00875-8
מילות מפתח: דיסקינזיה של ריסים ראשונית, ODAD1, ריסים נעים, שלד ציטופלסמתי של אקטין, תרפיה גנטית