Clear Sky Science · he
צנרת פרופיל מרחבי משולב לקביעת ארכיטקטורות סביבת הגידול בממצאים קליניים ארכיביים באמצעות טכנולוגיית CmTSA סופר־פלקס
מדוע הנוף הנסתר סביב הגידולים חשוב
סרטן אינו גדל בבדידות. הוא מוקף שכונה פעילות של תאים חיסוניים, תאי תמיכה, כלי דם ורקמת צלקת היוצרת יחד את ה"מיקרו־סביבה" של הגידול. מאמר זה מציג שיטה מעשית למיפוי נוף נסתר זה בפרטי פרטים באמצעות דגימות רקמה סטנדרטיות מבתי חולים. על ידי חשיפת אילו סוגי תאים עומדים זה לצד זה ואיך הם מתארגנים לשכונות מועילות או מזיקות, השיטה עשויה לסייע לרופאים לחזות טוב יותר כיצד הסרטן של המטופל יתנהג ואילו טיפולים סביר שיעבדו.
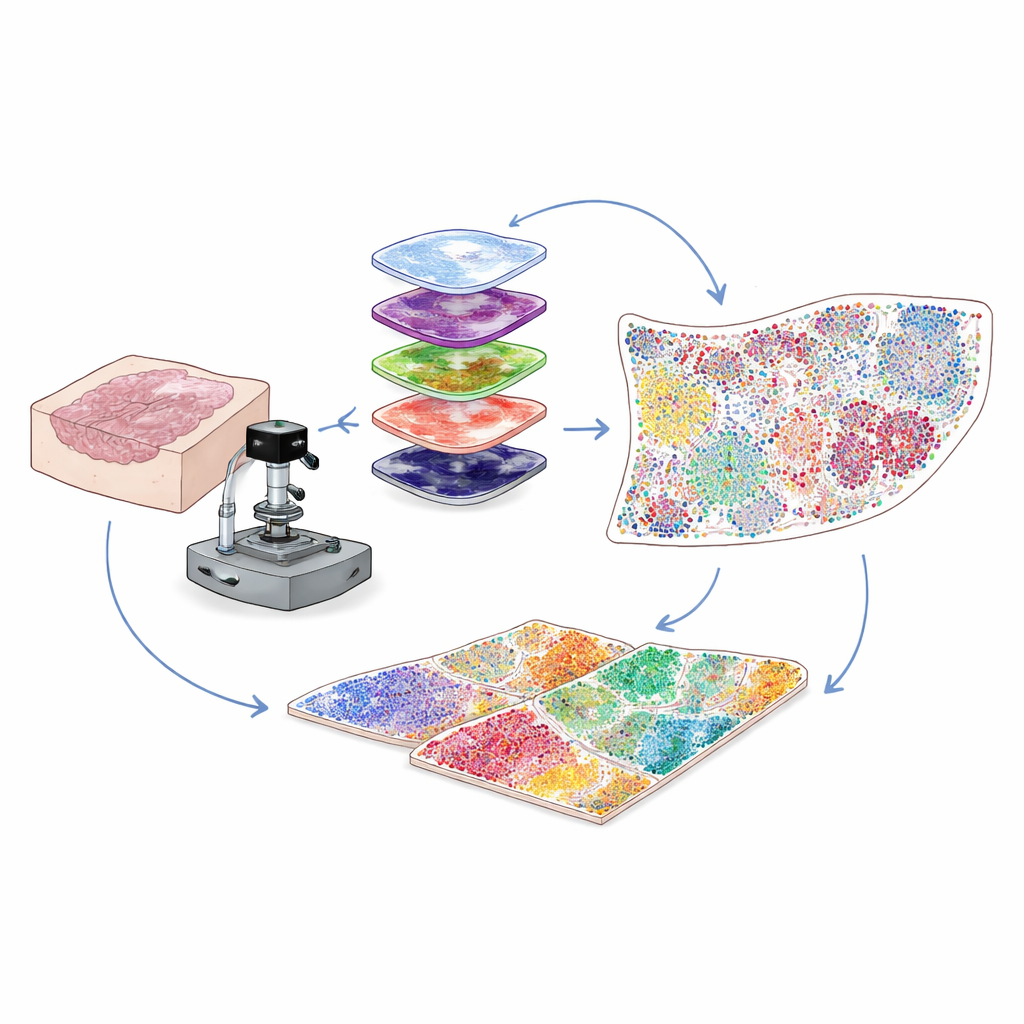
לראות יותר בדגימות יומיות מבתי חולים
רוב דגימות הסרטן הקליניות נשמרות כפרוסות דקות של רקמה מוטמעת בשעווה, הידועות כבלוקים FFPE, שניתן לאחסן שנים רבות. אלו הן אוצר למחקר, אך בעיה טכנית הגבילה מדענים: דגימות כאלה מפיקות זוהר רקע טבעי שמבליע את האותות החלשים של חלבונים רבים חשובים. המחברים פתרו זאת על ידי שילוב של אור עז ומכוון יחד עם טיפול כימי מתון למחיקה סלקטיבית של זוהר הרקע בלי לפגוע ברקמה או במטרות החלבון. שלב "הלבנה" ההיברידי האופטי־כימי הזה משפר באופן חד את בהירות התמונה, ומאפשר לזהות אותות חלבון חלשים שלא היו נראים אחרת.
צובעים עשרות תגיות חלבון על אותה פרוסה
כדי להבין אילו תאים נוכחים ומה הם עושים, מדענים עושים צביעה של רקמות בנוגדנים הנקשרים לחלבונים ספציפיים. שיטות מרובות-סימנים מסורתיות נתקעות לעתים באות חלש לחלבונים נדירים או יכולות לעקוב רק אחרי מספר מוגבל של סמנים בבת אחת. כאן, הקבוצה משתמשת בגישה הנקראת הגדלת אות באמצעות טיראמיד מעגלית (cyclic tyramide signal amplification). בכל סיבוב צובעים קבוצה קטנה של סמנים ומפתחים אנזימטית פלואורסצנטית בהירה שנשארת קבועה ומוצמדת. לאחר מכן הנוגדנים נושרים בעדינות בעוד שהאות נותרת, הרקע מואר מחדש, ומוסיפים את קבוצת הסמנים הבאה. על ידי חזרה על מחזור זה פעמים רבות ובהצמדת התמונות באמצעות האות הקבועה של גרעיני התאים, ניתן להמחיש באופן אמין 30 עד 60 חלבונים שונים על פרוסת רקמה אחת, על כל השקף, ברזולוציה של תא-יחיד.
ממירים תמונות צבעוניות לאטלס תא-תא
תמונות עם ריבוי סמנים מכילות מיליוני פיקסלים, הרבה יותר מכפי שאדם יכול לנתח בעין. לכן המחברים בונים צנרת ראייה ממוחשבת שמוצאת ומשרטטת תחילה כל גרעין תאי באמצעות כלים של למידה עמוקה שפותחו במקור לחלוקת תאים כללית. ואז, בהתבסס על היכן מופיע הפלואורסנציה של כל חלבון—על ממברנת התא, בציטופלסמה או בגרעין—ובמערכי כללים לוגיים, כל תא מוקצה לסוג או לתת-סוג, כמו תא גידול, תא T מסייע, תא T קוטל, תא B, פיברובלסט או אחרים. הפלט הוא טבלה דיגיטלית שמפרטת, עבור כל תא בשקף, את זהותו ואת הקואורדינטות המדויקות שלו. זה משנה תמונה מורכבת למפה כמותית של מי נמצא היכן בתוך מיקרו־סביבת הגידול.
גילוי שכונות תאי שעושות את ההבדל בתוצאה
תאים לעתים רחוקות פועלים לבד; מה שחשוב הוא מי השכנים שלהם. כדי ללכוד זאת, החוקרים בוחנים דרכים שונות להגדיר שכונות מקומיות סביב כל תא ומסכימים על גישה רשתית מבוססת רדיוס. דמיינו שציור מעגל קטן—בערך בעובי שערה אנושית—סביב כל תא ורישום מי גרים בתוכו. על ידי קיבוץ תאים שהמעגלים שמסביבם מכילים תערובות שכנים דומות, השיטה מזהה "נישות פונקציונליות" חוזרות, כגון אזורי עשירים בחיסון, מחסות כבושות בפיברובלסטים, או אזורים שדומיננטיים על ידי הגידול. יישום אסטרטגיה זו על רקמת המעי הגס מראה ששכונות מבוססות רדיוס מתיישבות יותר עם מבנים אנטומיים ידועים מאשר שיטות חלופיות. בדגימות סרטן צוואר הרחם ממטופלים עם תוצאות טובות לעומת גרועות, הקבוצה מוצאת שנישות עשירות בתאים חיסוניים מצטברות קרוב לקצה הגידול אצל החולים שהצליחו יותר, בעוד שחולים עם תוצאות גרועות מראים אזורים עבים צפופים בפיברובלסטים שמקיפים תאי הגידול ונראים כחוצצים מול תאי החיסון התוקפים.
ממפות מרחביות לטיפול מותאם
בשילוב צביעה איכותית וזולה של חלבונים רבים עם ניתוח תמונה חזק, עבודה זו מספקת צינור מקצה לקצה שניתן ליישם על מספר גדול של דגימות סטנדרטיות מבתי חולים. השיטה הופכת רקמה משומרת למפות מפורטות של האופן שבו תאי הגידול, החיסון והסטורם מיישבים ומתערבים זה עם זה. לקורא שאינו מקצועי, המסקנה היא שלא רק סוגי התאים, אלא גם דפוסי השכונה המדויקים שלהם משפיעים על התנהגות הסרטן. הפלטפורמה עשויה לסייע לחוקרים לזהות מוקדי חיסון מגן, לאתר מחסומים תאיים מדכאים, ולבסוף לתמוך בפרוגנוזה מדויקת יותר ובאסטרטגיות אימונותרפיה עדינות יותר.
ציטוט: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
מילות מפתח: מיקרו־סביבת הגידול, פרוטאומיקה מרחבית, דימות מרובה סימנים, אימונולוגיה של סרטן, ניתוח תא-יחיד