Clear Sky Science · he
שינויים דינמיים במיקרו‑הסביבה החיסונית בסרטן השחלות לאחר כימותרפיה ניאו‑אדג'ובנטית
מדוע מחקר זה חשוב לנשים עם סרטן השחלות
סרטן שחלות מתקדם מטופל לעיתים קרובות בכימותרפיה חזקה לפני או אחרי ניתוח, ועדיין רבות מהמטופלות חוות חזרת מחלה ואיבוד תגובה לתרופות. המחקר שואל שאלה דחופה: כיצד הכימותרפיה מעצבת בדממה את ההגנות הטבעיות של הגוף סביב הגידול, והאם ניתן לתקן תגובה זו כדי לשמר את יעילות הטיפול לאורך זמן? באמצעות בחינה של תאים בודדים ובדיקת שילובי תרופות חדשים בעכברים, החוקרים מגלים תפקיד נסתר למולקולות שומניות דמוי‑הורמונים הנקראות פרוסטגלנדינים בסיוע לגידולים להתחמק ממערכת החיסון לאחר כימותרפיה.
שדה קרב משתנה סביב הגידול
גידולי שחלות אינם גדלים בבידוד: הם יושבים ב"שכונה" עמוסה של תאים חיסוניים, רקמת חיבור ונוזל הבטן. לפני הטיפול, השכונה הזו כבר מוטה לטובת הסרטן, עם מעט תאי T קטלניים אגרסיביים והרבה תאים שמדכאים את ההתקפה החיסונית. הצוות ניתח נתוני ריצוף RNA בתא בודד שפורסמו קודם לכן מנשים עם סרטן שחלות סרוזי מדרגה גבוהה, והשווה דגימות שנלקחו לפני ואחרי כימותרפיה ניאו‑אדג'ובנטית (כימותרפיה שניתנת לפני ניתוח). הם מצאו כי הכימותרפיה לא רק הורסת תאי גידול; היא גם עוררה זמנית פעילות חיסונית, הגברה של איתותים המקושרים לגירוי תאי T ודלקת, תוך ירידה בחלק מתאים רגולטוריים שגרתית מדכאים את ההתקפה.
כששינויים מועילים הופכים להזיקים
למרות הדחיפה הזמנית הזו, ברוב המטופלות המחלה חוזרת ונוצרת עמידות לתרופות פלטינום כמו ציספלטין. כדי להבין מדוע, החוקרים חקרו לעומק כיצד סוגי התאים השונים מתקשרים זה עם זה לאחר הטיפול. הם גילו כי הכימותרפיה הגבירה בצורה חזקה גנים המעורבים בייצור פרוסטגלנדינים במאקрофאגים ובלוריות המשויכות לגידול, והגבירה את התקשורת בין תאים אלו לתאי T. באמצעות כלים מתמטיים מתקדמים הראו החוקרים שהסביבה הכוללת זזה לכיוון מצב פרו‑דלקתי אך בסופו של דבר מדכא, עם עליה בכימוקינים שמגייסים תאים מיואליים והגברה של מסלולים שיכולים לעייף תאי T לאורך זמן. תוצאה זו מרמזת כי הפרוסטגלנדינים עשויים לפעול כתמסורת מולקולרית, שהופכת את גל העליה החיסוני הראשוני לבלם מתמשך על החיסון נגד הגידול.
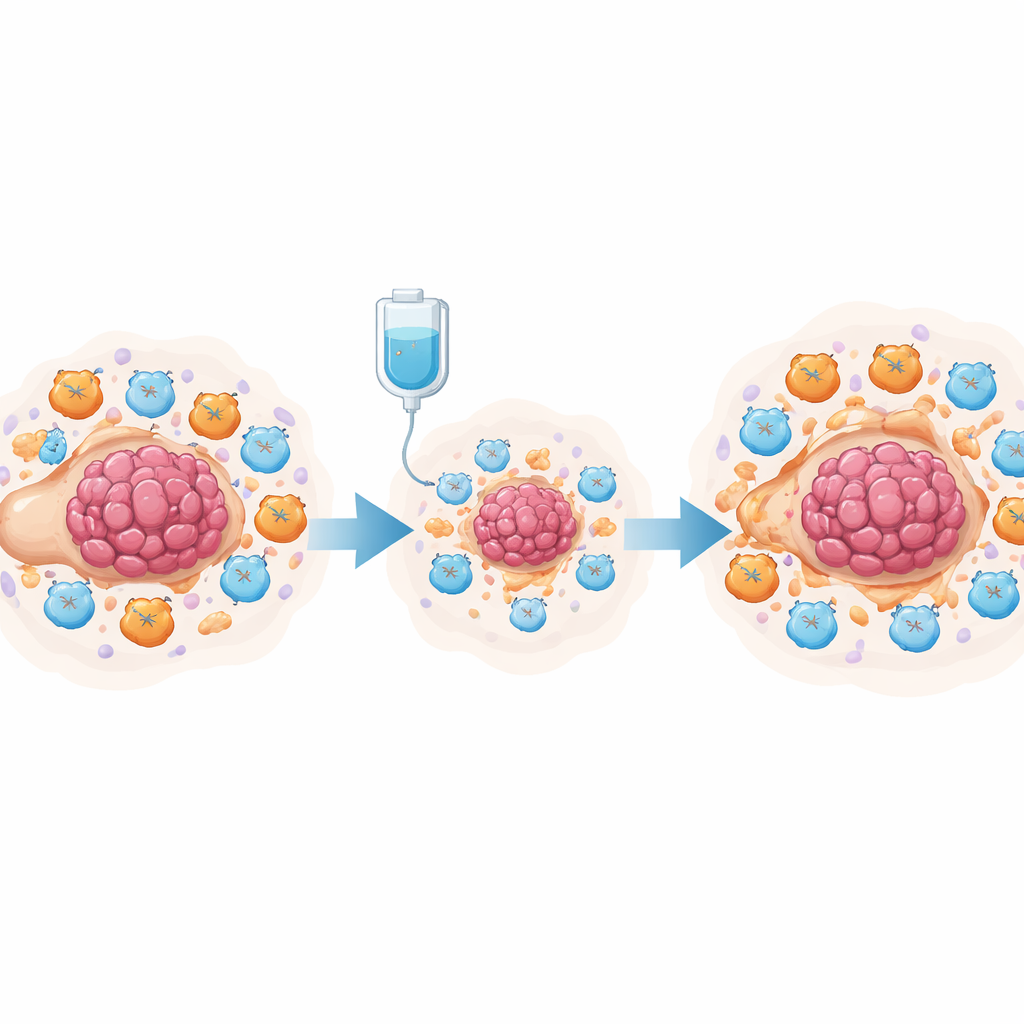
כימותרפיה, פרוסטגלנדינים ותאי T מושתקים
כדי לבחון רעיון זה ניסיונית, הצוות השתמש במודל עכבר לסרטן השחלות שטופל בציספלטין. ניתוח תא‑בודד של עשרות אלפי תאים ממכתש הבטן הראה כי ציספלטין הקטין את תאי הגידול והגדיל את סך תאי ה‑T, אך גם הרחיב באופן ניכר תאים מדכאי מקור מיואידי (MDSCs) ותאי T קטלניים מותשים. הן תאי הגידול והן תאי המדכאים הללו הפיקו רמות גבוהות של אנזימים לייצור פרוסטגלנדינים. בתרביות משותפות, תאי גידול שטופלו בציספלטין הובילו תאי מח עצם לאמץ מצב הדומה ל‑MDSC ופגעו בפעילות ובגדילה של תאי CD8+ קטלניים. החוקרים עשו מעקב והצביעו על מסלול האיתות NF‑κB בתאי הגידול, שהפעיל את גן PTGES — צעד מרכזי בייצור פרוסטגלנדין E2. חסימת מסלול זה הורידה את רמות PTGES ואת תפוקת הפרוסטגלנדינים.
להטה במערכה עם טיפול משולב
השאלה הפרקטית היא האם חסימת פרוסטגלנדינים יכולה לשפר את יעילות הכימותרפיה. בעכברים השתמשו החוקרים בהשמדה גנטית של Ptges בתאי הגידול, בנוגדנים שמנטרלים פרוסטגלנדין E2 או בתרכובות קטנות שמעכבות סינתאזת פרוסטגלנדינים. כל הגישות האלה הורידו את רמות הפרוסטגלנדינים, הפחיתו את הצטברות ה‑MDSCs והשיבו את יכולת ההרג ואת החוסן הדמוי‑הגזע של תאי CD8+ T. בשילוב עם ציספלטין, או עם הרגיל ציספלטין‑פאצ׳יטקסל, מעכבי פרוסטגלנדינים האטו גדילה והתפשטות גידול ביעילות רבה יותר מאשר כימותרפיה לבדה. הנתונים מצביעים על כך שהדיכוי החיסוני המונע על‑ידי פרוסטגלנדינים אינו פרט שוליים אלא סיבה מרכזית לבריחת הגידולים לאחר תגובה ראשונית.
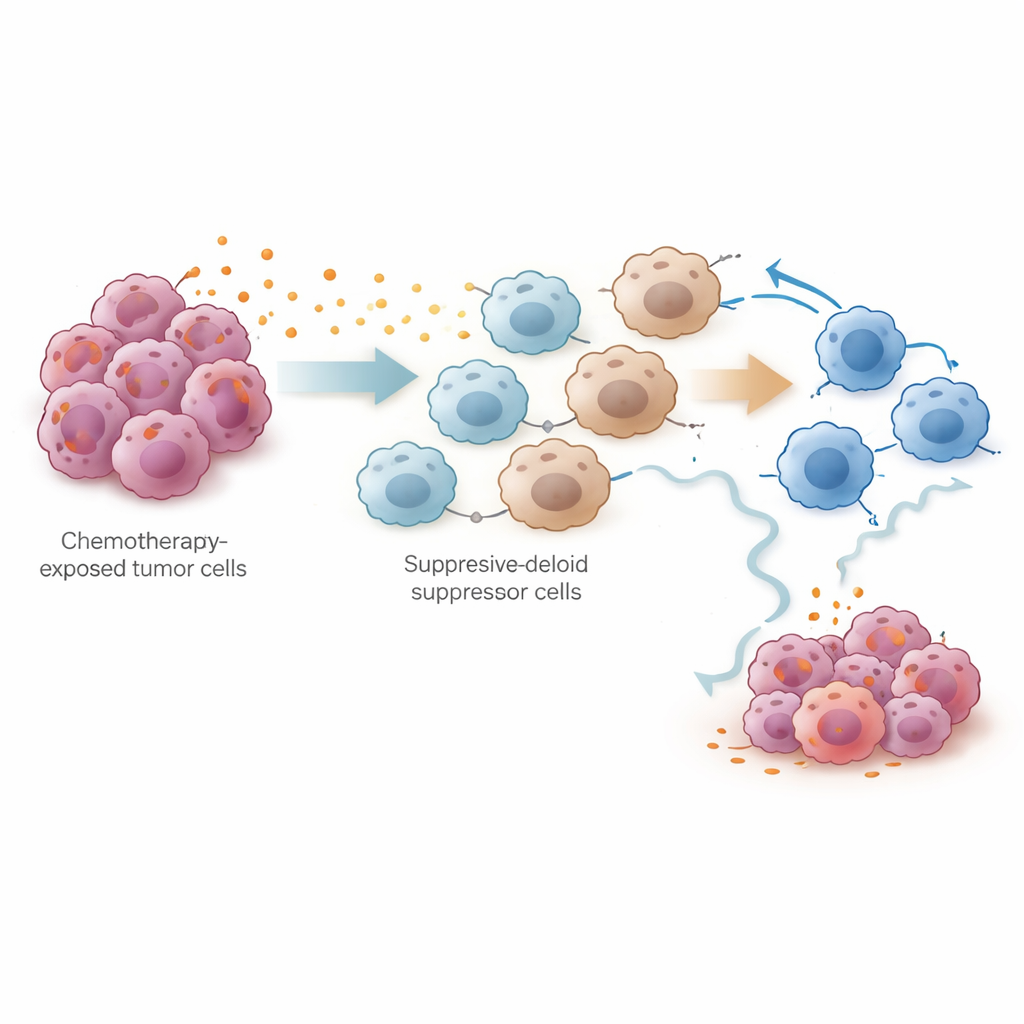
זווית חדשה לשמירה על יעילות הטיפול
במונחים יום‑יומיים, עבודה זו מציעה שמגע הכימותרפיה משנה את סביבת הגידול בשני שלבים: ראשית היא מחלישה את הסרטן ומגייסת לזמן קצר את מערכת החיסון, אך לאחר מכן היא מפעילה גל של פרוסטגלנדינים שמזמינים תאים מדכאים ומעייפים את כוחות ההרג הטבעיים של הגוף. על‑ידי זיהוי ייצור הפרוסטגלנדינים המונע על‑ידי PTGES כחשוד מרכזי, המחקר מצביע על אסטרטגיה ממשית: שילוב כימותרפיה פלינאית סטנדרטית עם תרופות החוסמות מסלולי פרוסטגלנדינים עשוי לסייע לשמר מתקפה חיסונית חזקה ולעכב או למנוע חזרה של המחלה בסרטן השחלות. אמנם יש צורך בניסויים קליניים נוספים, אך גישת השילוב הזו מציעה כיוון מבטיח להארכת תועלת הטיפולים הקיימים.
ציטוט: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
מילות מפתח: סרטן השחלות, מיקרו‑הסביבה של הגידול, התנגדות לכימותרפיה, פרוסטגלנדינים, אימונותרפיה