Clear Sky Science · he
ATP6V1B2 מקל על סטאטוזיס בכבד על ידי קידום חומציות הליזוזומים בהפטוציטים
מדוע כבד שומני חשוב
רבים נושאים שומן עודף בכבד מבלי לדעת זאת. מצב זה, הקרוי כיום מחלת כבד סטאטוטית הקשורה להפרעות מטבוליות (MASLD), משפיע על כ־25% מאוכלוסיית העולם ועלול להתפתח בשקט לצלקת, לכשלים בכבד ולמחלות חמורות נוספות. עם זאת, רופאים עדיין חסרים כלים טובים לחזות מי ידרדר ומעט טיפולים שמכוונים ישירות לבעיות התוך‑תאיות הבסיסיות. המחקר הזה חושף כיצד "משאבת חומצה" תאית שהייתה עד כה פחות מוכרת מסייעת לתאי הכבד להיפטר מעודפי שומן ומציע כיוון חדש לאבחון וטיפול.
עוזר נסתר בתוך תאי הכבד
בתוך כל תא כבד יש מרכזי מיחזור קטנים הנקראים ליזוזומים. הם נשענים על סביבה חומצית פנימית כדי לפרק חלקים בלויים ושומן עודף. החומציות נשמרת על ידי משאבה מולקולרית ידועה כ‑V‑ATPase, שנבנית ממספר רכיבי חלבון. המחברים התרכזו בחלק מרכזי אחד, ATP6V1B2, שחשוב במיוחד לשמירה על חומציות הליזוזום. הם בדקו האם שינויים בחלבון זה עשויים להסביר מדוע שומן מצטבר ב‑MASLD והאם רמותיו בדם יכולות לסמן על המחלה.
רמזים ממטופלים ומדגמי בעלי חיים
כאשר החוקרים בחנו מאגרי גנום ציבוריים ודגימות דם של מטופלים, הם מצאו שרמות ATP6V1B2 היו באופן עקבי נמוכות יותר אצל אנשים עם MASLD ואף נמוכות יותר אצל אלה עם שחמת, צורת נזק קשים בכבד. רמות נמוכות של ATP6V1B2 בכבד נקשרו ליותר דלקת, לצלקת גרועה יותר ולסמנים גבוהים יותר של פגיעה בכבד בדם. במודלים של עכברים שניזונו מתפריטים עשירים בשומן או חסרי רכיבים תזונתיים — שיטות מקובלות לדמות MASLD — גם אספקת ATP6V1B2 בכבד ירדה. ממצאים אלה מצביעים על כך שאובדן החלבון אינו רק תופעת לוואי אלא עשוי להיות קשור בקשר הדוק להתקדמות המחלה.
מה משתבש בתוך תאים כבדיים בסטרס
כדי לראות מה קורה כאשר ATP6V1B2 מופרע, הקבוצה פנתה לתאי כבד בתרבית העמוסים בחומצות שומן, המדמים סביבה "ליפוטוקסית". כאשר הורידו במכוון את ATP6V1B2, טיפות השומן בתאים נפחו, תוצרי חמצון מזיקים עלו באופן חזק והמייטוכונדריה — תחנות האנרגיה של התאים — החלו להיכשל. אותות סטרס תוך‑תאיים זינקו, ואנזים מרכזי לבניית שומן בשם FASN עלה באופן ניכר. לעומת זאת, כאשר הגבירו את ATP6V1B2, התאים התמודדו טוב יותר עם העומס השומני: טיפות השומן הצטמצמו, הלחץ החמצוני הקל והמיטוכונדריה התאוששו. ניסויים אלה מראים ש‑ATP6V1B2 פועל כבלם מגן מפני הצטברות שומן ונזק תאי.
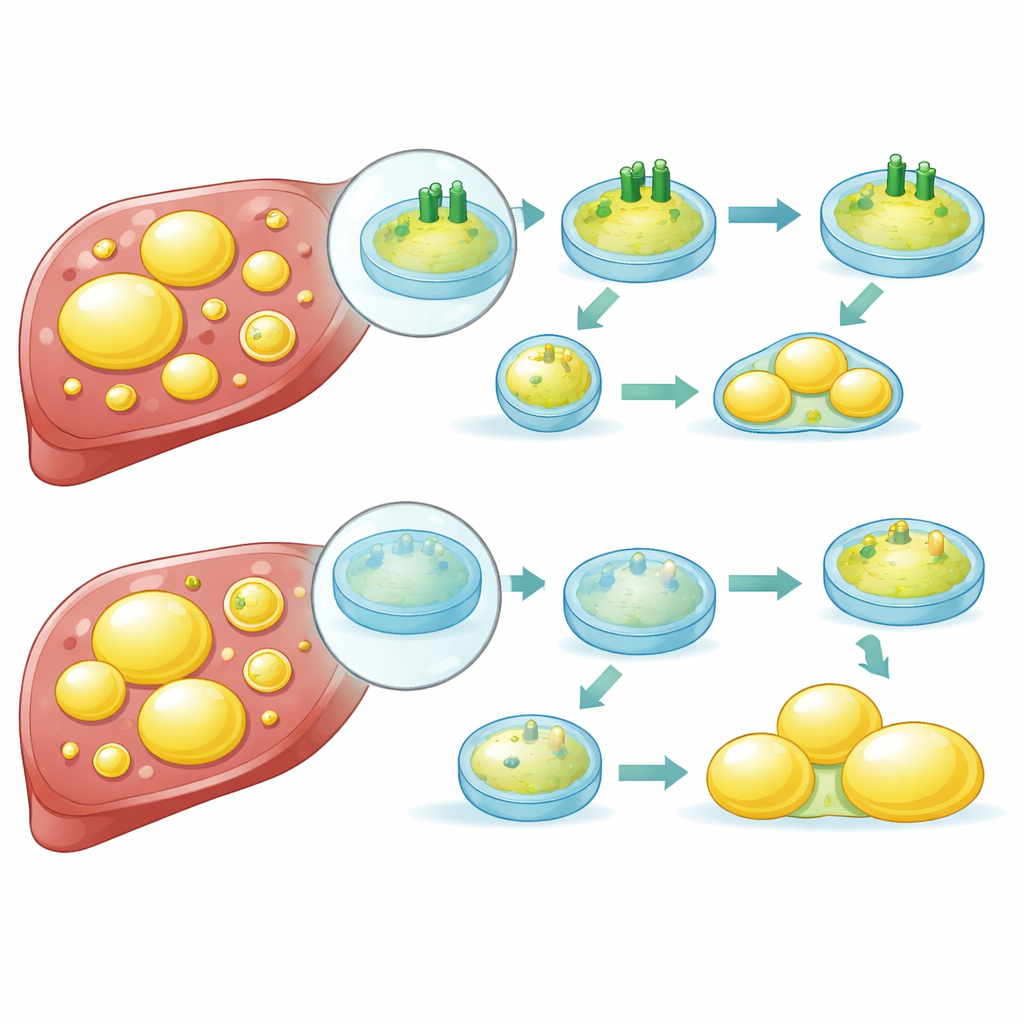
כיצד מיחזור שבור מוביל להצטברות שומן
בהעמקה נוספת, החוקרים גילו ש‑ATP6V1B2 שולט עד כמה הליזוזומים נשארים חומציים ופעילים. כאשר החלבון ירד, הליזוזומים איבדו חומציות, יכולתם לפרק מטען פחתה וזרימת החומרים במערכת המיחזור התאית (אוטופאגיה) נחסמה. בתנאים רגילים, FASN יכול להישלח לליזוזומים להריסה. כש‑ATP6V1B2 בריא, הנתיב הזה פועל ביעילות, משמורן את רמות FASN ומגביל ייצור שומן חדש. אך כאשר ATP6V1B2 דליל, הליזוזומים אינם מסוגלים לפרק את FASN כראוי. האנזים מצטבר, התא מעלה את סינתזת השומן וטיפות השומן ממשיכות לגדול. המחקר גם מציע שדרכי סטרס תוך‑תאיות מגבירות עוד יותר את ייצור ה‑FASN כש‑ATP6V1B2 נמוך, ויוצרות מעגל מרושע.
מה המשמעות לטיפול בעתיד
בעבור קהל לא‑מומחה, המסר ברור: חלבון בודד העוזר לשמור על חומציות הליזוזומים יכול להשפיע באופן משמעותי על כך שתאי הכבד יאחסנו או יפנו שומן. רמות נמוכות של ATP6V1B2, הנצפות גם במטופלים וגם במודלים של MASLD, מחלישות את מערכת המיחזור הפנימית של הכבד, ומאפשרות הצטברות שומן ונזק. מדידת חלבון זה בדם עשויה לסייע לרופאים להעריך חומרת המחלה, ואסטרטגיות המשחזרות את חומציות הליזוזומים או מחזקות את פעילות ATP6V1B2 יכולות לשמש בסיס לטיפולים חדשים. על ידי הארת תפקיד ה"משאבת חומצה" הזו ושליטתה באנזימי עיבוד השומן, המחקר מצביע על טיפולים ממוקדי ליזוזום כדרך מבטיחה לעצור או להפוך את מחלת הכבד השומני.
ציטוט: Xu, R., Yang, F., Zhang, Z. et al. ATP6V1B2 alleviates hepatic steatosis by promoting lysosomal acidification in hepatocytes. Cell Death Discov. 12, 170 (2026). https://doi.org/10.1038/s41420-026-03052-8
מילות מפתח: מחלת כבד שומני, ליזוזומים, אוטופאגיה, מטבוליזם שומנים, דלקת כבד