Clear Sky Science · he
ניצול פיירופטוזיס בטיפול בסרטן השד: מנגנונים חיסוניים ואסטרטגיות ביומواد מתפתחות
הפיכת מוות תאי לנשק חדש נגד סרטן השד
סרטן השד נותר אחד הסרטנים השכיחים והעמידים ביותר ברחבי העולם. גידולים רבים בסופו של דבר מתחמקים מניתוח, כימותרפיה ואפילו מאימונותרפיות מודרניות. סקירה זו בוחנת רעיון עולה: לגרום במכוון לצורה בוערת של מוות תאי, הנקראת פירופטוזיס, בתוך גידולי השד. על ידי גרימת התפוצצות מבוקרת ודלקתית של תאי הסרטן, מקווים המדענים להרוג את הגידול ישירות ולעורר את המערכת החיסונית להצטרף למתקפה.
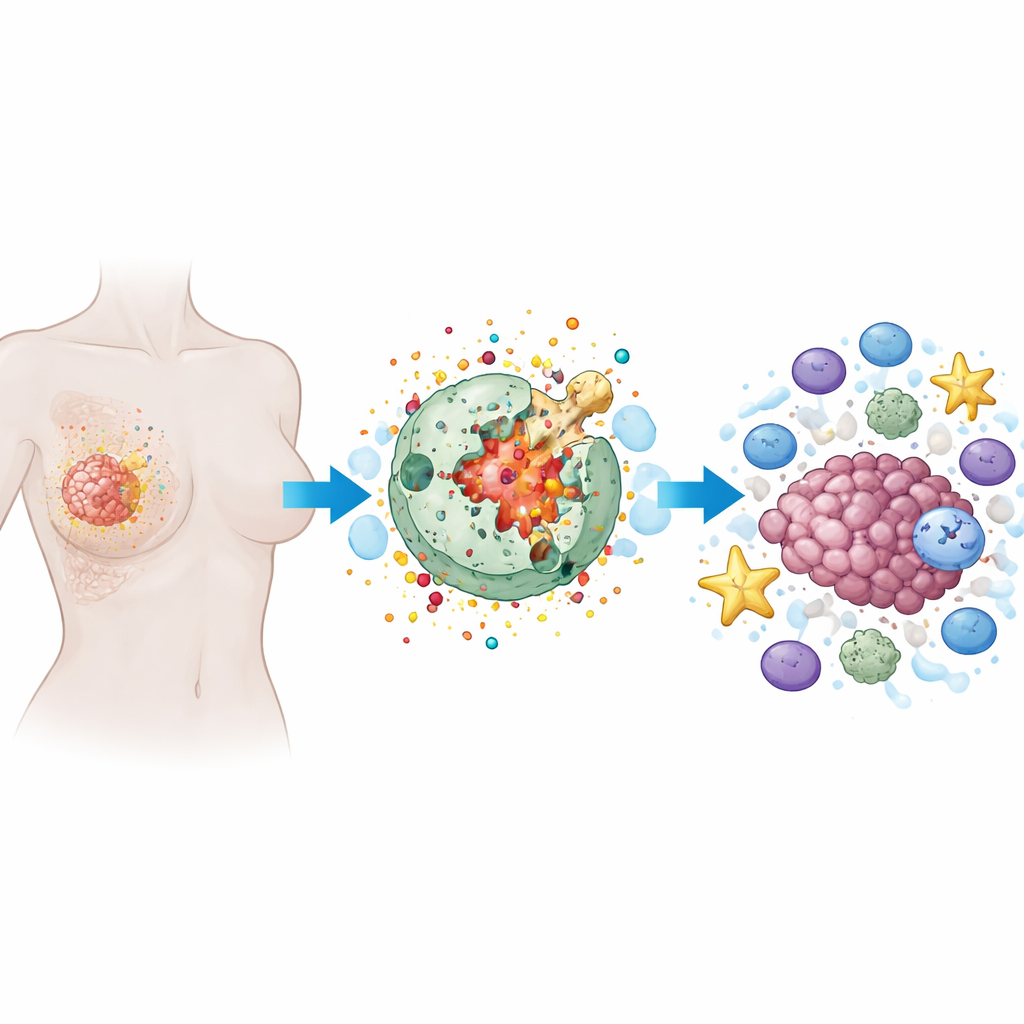
כיצד פועלת צורת מוות תאי בוערת
פירופטוזיס היא צורה מתוכננת של מוות תאי שבה התא מתנפח, קרום התא נפתח בחורים ולבסוף הוא מתפקע, משחרר את תכולתו. שלא כמו מוות תאי שקט ומסודר הנראה בטיפולים רבים, פירופטוזיס הוא רועש ודלקתי. חלבונים מיוחדים, במיוחד משפחה הנקראת גאזרדמינים, פועלים כמטעני הריסה זעירים. לאחר שהם נחתכים על ידי אנזימים פנימיים, הגאזרדמינים מחוררים את קרום התא. זה לא רק הורס את תא הסרטן אלא גם משחרר אותות אזעקה ומולקולות דלקת שיכולות למשוך ולהפעיל תאי חיסון.
מדוע גידולי השד מהווים אתגר מיוחד
סרטן השד אינו מחלה אחת אלא אוסף של תת‑סוגים עם התנהגויות שונות. חלקם, כגון סרטן שד שלילי משלוש מחסומים (triple‑negative), חסרים מטרות תרופתיות נפוצות ולעיתים עמידים לטיפול. גידולי שד רבים נחשבים ל"קרים אימונולוגית", כלומר יש בהם מעט תאי חיסון פעילים. הסקירה מסבירה כיצד מאפייני מיקרו‑הסביבה של גידול השד — כולל תאי סטרומה, תאים מדכאי חיסון ומחסור מקומי בחמצן — יכולים גם להניח את הבסיס לפירופטוזיס ואם אינם נשלטים היטב, להפוך את הדלקת לתדליק לצמיחה ולהתפשטות הגידול. הטבע הדו‑חרכי הזה הופך דיוק לשיקול מרכזי.
מתגי הגאזרדמין בתוך תאי הגידול
נושא מרכזי במאמר הוא כיצד חלבוני גאזרדמין שונים פועלים כמתגים מולקולריים בתוך תאי סרטן השד. גרסאות כגון GSDMD ו‑GSDME יכולות להמיר איתותים מכימותרפיה, קרינה או תאי חיסון תוקפים לפירופטוזיס מלא. אחרים, כמו GSDMC וחלק מצורות GSDMB, נמצאים לעתים גבוהים יותר בגידולים אגרסיביים ויכולים לקדם או להגביל את המחלה בהתאם לאופן בו מופעלים. רבים מהסרטנים של השד משתיקים כימית את GSDME, מה שמחליש את הפירופטוזיס ואת ההפעלה החיסונית. השבתה או גירוי סלקטיבי של הגאזרדמינים הנכונים עשויים להכריע אם טיפול יהרוג רק כמה תאים או יהפוך את כל הגידול לחיסון לאתר שמזהיר את המערכת החיסונית.
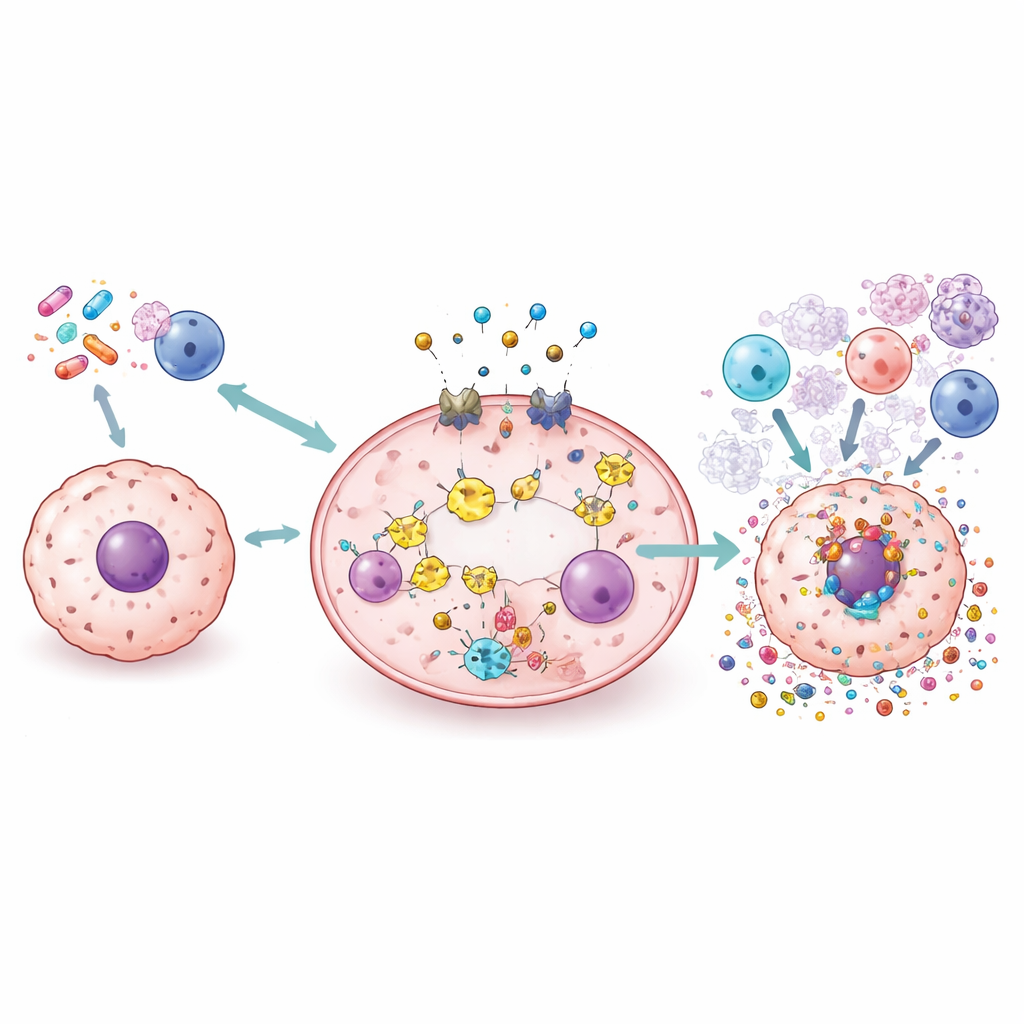
כלים חדשים: תרופות, חלקיקים ננומטריים, וירוסים וקרינה
הסקירה סוקרת מגוון רחב של אסטרטגיות הנחקרות לניצול פירופטוזיס בבטחה. תרופות סטנדרטיות כגון ציספלטין ודוקסורוביצין ניתנות לשימוש מחדש או לרפורמולציה כדי להטות תאים סרטניים לעבור פיצוץ מונע גאזרדמין במקום מוות שקט. מולקולות קטנות יכולות להגביר או לחסום חלקים מהנתיב בכדי לכוונן את הדלקת באופן מדויק. חלקיקים ננומטריים ונשאים ביומימטיים מתוכננים לשאת כימותרפיה, יוני נחושת או מולקולות הפעולות באור ישירות לתוך הגידולים, שם הם מעוררים פירופטוזיס תוך שמירה על רקמות בריאות. וירוסים אונקוליטיים וקרינה ניתנים גם הם להנדסה או לשילוב עם סוכנים אחרים כדי לעורר פירופטוזיס ולעצב מחדש את הנוף החיסוני של הגידול, מה שעשוי להפוך תרופות חוסמות נקודות הצ'קפוינט ליעילות יותר.
איזון בין תועלת עזה לסיכונים ממשיים
מכיוון שפירופטוזיס הוא כה דלקתי, אותן תגובות שעוזרות למערכת החיסון להילחם בסרטן עלולות גם לפגוע ברקמות תקינות או אפילו לקדם את הגידול אם יהפכו כרוניות. המחברים מדגישים סמנים ביולוגיים מוקדמים — כגון חתימות גנטיות, דפוסי מתילציה, חתיכות של חלבוני גאזרדמין בדם ופרופילי ציטוקינים — שעשויים לסייע לזהות אילו מטופלים צפויים להפיק תועלת ומי בסיכון גבוה לסופות ציטוקינים מסוכנות. עיצובים מתקדמים בננו‑רפואה, שילובי תרופות נבחרים בקפידה וניטור בזמן אמת של סמני דלקת נבחנים כולם כדי לשמור על תגובה חדה אך מבוקרת.
מה זה עשוי לאפשר למטופלים עתידיים
באופן פשוט, הסקירה טוענת כי לגרום לתאי סרטן "למות בקול" יכול לשנות את טיפול בסרטן השד. על ידי חימום פירופטוזיס בקבוצה מדויקת של תאי גידול, רופאים עלולים גם להקטין את הנפח הגידולי וגם להעיר תגובה חיסונית חזקה ומתמשכת, להמיר גידולים קרים לחמים ולהפוך אותם לרגישים יותר לאימונותרפיות מודרניות. עם זאת, פירופטוזיס הוא בעל ברית מתפרץ: אם ישוחרר בצורה רחבה מדי או למשך זמן ארוך מדי, הוא עלול להחמיר דלקת או לעודד תאים עמידים לשגשג. מחקר עתידי יתמקד במיפוי מי יפיק תועלת, השלמת מערכות מסירה ממוקדות והרצת ניסויים קליניים שמשלבים שיטות מעוררות פירופטוזיס עם תרופות חיסוניות. אם ניתן לפתור את האתגרים האלה, ניצול פירופטוזיס עשוי להוסיף ממד רב‑עוצמה חדש לטיפול בסרטן השד.
ציטוט: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
מילות מפתח: פירופטוזיס, סרטן השד, גאזרדמין, מיקרו‑סביבת הגידול, ננו‑רפואה