Clear Sky Science · he
מעבר אפיתל-מזנכימלי ממוצא אנדותל המתווך על ידי APOA2 ותכנות מחודש של חילוף החומרים של שומנים בסרטן מקנים עמידות לתרופות אנטיאנגיוגניות באמצעות TGF-β
מדוע הממצא הזה משמעותי עבור מטופלים
רופאים משתמשים יותר ויותר בתרופות שמרעיבות גידולים בכבד על ידי ניתוק אספקת הדם שלהם, אך אצל מטופלים רבים הסרטן מפסיק להגיב לאחר תועלת ראשונית. המחקר חוקר שאלה דחופה: מדוע חלק מהסרטן בכבד מפתח עמידות לטיפולים החוסמים כלי דם וכיצד ניתן להתגבר עליה? החוקרים חושפים שותפות נסתרת בין חלבון שומנים בדם לאות גדילה חזק שמאפשרת לגידולים לכוונן מחדש הן את כלי הדם שלהם והן את שימושם באנרגיה — ומצביעים על גישה שונה לטיפול בסרטן שקשה לרפא.
גידול שלומד לחיות בלי חבל ההצלה הרגיל שלו
סרטן הכבד מסוג הפטוצלולר קרצינומה, הצורה השכיחה ביותר של סרטן הכבד, תלוי במידה רבה בכלי דם חדשים כדי לצמוח. התרופות המקובלות למחלה מתקדמת נועדו לחסום מסלול מרכזי לצמיחת כלי דם שמבוסס על VEGF וקולטן VEGFR2. ובכל זאת, אצל מטופלים רבים, הגידולים ממשיכים לשגשג למרות תרופות אלה. בהשוואת דגימות גידול ממטופלים שהגיבו ולא שהגיבו לתרופה האנטיאנגיוגנית אפטיניב, המחברים מצאו שגן אחד, APOA2, בולט במיוחד. בגידולים של מטופלים עמידים היו רמות גבוהות באופן משמעותי של APOA2, חלבון הידוע בעיקר בתפקידו בהובלת שומנים בדם. ממצא זה העלה את האפשרות ש-APOA2 עשוי לסייע לגידולים להתחמק מתרופות המכוונות לכלי דם.
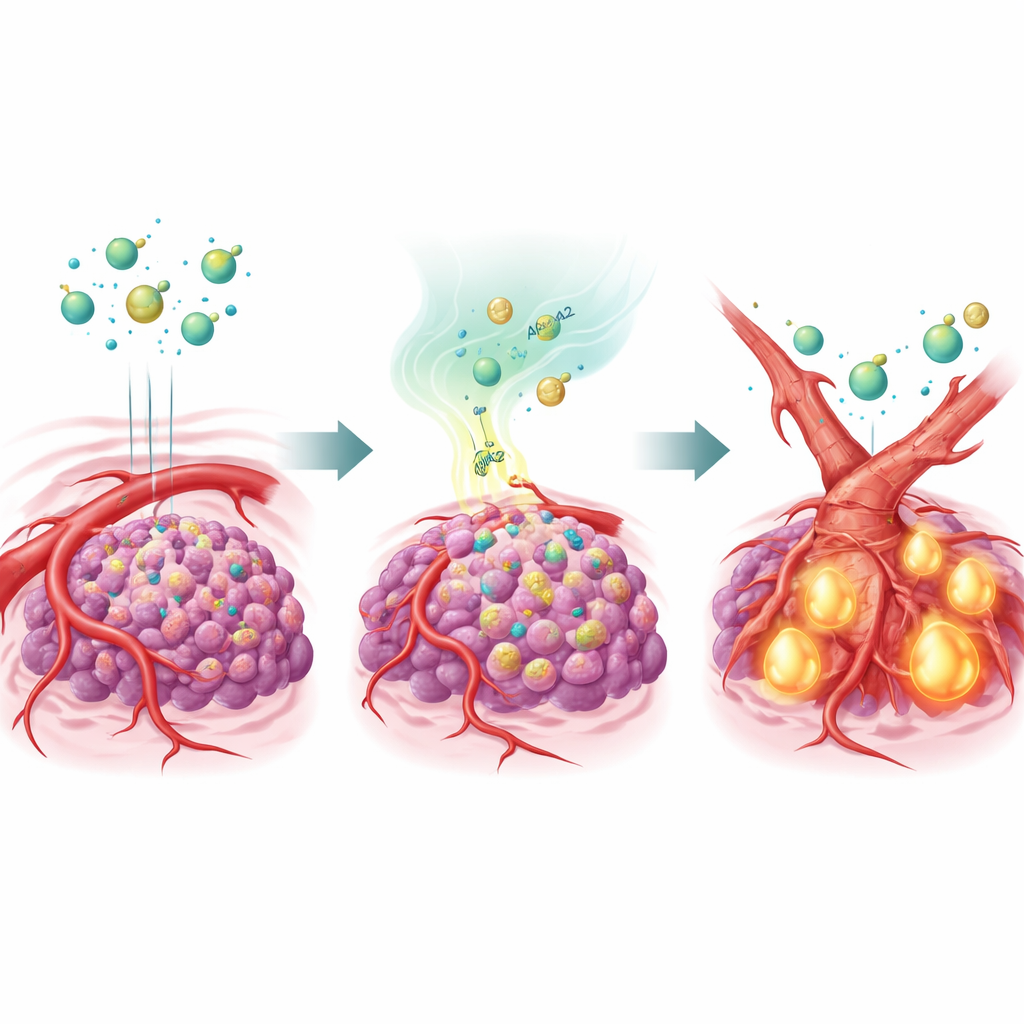
חלבון הובלת שומן שמשנה את מבנה כלי הדם
כדי לבחון רעיון זה, הצוות הנדס תאי סרטן כבד לייצר כמות עודפת של APOA2 והשתיל אותם בעכברים. כשהטופלו בכמה תרופות אנטיאנגיוגניות שונות, גידולים עשירים ב-APOA2 כמעט שלא הגיבו לטיפול: כלי הדם שלהם נותרו, והסרטן המשיך לצמוח. ניתוח מפורט הראה שאות שליטה שנקרא TGF-β הופעל באופן חזק בגידולים אלה, ורמותיו היו מוגברות גם בסביבת הגידול וגם בדם החיות. TGF-β השפיע על תאי הציפוי של כלי הדם, ודחף אותם לשנות זהות בתהליך שנקרא מעבר אנדותל-למזנכימה. כאשר הם הוסטו למצב מזנכימלי יותר, דמוי צלקת, תאים אלה איבדו הרבה מ-VEGFR2 — הקולבן שאותו מיועדות לתפוס תרופות אנטיאנגיוגניות. למעשה, כלי הדם שונו לצורה שהתרופות כבר לא יכלו לזהות כיעד.
חריגה מטאבולית ששומרת על אספקת הדלק של התאים הסרטניים
הסיפור לא הסתיים בדופן כלי הדם. אותו אות TGF-β שמופעל על ידי APOA2 גם תכנת מחדש את הדרך שבה תאי הסרטן מזינים את עצמם. במקום להסתמך בעיקר על פירוק סוכרים, תאים בעלי רמות גבוהות של APOA2 החלו לספוג יותר חומצות שומן חופשיות מהסביבה ולשריין אותן במיטוכונדריה באמצעות חמצון חומצות שומן. ניסויים שמדדו שימוש במזון וצריכת חמצן הראו שהתאים האלה הפכו להיות תלויים יותר בשומן כמקור אנרגיה וייצרו יותר דלק תאית (ATP). שינוי זה איפשר לתאי הגידול להמשיך להתחלק במהירות ולהימנע ממוות תאי, גם כאשר אספקת הדם הושפעה על ידי טיפולים אנטיאנגיוגניים.
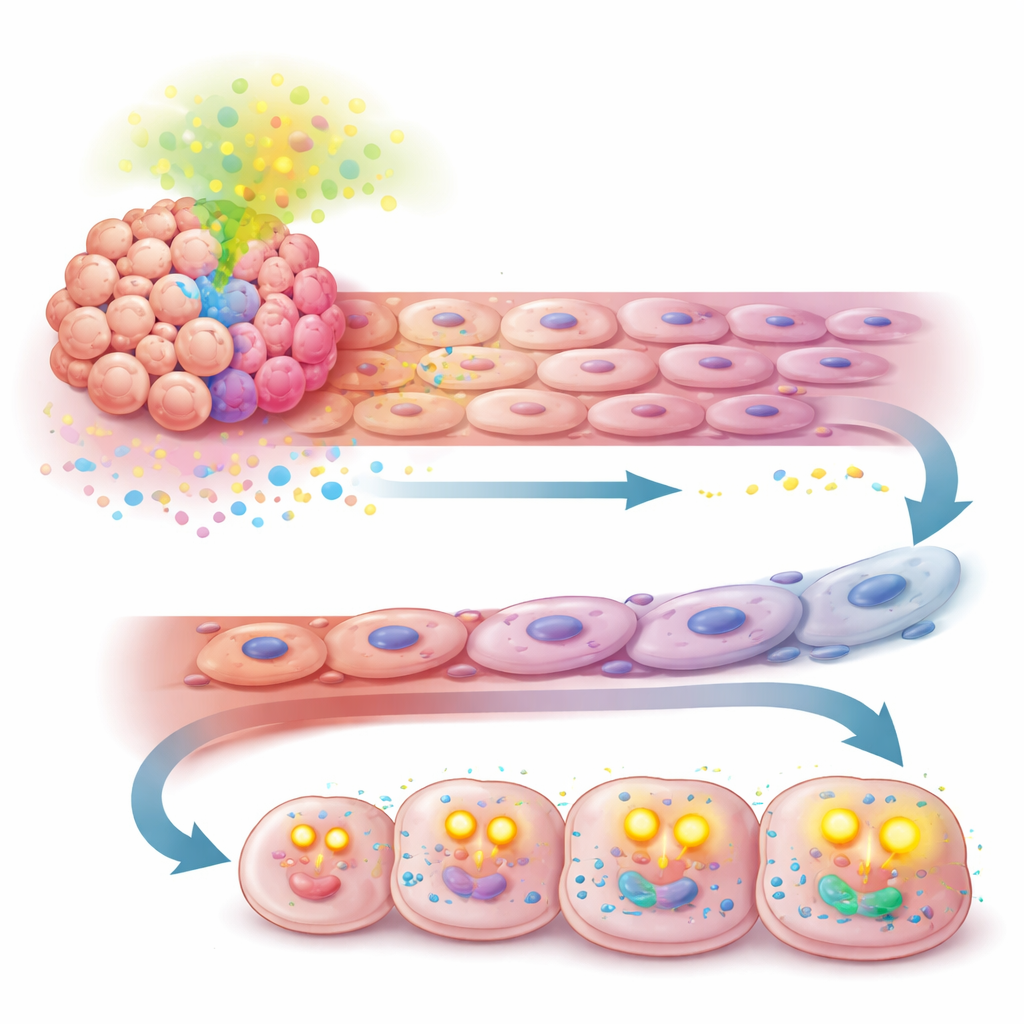
הפיכת נקודת תורפה למטרה טיפולית חדשה
חשוב לציין כי כאשר החוקרים חסמו את TGF-β, היתרונות שהעניק APOA2 נעלמו. עיכוב אות זה במודלים של עכבר צמצם את השינויים הבלתי תקינים בכלי הדם, השיב את הרגישות לטיפול והאט את גדילת הגידול. אף יותר מעודד, נוגדן כפול שחוסם במקביל את TGF-β ואת מצופי המעכב החיסוני PD-1 עבד טוב יותר מאשר כל גישה בנפרד בגידולים עם רמות גבוהות של APOA2. תוצאות אלה מציעות שבתת-קבוצה של סרטן הכבד המסומנת ב-APOA2 גבוה, המחלה באופן שקטה החליפה את התלות מן המסלול הרגיל של VEGF למסלול שמרכזו TGF-β אשר תומך הן בכלי הדם והן בחילוף החומרים של הגידול.
מה משמעות זאת לטיפול העתידי בסרטן הכבד
לציבור הרחב, המסר המרכזי הוא שלפחות חלק מהגידולים בכבד בורחים מתרופות נוכחיות המכוונות לכלי דם על ידי כיוונון מחדש הן של מערכות הצנרת שלהם והן של אספקת האנרגיה שלהם. חלבון הקשור לשומנים, APOA2, מעלה את אות ה-TGF-β, אשר בתורו מסתיר כלי דם כך שהתרופות הקיימות אינן יכולות לזהותם ומלמדת את תאי הסרטן לחיות על שומנים במקום על סוכר. המחקר מציע כי בדיקה של רמות APOA2 בגידול עשויה לאתר מטופלים שסביר שלא ייהנו מתרופות אנטיאנגיוגניות סטנדרטיות אך עשויים להגיב לתרופות החוסמות TGF-β, בייחוד בשילוב עם אימונותרפיה מודרנית. בקיצור, חשיפת הדרך שבה הגידולים מותאמים מצביעה על אסטרטגיה ממוקדת יותר התוקפת הן את כלי הדם והן את מקור האנרגיה שעליו סומכים סרטן עמידים אלה.
ציטוט: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
מילות מפתח: סרטן תא כבד הפטוצלולרי, עמידות לאנטיאנגיוגנזה, APOA2, אותות TGF-β, חילוף חומרים של שומנים בסרטן