Clear Sky Science · he
KCTD1 מייצב את c-Myc כדי להגביר PD-L1 ולעכוב את החיסון האנטי‑גידולי בסרטן הכבד ההפטוצלולרית
מדוע הדבר חשוב לטיפול בסרטן בעתיד
רבים מהחולים בסרטן כבד אינם נהנים מהאימונותרפיות המבטיחות ביותר כיום, שנועדו לשחרר את תאי ה‑T של הגוף נגד הגידולים. המחקר הזה בוחן מדוע צורה עיקרית של סרטן הכבד, הסרטן ההפטוצלולרי, עדיין יכולה להתחבא מפני התקפה חיסונית גם בזמן טיפול — ומזהה מתג מולקולרי חדש, הנקרא KCTD1, שעשוי לגרום לכך שתרופות אימונותרפיות קיימות יעבדו טוב יותר.
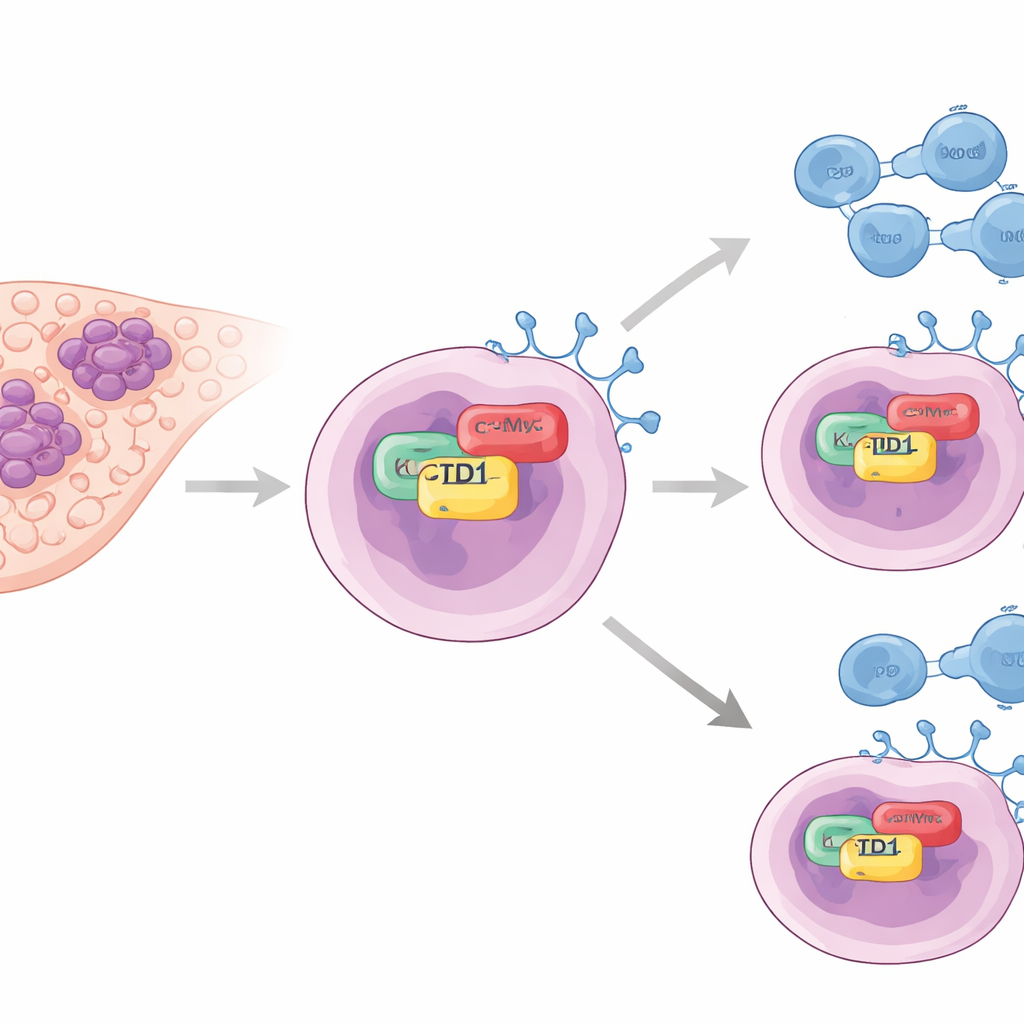
עוזר נסתר ל׳מפסקים׳ של הגידול
המחברים התמקדו בחלבון בשם KCTD1, שזוהה בעבר בקידום גדילת גידולים בכבד אך לא נחקר בהרחבה בהקשר של התחמקות חיסונית. במדגמים של גידולים מחולים הם מצאו שרמות KCTD1 היו גבוהות משמעותית ברקמת כבד ממאירה לעומת כבד נורמלי. באופן חשוב, לגידולים עשירים ב‑KCTD1 היו גם רמות גבוהות של PD‑L1, חלבון על-גבי מתאי הסרטן שמתחבר ל‑PD‑1 על תאי ה‑T וכמו־שזה אומר למערכת החיסון להאט. חולים שלגידוליהם היו רמות נמוכות יותר של KCTD1 נטו לחיות זמן ארוך יותר, מה שמרמז כי חלבון זה קשור הן לחומרת המחלה והן לחוזק המגן החיסוני של הגידול.
קישור הנקודות המולקולריות בתוך תאי הגידול
כדי להבין כיצד KCTD1 מגדיל את PD‑L1, הצוות פנה לקווי תאי סרטן כבד שגודלו במעבדה. כאשר הם הפחיתו KCTD1, רמות חלבון PD‑L1 ירדו וה‑PD‑L1 שנספג נשבר מהר יותר, מה שמעיד כי KCTD1 עוזר לייצב את PD‑L1 ולא רק להפעיל את הגן שלו. באמצעות ניסויי משיכה ביוכימיים ומיקרוסקופיה פלואורסצנטית הם הראו ש‑KCTD1 נקשר פיזית לדוּחף סרטני מרכזי נוסף, חלבון האונקופריוטין c‑Myc, בתוך גרעין התא. האינטראקציה הזו מתרחשת דרך אזורי מגע ספציפיים בשני החלבונים ומובילה ליציבות גדולה יותר של c‑Myc, שבתורה מגבירה את ייצור ה‑PD‑L1. כאשר c‑Myc הורד לבדו, PD‑L1 ירד גם אם KCTD1 היה בשפע, מה שממקם את c‑Myc כקישור האמצעי הקריטי בשרשרת KCTD1–c‑Myc–PD‑L1.
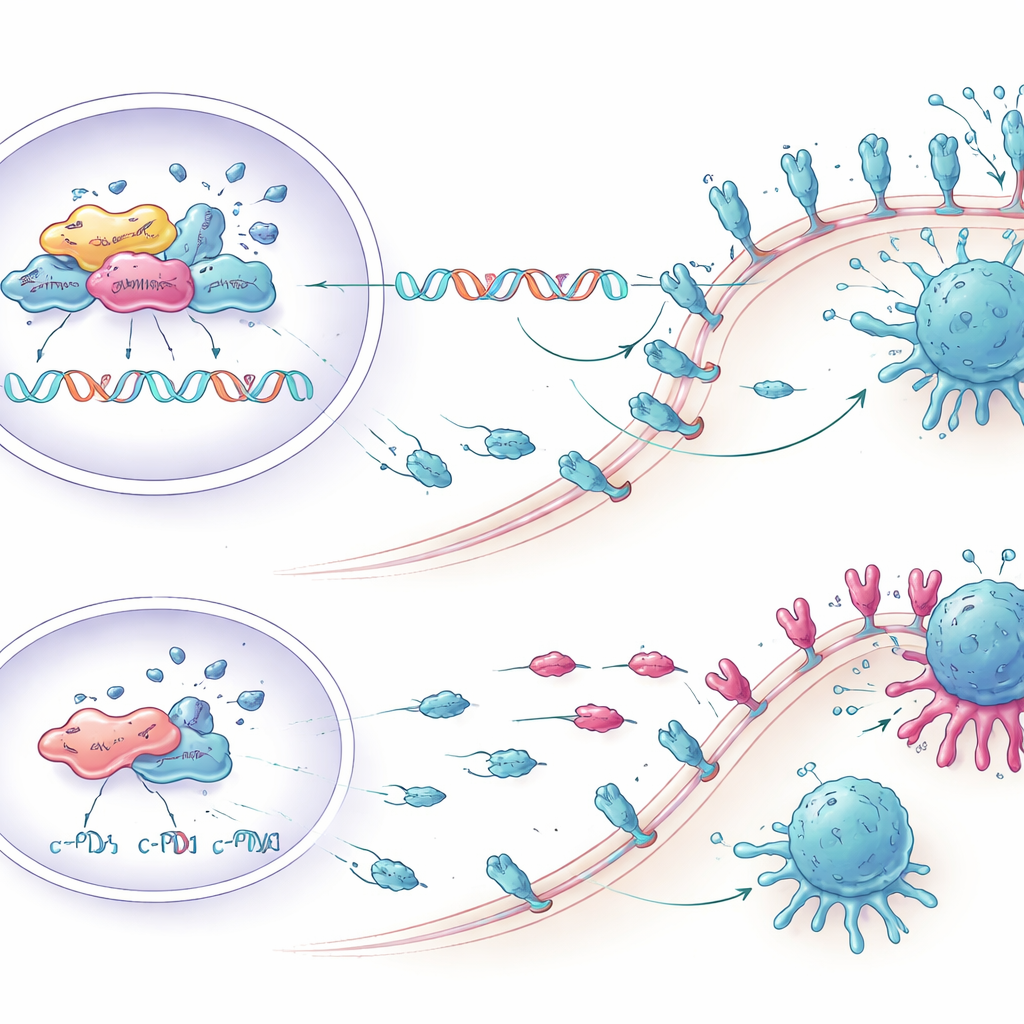
הפעלת תאי T מחדש במעבדה
החוקרים שאלו האם הפחתת KCTD1 יכולה למעשה להגביר את ההתקפה החיסונית. הם גידלו במשותף תאי סרטן כבד אנושיים עם תאי חיסון שנלקחו מתורמי דם. תאי הגידול שהונדסו להכיל פחות KCTD1, ולאור זאת פחות PD‑L1, עוררו תגובות חזקות יותר מתאי CD8 — קוטלי הסרטן העיקריים של המערכת החיסונית. יותר מתאי ה‑T האלה ייצרו מולקולות דלקתיות כגון TNF‑α ואינטרפרון‑גמא, הראו סמנים גבוהים יותר של גדילה והפעלה ונשאו פחות סימנים של תשישות. כתוצאה מכך, יותר תאי גידול נכנסו למוות מתוכנת כאשר KCTD1 דוכא, מה שמדגים שהשינויים המולקולריים התרגמו להגברה ממשית של הריגת הגידול על ידי החיסון.
בדיקת המנגנון בעכברים
כדי לראות אם אותו תבנית מתקיימת בארגוניזמים חיים, הקבוצה השתילה תאי סרטן כבד עכבריים חסרי KCTD1 ישירות בכבדם של עכברים. לגידולים עם KCTD1 מופחת נוצרו נודולים פחותים וקטנים יותר, חלוקת התאים הייתה איטית יותר והיו יותר תאי גידול הנמצאים במוות תאי. גידולים אלה גם הביעו פחות c‑Myc ו‑PD‑L1. הסרה של תאי CD8 מהעכברים מחקה חלק גדול מהתועלת הזו, מה שמעיד על כך שהאטת הגידול תלויה במידה רבה בפעילות תאי ה‑T. לבסוף, כשהחוקרים שילבו דיכוי KCTD1 עם נוגדן אנטי‑PD‑1 — תרופה קיימת החוסמת נקודות עצירה חיסוניות — העכברים חוו את העומס הגידולי הקטן ביותר ואת הרמות הגבוהות ביותר של תאי CD4 ו‑CD8 שחדרו לתוך הגידולים שלהם.
מה זה יכול betekenen עבור מטופלים
סיכום הממצאים מראה כי KCTD1 הוא מתאם מרכזי שמייצב את c‑Myc, מעלה את PD‑L1 על תאי סרטן כבד ומחליש את התקפת תאי CD8. שיבוש המסלול הזה עושה את הגידולים פגיעים יותר למערכת החיסון ורגישים יותר לתרופות החוסמות PD‑1 בעכברים. עבור מטופלים, הדבר מציע כי תרופות המיועדות ל‑KCTD1 או לממשק המגע שלו עם c‑Myc עשויות בעתיד להיות משולבות עם אימונותרפיות קיימות כדי לאפשר ליותר חולים עם סרטן כבד להנות מבקרת חיסון ממושכת על מחלתם.
ציטוט: Zhong, D., Long, S., Dai, Y. et al. KCTD1 stabilizes c-Myc to upregulate PD-L1 and suppress anti-tumor immunity in hepatocellular carcinoma. Cell Death Discov. 12, 129 (2026). https://doi.org/10.1038/s41420-026-02975-6
מילות מפתח: סרטן הכבד ההפטוצלולרי, אימונותרפיה נגד גידולים, מסלול PD‑1 PD‑L1, אותות c‑Myc, חיסון תאי T נגד גידולים