Clear Sky Science · he
ניתוח רב-אומי מגלה שונות ואוכלוסיות פונקציונליות של תאי אם אוליגודנדרוציטים שעובדו מתאים עצביים אנושיים
מדוע חשוב להגן על הבידוד העצבתי
החיווט של המוח שלנו תלוי בציפוי שומני שנקרא מיאלין, העוטף את סיבי העצב בדומה לבידוד בכבלים חשמליים. כאשר המיאלין נפגע, כפי שקורה במחלות כמו טרשת נפוצה ובמצבים נוספים, האותות מאטים או מתנתקים, מה שגורם לבעיות בתנועה, בראייה ובחשיבה. המחקר הזה חוקר קבוצה מיוחדת של תאים אנושיים שיכולים לשקם מיאלין ושואל שאלה מעשית: אילו תאים מתאימים ביותר לטיפולי תאים עתידיים לשיקום בידוד חיוני זה?
מתאי התחלה של המוח ליצרני מיאלין
החוקרים התחילו מתאי אם עצביים אנושיים — תאי התחלה רב-תכליתיים שנלקחו מרקמת מוח עוברית שכבר נטועים להפוך לתאי מערכת העצבים. במעבדה הם עוררו תאים אלו להפוך לתאי אם אוליגודנדרוציטים (hOPCs), שמהווים את המקודמים הישירים לתאים המייצרים מיאלין. תחת המיקרוסקופ התאים השתנו מצורות עגולות ופשוטות לצורות מורכבות יותר עם הסתעפויות מרובות, והבעירו חלבונים מובחנים שמייצגים שלבים בדרך לתא בוגר שיוצר מיאלין. כך נוצר מקור מהימן ובטוח למדי של מקדמי בניית מיאלין אנושיים לניתוח מפורט.
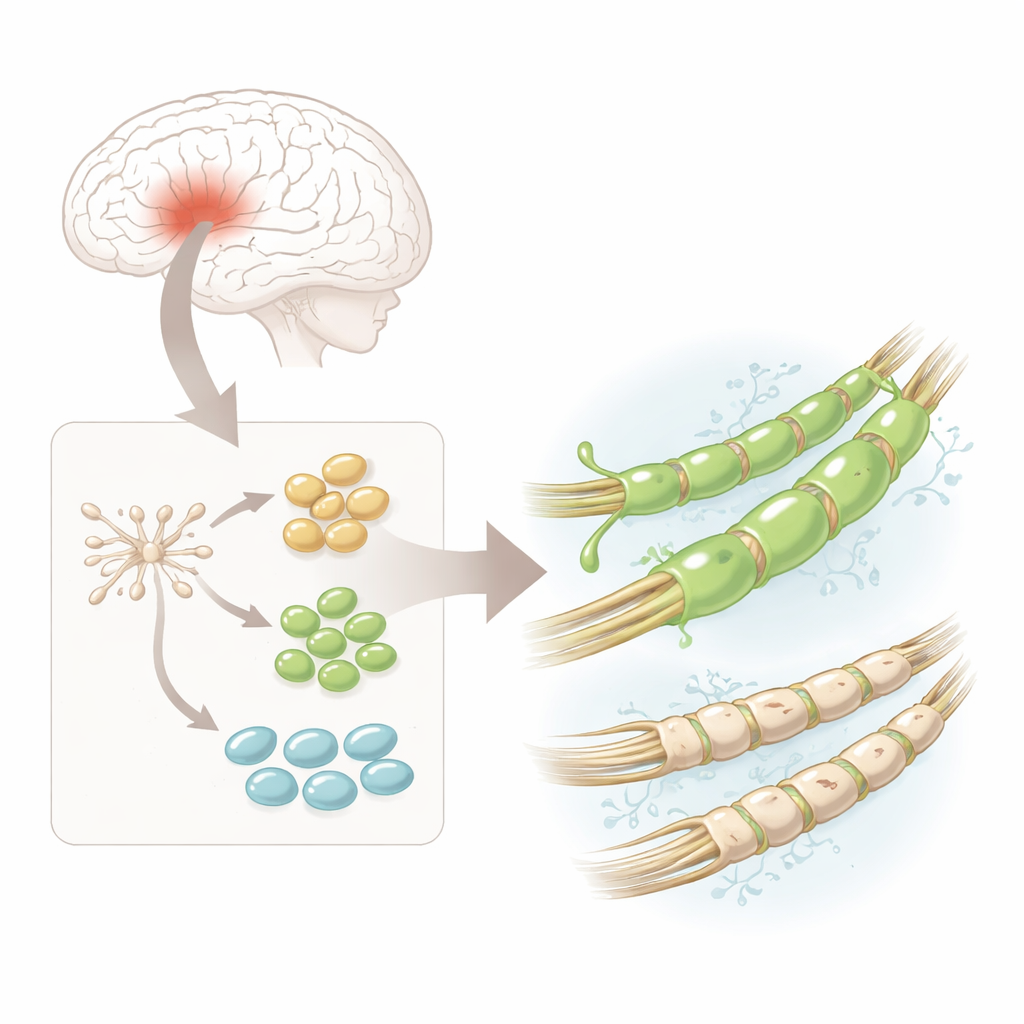
סוג תא אחד, שונות נסתרת רבה
באמצעות ריצוף RNA בתא-יחיד — שיטה שמזהה אילו גנים פעילים באלפי תאים בודדים — הצוות גילה כי ה-hOPCs אינם זהים זה לזה. במקום זאת הם התרכזו לשלוש שלבים עיקריים: "קדם-פרוגניטורים" מוקדמים, פרוגניטורים מחויבים יותר ותאים המתקרבים לזהות אוליגודנדרוציטית בוגרת. בכל השלבים הללו בלט גן אחד: PDGFRA, הממקודד לקולטן ממברנלי. שיטת דימות רבת-רגישות בשם RNA-Scope אישרה שהמסר והחלבון של PDGFRA מצויים בכמויות גדולות יותר משאר הסמנים המרכזיים בכל שלב, מה שמרמז כי הקולטן הזה עשוי להגדיר תת-אוכלוסייה בעלת יכולת גבוהה במיוחד לבנות מיאלין.
מיון תאי התיקון העוצמתיים ביותר
כדי לבדוק רעיון זה, המדענים הפרידו את ה-hOPCs לשתי קבוצות על בסיס נוכחות קולטן PDGFR-α על פני הממברנה. לאחר מכן השוו בין תאים חיוביים ל-PDGFR-α, תאים שליליים ותרבית לא ממוינת במגוון מבחנים פונקציונליים. כאשר הושתלו בעכברי "שיברר" — שאינם מסוגלים ליצור מיאלין תקין — התאים החיוביים ל-PDGFR-α ייצרו מיאלין צפוף ומדוד יותר סביב הסיבים העצביים בהשוואה לקבוצות האחרות. תאים אלה גם נדדו למרחקים גדולים יותר והתרבו מהר יותר במבחני מעבדה. במילים אחרות, אוכלוסיית ה-PDGFR-α–חיובית הייתה היותר פעילה במעבר למקומות הנדרשים, בהתרבות ובשיקום הבידוד.
אותות פנימיים שמניעים גדילה ותיקון
בהעמקה נוספת השוותה הקבוצה את פעילות הגנים בין תאים חיוביים ל-PDGFR-α לבין תאים שליליים. הם מצאו שהתאים החיוביים הפעילו רשתות גנים המעורבות בצמיחת תאי גליה וביצירת מיאלין, וכן מספר מסלולי איתות פנימיים מרכזיים. שני מסלולים בולטים במיוחד היו PI3K–AKT–mTOR, הקשור מזה זמן לצמיחת תאים ולייצור מיאלין, ואיתות TGF-β, שמשפיע על בחירת גורלות של תאים מוחיים צעירים. הנתונים הציעו כי הפעלת PDGFR-α מזינה את PI3K–AKT–mTOR, אשר בתורה מחזק את אותות ה-TGF-β, וביחד דוחפים תאים לעבר היותם יצרני מיאלין יעילים.
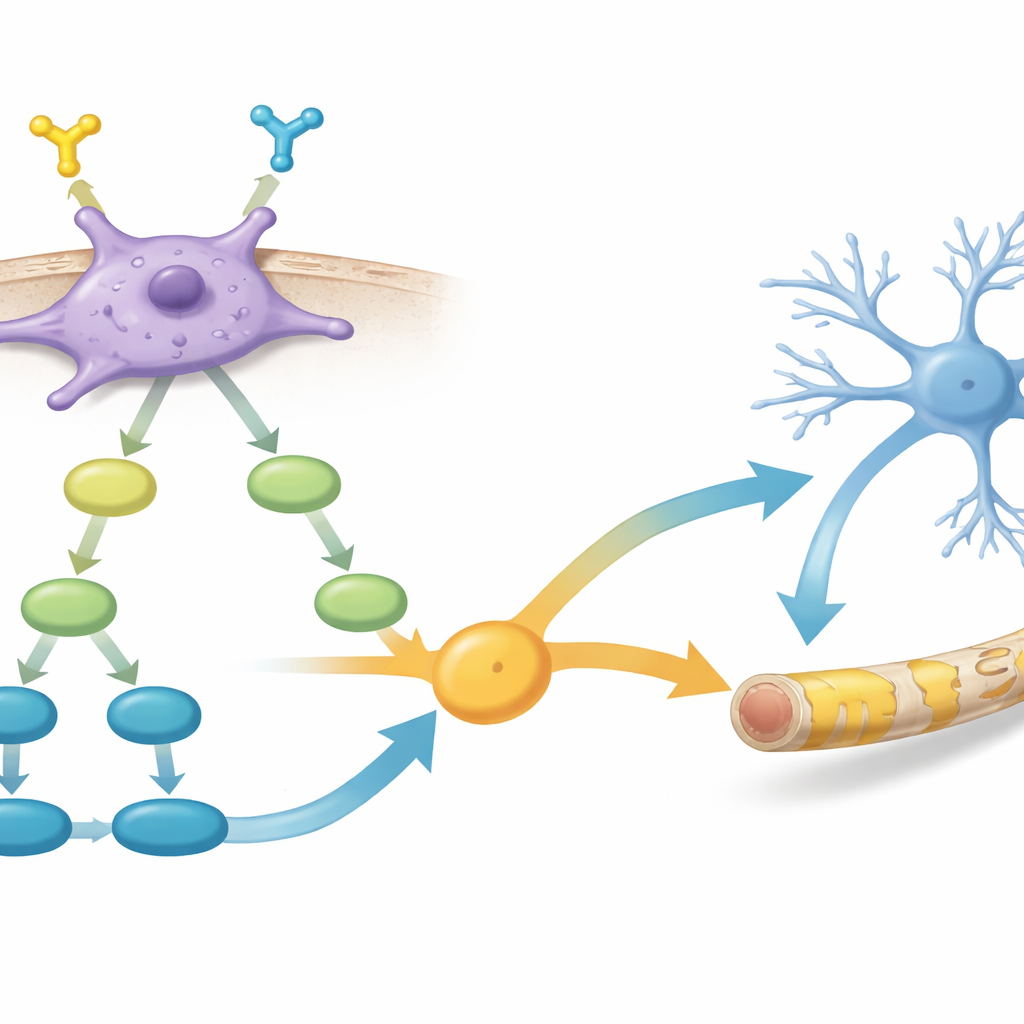
הגברת תיקון המיאלין בעזרת מסייע כימי
החוקרים שאלו האם ניתן לשפר עוד את התאים המבטיחים הללו. הם טיפלו בתאי hOPCs חיוביים ל-PDGFR-α במולקולה קטנה שמפעילה את מסלול ה-TGF-β ובחנו הן פעילות גנטית והן התנהגות. לאחר הטיפול הראו התאים רמות מוגברות של כמה גנים הקשורים למיאלין וייצרו מעטפות מיאלין עבות ומלאות יותר כאשר הושתלו בעכברי שיברר, בהשוואה לתאים חיוביים ל-PDGFR-α שלא טופלו. ממצאים אלה תומכים ברעיון כי כוונון זהיר של אותות פנימיים בתאי פרוגניטור שנבחרו היטב יכול לשפר עוד את הביצועים שלהם ככלי חי לתיקון מיאלין.
ממה זה מעמיד טיפולים עתידיים
ללא-מומחים, המסר המרכזי הוא שלא כל תאי המקדמים בניית מיאלין שווים. בשילוב כלים רבי-עוצמה לקריאת גנים ודימות, המחקר מזהה תת-קבוצה בולטת — hOPCs חיוביים ל-PDGFR-α — שנודדת טוב יותר, מתחלקת יותר ומשקמת מיאלין ביעילות רבה יותר מעמיתיה. הוא גם מדגיש מסלולי איתות פנימיים שאפשר לדחוף כימית כדי להפוך תאים אלה לעוצמתיים עוד יותר. יחד, תובנות אלה מסמנות מפת דרכים לתכנון טיפולי תאים בטוחים ויעילים יותר לשחזור בידוד המוח במחלות שבהן המיאלין נאבד.
ציטוט: Ye, D., Zhou, H., Qu, S. et al. Multi-omics reveals heterogeneity and functional populations of oligodendrocyte progenitor cells induced by human neural stem cells. Cell Death Discov. 12, 112 (2026). https://doi.org/10.1038/s41420-026-02971-w
מילות מפתח: תיקון מיאלין, תאי אם אוליגודנדרוציטים, תאי אם עצביים, טיפולי תאים, ריצוף RNA תא-יחיד