Clear Sky Science · he
התקשורת בין ביואנרגטיקה מיתוכונדריאלית ל‑SASP קובעת את יעילות הסנוליטיקה במהלך סנescence מוּחִקת‑טיפול
למה לחסל "תאי זומבי" של סרטן כל כך מסובך
לא הרבה מהתרופות המודרניות נגד סרטן הורגות כל תא גידול באופן מידי. במקום זאת, חלק מהתאים נכנסים למצב גבולי שנקרא סנescence: הם מפסיקים להתחלק אבל נשארים בחיים, במין מצב של "תאי זומבי". תאים שנכנסו למצב זה בעקבות טיפול יכולים בהתחלה להיות מועילים, אך אם הם מתמשכים הם עלולים לעודד הישנות, עמידות ותופעות לוואי. מדענים בוחנים לכן תרכובות סנוליטיות שנועדו להרוג באופן סלקטיבי תאים מזדקנים. מאמר זה שואל שאלה שבמבט ראשון נראית פשוטה אך מטעה: מדוע חלק מתאי הסרטן המזדקנים מתים כאשר נחשפים לסנוליטיקה, בעוד אחרים שורדים בעקשנות?
תחנות כוח שמזכירות את העבר שלהן
בלב המחקר עומדות המיטוכונדריות, תחנות הכוח הזעירות בתוך התאים. המחברים בדקו האם האופן שבו המיטוכונדריות בורקות דלקים שונים — כגון סוכרים, שומנים וחומצות אמינו — משפיע על הרגישות של תאים מזדקנים לסנוליטיקה שמכוונת לחלבון הישרדות בשם BCL‑xL. באמצעות מבחן בר־קנה מידה (MitoPlate S‑1) הם ערכו "טביעת אצבע" תפקודית של פעילות מיטוכונדריאלית במספר שורות תאים סרטניות לפני ואחרי שהגרמו לסנescence בעזרת טיפולים שונים (תרופות המגרות נזק לדנ"א, חוסמי מיטוזה, סטרס חמצוני או מעכבי מחזור התא). הם מצאו שסנescence הנגרם על־ידי טיפול לא יצר מצב מיטוכונדריאלי אחיד אחד. במקום זאת, כל תרופה הותירה "טביעת ביואנרגטיקה" ייחודית, ששינתה עד כמה ובאיזה עוצמה המיטוכונדריות יכולות לנצל מקורות אנרגיה שונים. מה שחשוב הוא שהגמישות הזו הייתה מסווגת מעל קו בסיס קיים: התצורה המיטוכונדריאלית המקורית של תאי האב קבעה גבול עליון — "תקרה" — על עוצמת תגובת הסנוליטיקה העתידית.
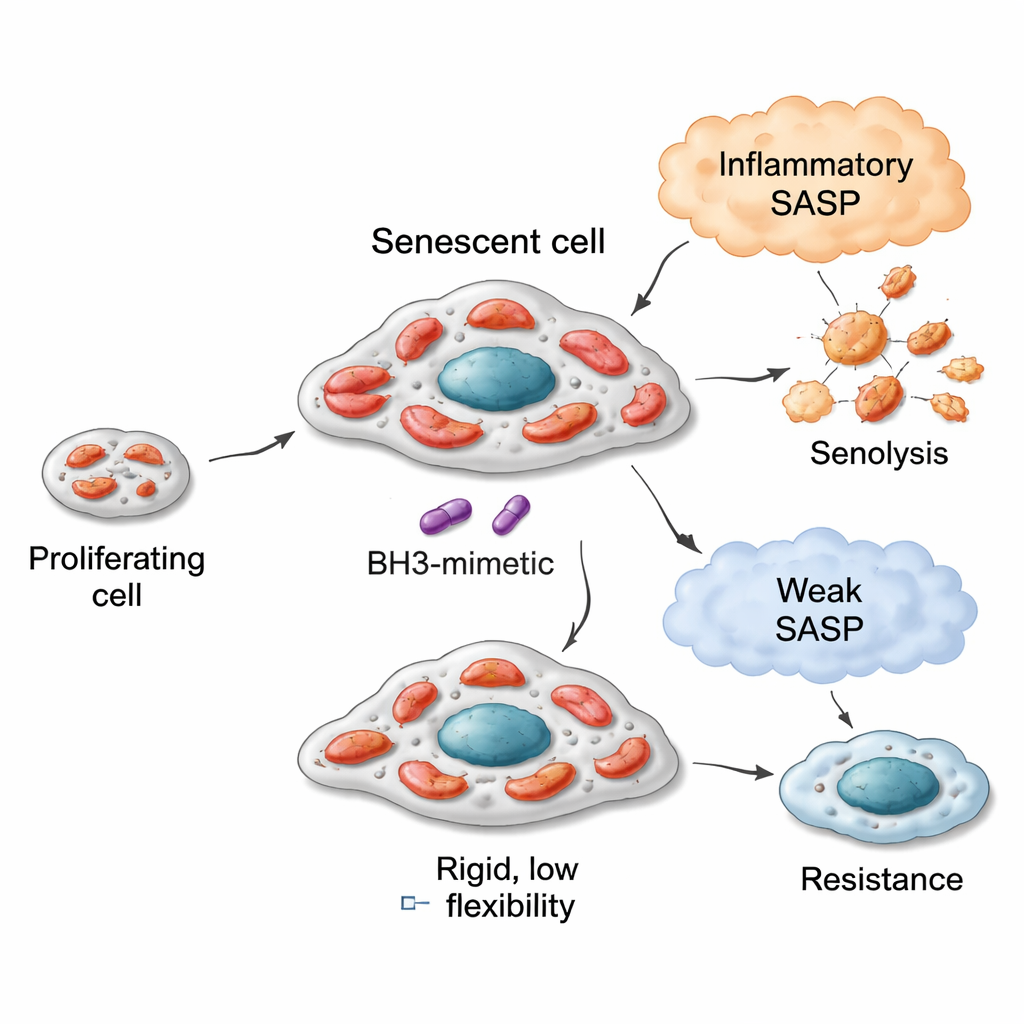
מנועים גמישים, דלקים שונים ורגישות לסנוליטיקה
במודלים של סרטן ריאה, שד ומעי גס, תאים מזדקנים עם מיטוכונדריות גמישות יותר — שיכולות לחמצן מגוון רחב יותר של דלקים — נטו להיות פגיעים יותר לסנוליטיקה המכוונת ל‑BCL‑xL כמו נאויטוקלקס (navitoclax, ABT‑263) ו‑A1331852. למשל, תאי ריאה שנכנסו לסנescence לאחר חשיפה לבליאומיצין פיתחו מיטוכונדריות שהשתמשו בתיבוליות גבוהה במגוון מצעדי תזונה, במיוחד אלה הקשורים לשבירת חומצות שומן ולמסלולי חומצות אמינו מסוימים. תאים אלה היו רגישים מאוד לסנוליטיקה. לעומת זאת, תאים שהוכנסו לסנescence על ידי מעכב CDK4/6 (פלבוסיקליב) הראו רפרטואר מטבולי צר יותר וענו באופן גרוע לאותם סנוליטיים. עם זאת, למערכת זו היו מגבלות: תאי שד גם כן יכלו להפוך לגמישים מטבולית לאחר סנescence, אבל מאחר שמטוכונדריותיהם המקוריות היו פחות מוכנות לאפופטוזה, תגובת הסנוליטיקה שלהם הייתה מתונה. תאי מעי גס עם מכניזם אפופטוטי פגום נשארו עמידים ללא קשר לשינויי המטבוליזם שלהם. מדד יחיד — עד כמה תאים חימצנו את הדלק סוקסינאט במצב הבסיס — שימש כאינדיקטור פשוט לקיבולת המיטוכונדריאלית המיוחסת הזאת.
כאשר המטבוליזם משוחח עם דלקת
תאים מזדקנים ידועים ב‑SASP שלהם, שֶׁנֶּהֶגֶּת כסליל של גורמי דלקת וצמיחה המופרשים ויכולים להשפיע על רקמות סמוכות. הצוות חקר כיצד מטבוליזם מיטוכונדריאלי מתחבר להתנהגות המופרשת הזו על ידי שימוש בתאים שמונדדו בדיווח עבור miR‑146a, מיקרו‑RNA שמופעל על־ידי הבקר הדלקתי הראשי NF‑κB. הם מצאו שלמרות שפרופילי ה‑SASP הכוללים הוכתבו במידה רבה על ידי סוג התא, רק מצבי סנescence מסוימים הפעילו את ציר NF‑κB/miR‑146a. אלה היו אותם המצבים שהגיבו היטב לסנוליטיקה המכוונת ל‑BCL‑xL. חשיבותית, תאים מזדקנים עם SASP דלקתי־חיובי הראו גם שימוש מוגבר בחמצון חומצות שומן ועלייה בטרנסקריפציה של גנים שמובילים חומצות שומן ארוכות־שרשרת לתוך המיטוכונדריה. חסימת כניסת חומצות השומן בעזרת תרופת אתומוקסיר צמצמה את הפעלת miR‑146a מבלי להפוך את הסנescence במלואו, מה שמרמז כי בחירת דלק מיטוכונדריאלי מסייעת לאשר SASP דלקתי שמאפשר סנוליטיקה.
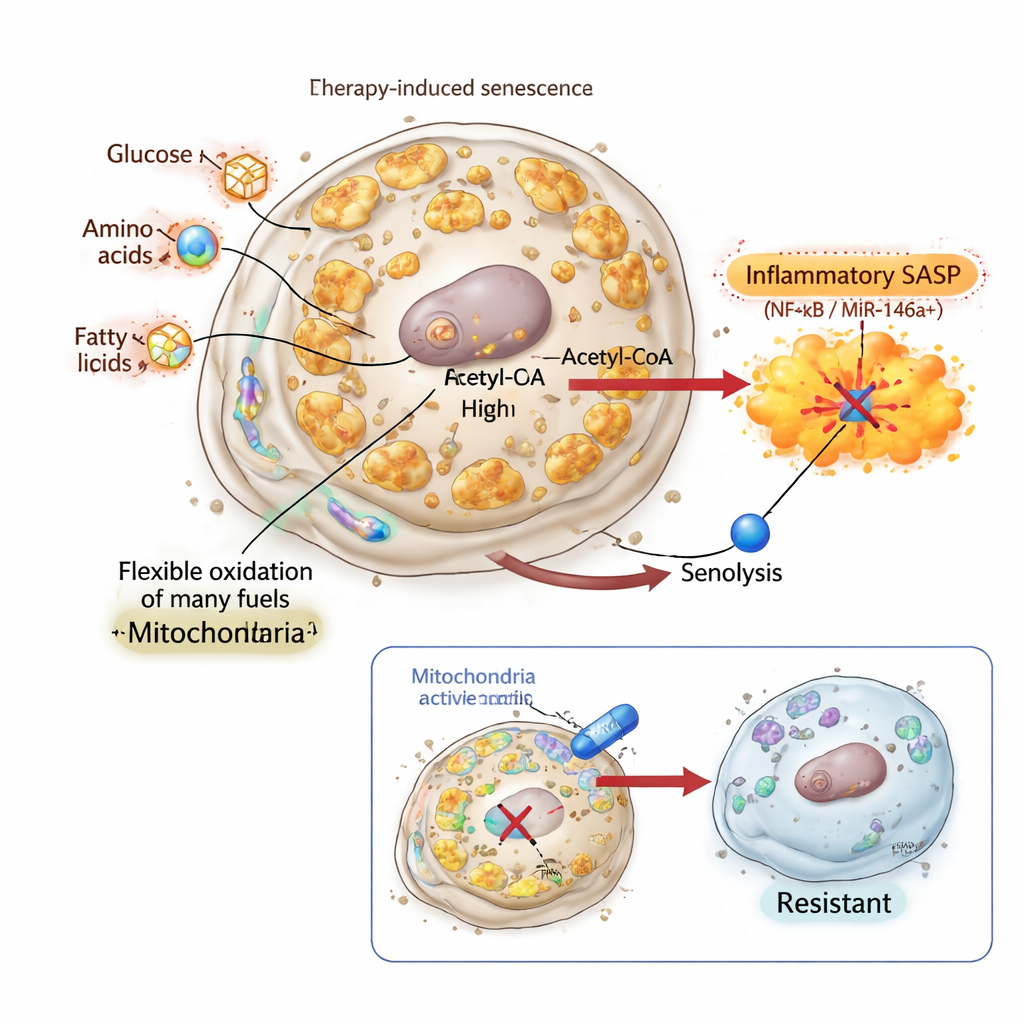
השתקת האות ויצירת תאי סנescence בלתי־הרגים
כדי לבדוק האם SASP הדלקתי אכן נחוץ להריגה בסנוליטיקה, החוקרים פנו לאינפלאַכְרוֹמן, תרכובת הקושרת חלבוני כרומטין HMGB1 ו‑HMGB2 וחוסמת את תפקידם בהפעלת גני SASP. בתאי ריאה ושד, אינפלכרומן עורר פנוטיפ סננס־טיפי: התאים הפכו גדולים, הפסיקו להתחלק והצטברו סימני הזדקנות. מסת המיטוכונדריה ופעילות הביואנרגטיקה שלהם עלו משמעותית, ושימושם בדלקים עוצב מחדש באופן ברור. עם זאת, ה‑SASP שלהם היה מוחלש ומדווח miR‑146a נותר בעיקר שקט. באופן בולט, אותם תאי סנescence חסרי SASP היו עמידים לחלוטין לסנוליטיקה המכוונת ל‑BCL‑xL, על אף שהיו להם מיטוכונדריות פעילות מבחינה ביואנרגטית, מיתוג מחדש של שימוש בדלקים וירידה בביטוי של הגן האנטי‑אפופטוטי הקלאסי BCL2. זה הראה ששינויים מיטוכונדריאליים לבדם אינם מספיקים; בלי פלט דלקתי מוּנחה על‑ידי מיטוכונדריה, ה"מכה השנייה" של הסנוליטיקה נכשלת.
מה משמעות הדבר לטיפולים עתידיים בסרטן
לקריאה פופולרית, מסקנת המחקר היא כי חיסול תאי "הזומבי" שנגרמו על ידי טיפול נשלט על‑ידי מעגל רב‑שכבתי. ראשית, הבריאות והחיבור המקורי של המיטוכונדריה של תא הגידול קובעים עד לאיזה טווח הסנוליטיקה יכולה להגיע. שנית, הטיפול הספציפי שגורם לסנescence יכול לדחוף את המטבוליזם המיטוכונדריאלי לכיוון של גמישות רבה או מועטה, ולהזיז את התאים קרוב יותר או רחוק יותר ממפתן האפופטוזה. שלישית — ובהכרחיות — סנוליטיקה פועלת היטב רק אם התכנות המטבולי מצליח להפעיל תוכנית SASP דלקתית שמתקשרת חזרה לגרעין. בלי תקשורת דלקתית זו, תאים מזדקנים יכולים להפוך למצב סיום חסר מוצא ועמיד לתרופות. מבחינה מעשית, הדבר מרמז שטיפולים עתידיים עשויים להיות מותאמים על‑ידי בדיקות פונקציונליות של גמישות מיטוכונדריאלית ודלקת SASP בגידולים, ולאחר מכן בחירה בקומבינציות של תרופות שמעוררות סנescence וסנוליטיקה כך שוודאי ה"תאים הזומבים" יישארו לא רק קפואים במקום, אלא מוכנים להסרה.
ציטוט: Llop-Hernández, À., Verdura, S., López, J. et al. Mitochondrial bioenergetics-SASP crosstalk determines senolytic efficacy in therapy-induced senescence. Cell Death Discov. 12, 103 (2026). https://doi.org/10.1038/s41420-026-02967-6
מילות מפתח: הזדקנות תאית, מיטוכונדריה, סנוליטיקה, מטבוליזם של סרטן, SASP דלקתי