Clear Sky Science · he
מנגנון חדש בתגובת הנוירונים להיפוקסיה: הפעלת מיטופאגיה תלויה PINK1 מתווכת על‑ידי HIF‑1α/STOML2 כנגד פגיעה עצבית
מדוע תגובת המוח לחוסר חמצן חשובה
מצבים נפוצים רבים — כולל שבץ, דום נשימה בשינה, אי‑ספיקת לב ואפילו חשיפה לגובה רב — מפחיתים את אספקת החמצן למוח. כשמתמעט החמצן, תאי המוח בסכנת נזק קבוע, שעשוי להוביל לבעיות זיכרון וסיבוכים נוירולוגיים אחרים. המחקר הזה חושף מערכת הגנה פנימית שנוירונים מפעילים בשלבים הראשונים של חוסר חמצן כדי לשמור על קיומם ותפקודם. הבנת המערכת עשויה לפתוח אפשרויות לטיפולים חדשים שמגנים על המוח לפני שהנזק נהפך חמור.
צרות מוקדמות, אבל עוד לא אסון
כדי לחקור איך המוח מגיב לחוסר חמצן, החוקרים חשפו עכברים לאוויר עם כ‑13% חמצן — דומה להתגוררות בפלטו גבוה — למשכי זמן שונים. בימים הראשונים, בעלי החיים הופיעו נורמליים במבחני זיכרון ומבוך ותאי המוח נראו בריאים במיקרוסקופ. רק לאחר שבוע מלא של חמצן מופחת החלו העכברים להראות אובדן זיכרון ברור ומבנה תאי מוח מבולגן. דפוס זה מצביע על כך שבשלבים המוקדמים הנוירונים אינם קורבנות פסיביים של חוסר חמצן; במקום זאת, הם מפעילים תגובות הגנתיות שמעכבות או מונעות נזק.
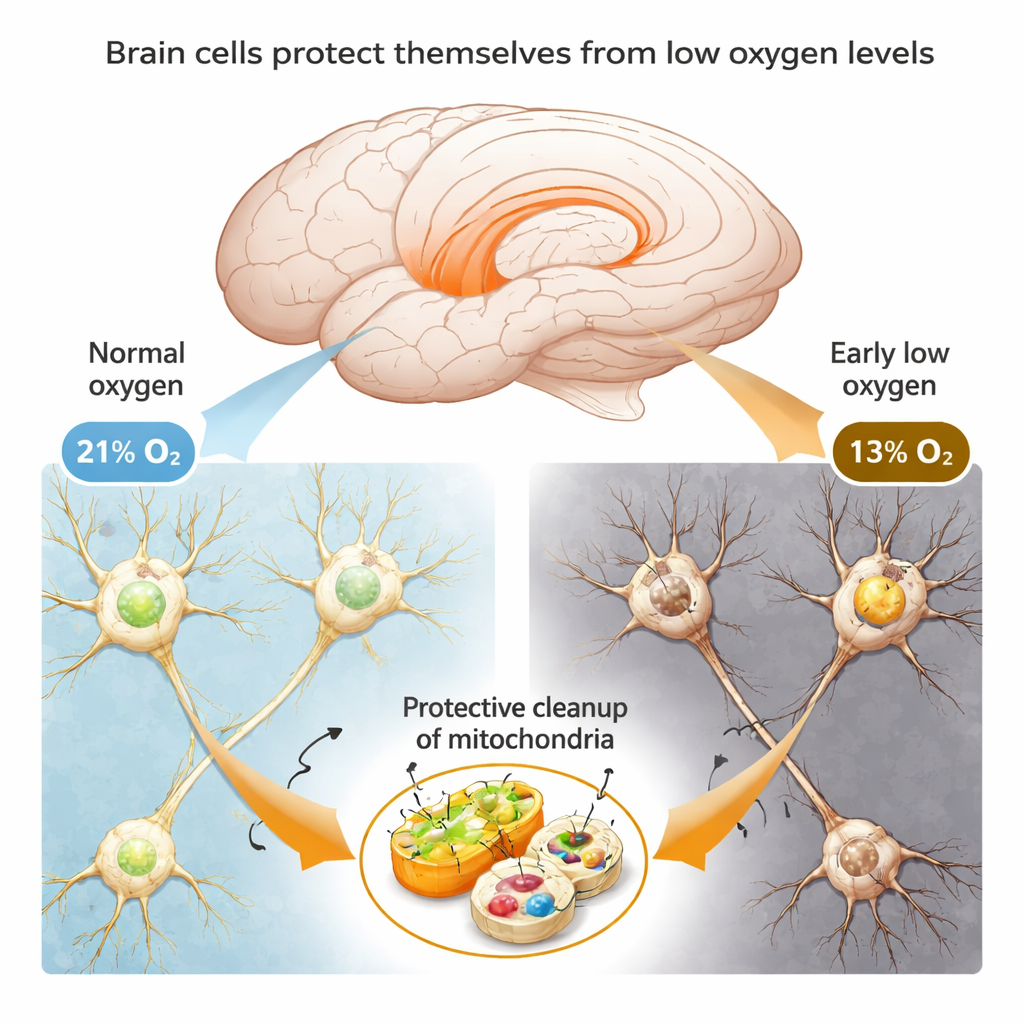
ניקיון תאי: הוצאת תחנות כוח מקולקלות
מוקד מרכזי במחקר הוא תחנות הכוח של התא — המיטוכונדריות — החשובות במיוחד בנוירונים מכיוון שחשיבה וזיכרון דורשים כמויות אנרגיה גדולות. בתנאי חוסר חמצן, המיטוכונדריות עלולות להיכשל ולדלוף תוצרי לוואי מזיקים הפוגעים בתאים. הצוות מצא שבשלב המוקדם של היפוקסיה הנוירונים מגבירים זמנית תהליך ניקוי מיוחד שנקרא מיטופאגיה, שמסלק באופן סלקטיבי מיטוכונדריות פגועות ושומרת על בריאות השאר. גם במוחות עכברים וגם בתאים עצביים ממקור אנושי שגודלו במעבדה, סמנים של התהליך הזה עלו זמן קצר אחרי ירידת החמצן, בדיוק כאשר התאים עדיין תפקדו היטב. כאשר המדענים חסמו כימית את המיטופאגיה, שרידיות התאים ירדה וסימני פגיעה עלו, מה שהראה שהשלב הזה של ניקוי חיוני להגנה.
שרשרת תגובתית מגוננת בתוך הנוירונים
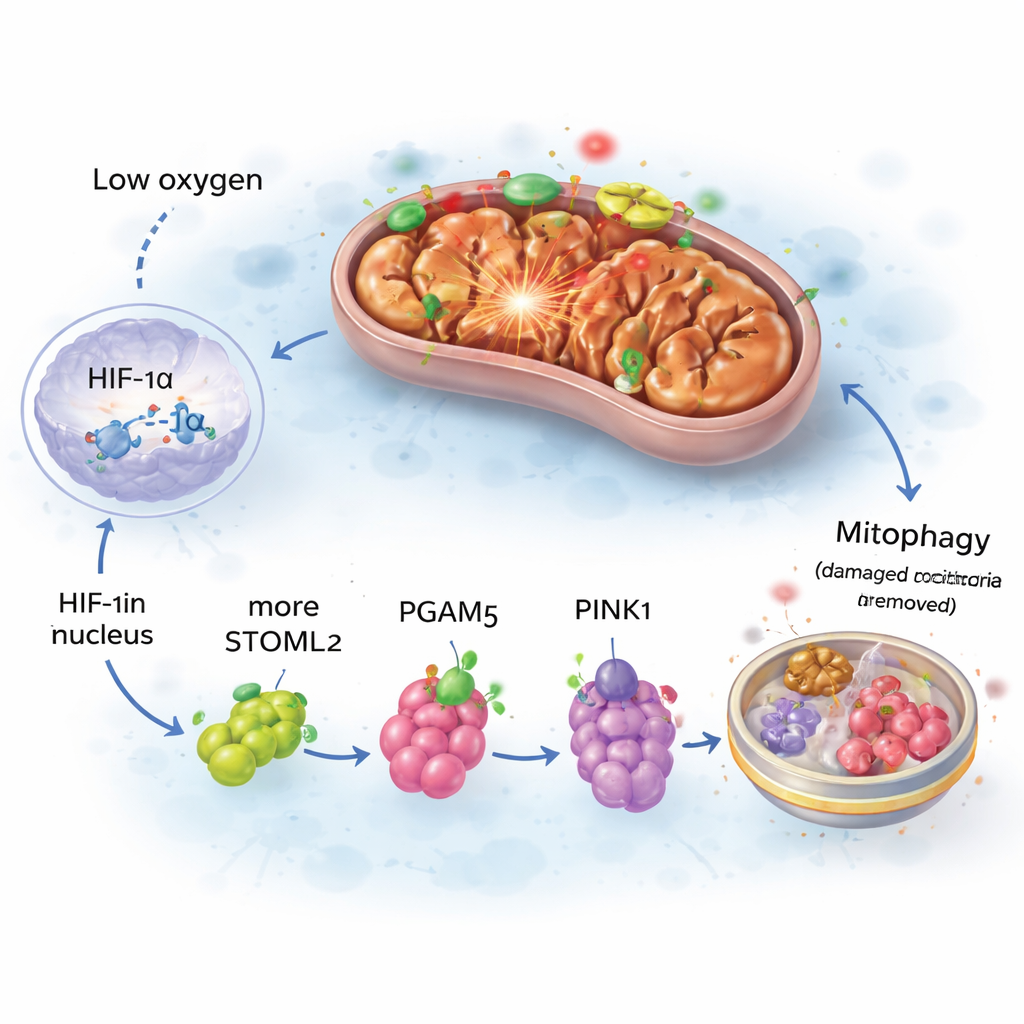
בהעמקה, החוקרים עקבו אחרי האופן שבו נדלקת מערכת הניקוי המיטוכונדריאלית. חוסר חמצן מייצב חלבון חישה בשם HIF‑1α, הנודד לגרעין התא ומשנה פעילות גנים. אחד ממטרותיו הוא STOML2, חלבון שמועבר לפני שטח המיטוכונדריה. שם STOML2 מסייע לשמור על חלבון נוסף, PGAM5, בצורתו המלאה. PGAM5 באה ומאפשרת למולקולה נוספת, PINK1, להצטבר על השכבה החיצונית של מיטוכונדריות פגועות. PINK1 מסמן אז את תחנות הכוח הלקויות להסרה על‑ידי מכונת המיחזור של התא. כאשר הצוות הקטין באופן סלקטיבי את HIF‑1α, STOML2, PGAM5 או PINK1 במוחות עכברים, גל המיטופאגיה המוקדם נעלם והנוירונים סבלו יותר מפגיעה במהלך חשיפה לחוסר חמצן. השלבים — HIF‑1α ל‑STOML2 ל‑PGAM5 ל‑PINK1 — צמחו כמסלול מגן מרכזי.
לאמן את המוח באמצעות חוסר חמצן לסירוגין
המחקר גם בדק אסטרטגיית "התניה" שנקראת היפוקסיה לסירוגין, שבה עכברים חוו מחזורים קצרים וחוזרים של חוסר וחזרת חמצן נורמלי לפני חשיפה לחוסר חמצן ממושך. הטיפול המוקדם הפעל את אותו מסלול HIF‑1α/STOML2/PGAM5/PINK1 והגביר מיטופאגיה במוח. למרבה ההפתעה, עכברים שעברו היפוקסיה לסירוגין שמרו על ביצועי הזיכרון גם לאחר שבוע של חוסר חמצן רציף, בעוד בעלי החיים שלא טופלו הידרדרו. תוצאות אלו מרמזות כי פרקי חוסר חמצן מבוקרים יכולים לאמן את הנוירונים להפעיל את מערכות הניקוי שלהם ביתר יעילות, בדומה לאופן שבו אימון גופני מכין את השרירים להתמודד עם עומס.
מה משמעות הממצאים להגנה על המוח
באופן פשוט, המחקר מראה שלנוירונים יש תוכנית חירום פנימית למצבי חוסר חמצן: הם חשים במהירות את השינוי, מעצימים שרשרת חלבונים מונעת ופונים לסלק תחנות אנרגיה שאינן מתפקדות לפני שהן יגרמו לנזק נרחב. כאשר תוכנית זו מופרעת, תאי המוח נחשפים לפגיעות רבה יותר. על‑ידי מיפוי המסלול בפירוט והדגמה כי היפוקסיה לסירוגין יכולה להפעילו בבטחה, העבודה מצביעה על טיפולים עתידיים שעשויים לדמות או לחזק את ההגנה הטבעית הזו. גישות כאלה עשויות בעתיד לסייע להגנה על המוח מפני שבץ, הפרעות נשימה שקשורות לשינה ומצבים אחרים שבהם אספקת החמצן בסיכון.
ציטוט: Li, Y., Xu, Z., Tian, Z. et al. Novel mechanism of neuronal hypoxia response: HIF-1α/STOML2 mediated PINK1-dependent mitophagy activation against neuronal injury. Cell Death Discov. 12, 104 (2026). https://doi.org/10.1038/s41420-026-02960-z
מילות מפתח: היפוקסיה מוחית, מיטופאגיה, הגנה על נוירונים, היפוקסיה לסירוגין, מיטוכונדריה