Clear Sky Science · he
PDHA1 מעלה את העמידות לפרופטוזיס בתאי סרטן הערמונית העמידים לאנואקיס על ידי ויסות כלפי מעלה של AIFM2
מדוע חלק מתאים של סרטן הערמונית מסרבים למות
כשתאי סרטן נפרדים מגידול ונכנסים למחזור הדם, רובם היו אמורים למות לפני שיגיעו לאיבר חדש. עם זאת, מיעוט מסוכן שורד, נע ויוצר גרורות שלעתים קרובות קטלניות. המחקר הזה שואל שאלה מרכזית: מה מאפשר לתאי סרטן ערמונית מסוימים לעמוד בפני צורת מוות תאית שמתרחשת בדרך כלל ברגע שהם מאבדים את המגע עם רקמת המקור שלהם? על ידי חשיפת מעגל הישרדות סמוי בתוך תאים אלה, המחקר מצביע על דרכים חדשות לחסום גרורה במקור שלה.
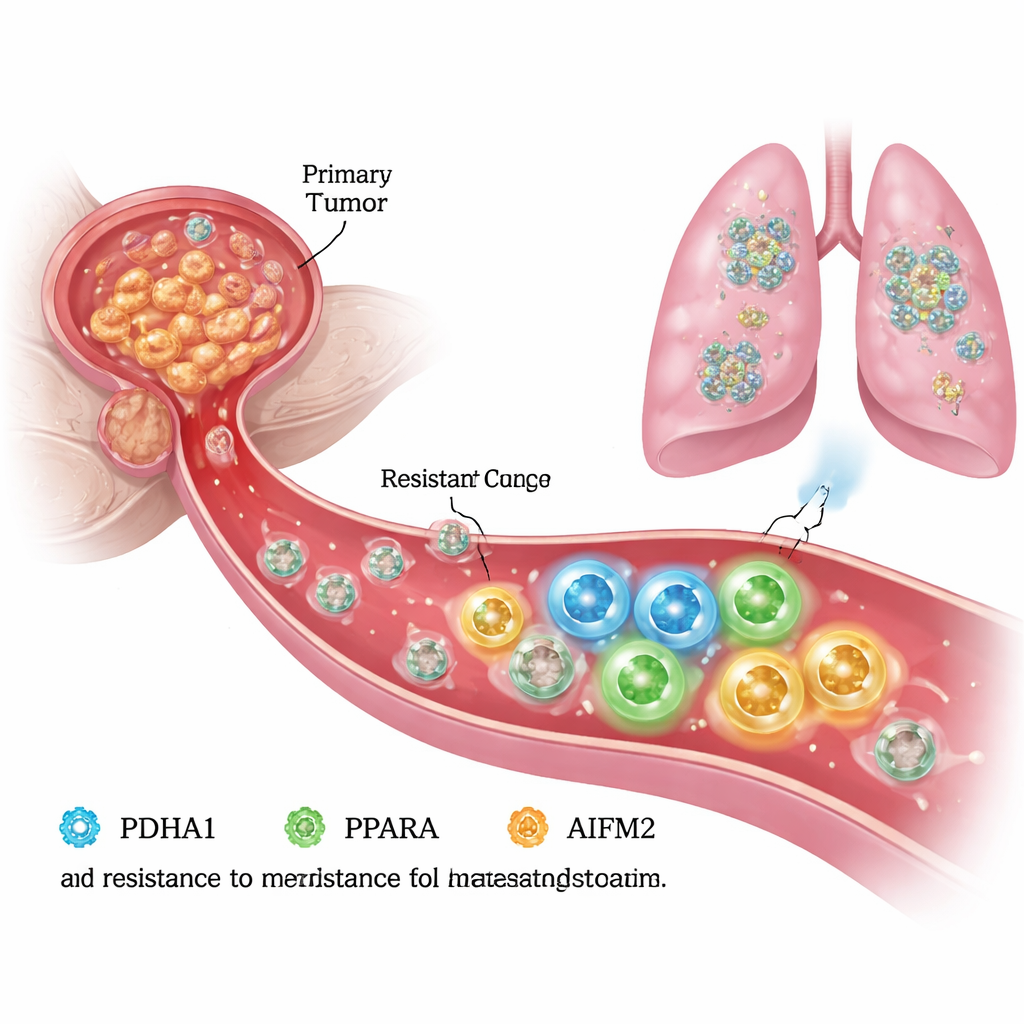
נמלטים מהמוות בזרם הדם
להתפשטות, תאי סרטן הערמונית חייבים לשרוד חיים ללא התמיכה של הרקמה הסובבת, המכונה המטריצה החוץ-תאית. בתנאים אלה של "ניתוק", תאים בריאים עוברים מוות מתוכנת שנקרא אנואקיס, ותאים סרטניים רבים גם רגישים לתהליך מוות קשור ברזל שנקרא פרורפטוזיס. החוקרים יצרו במעבדה תאי סרטן ערמונית עמידים לאנואקיס והשוו ביניהם לבין התאים "ההוריים" המקוריים. הם גילו שהתאים העמידים לא רק נודדים וחודרים ביתר תוקף, אלא גם שורדים טוב יותר בעמידות לניתוק, מה שמרמז שהם חידשו את המנגנונים הפנימיים שלהם כדי להימנע מפרורפטוזיס ולהמשיך לצמוח.
מתג מטבולי עם תפקיד שני
בהעמקה, הקבוצה התמקדה באנזים מטבולי בשם PDHA1, הידוע בעיקר בסיוע להפיכת פירובט המופק מסוכרים לאצטיל-CoA במיטוכונדריה, המזין את ייצור האנרגיה. בתאים העמידים לאנואקיס רמות הפעילות של PDHA1 היו גבוהות באופן בולט, ודגימות מטופלים הראו יותר PDHA1 בגידולים ראשוניים אצל גברים שסרטן הערמונית שלהם התפשט ללימפתיות או לאתרים מרוחקים. כאשר החוקרים הפחיתו את PDHA1, התאים העמידים איבדו חלק גדול מיכולתם לנוע, לפלוש ולשרוד. להפתעתם, חלק ניכר מ‑PDHA1 בתאים אלה כבר לא היה מוגבל למיטוכונדריה; הוא הועבר לגרעין, שם ה‑DNA מוארז עם היסטונים שניתן לשנות כימית כדי להדליק או לכבות גנים.
כתיבת פעילות גנים מחדש כדי לחסום פרורפטוזיס
בתוך הגרעין, נראה ש‑PDHA1 מזין ייצור מקומי של אצטיל‑CoA, בלוק בנייה מרכזי לאצטילציה של היסטונים. החוקרים הראו ש‑PDHA1 גרעיני חיזק סימן ספציפי, אצטילציה של H3K9, באזור הבקרה של הגן PPARA. השינוי הזה פעל כמו שחרור סלילי הכרומטין, מה שהקל על הפעלת PPARA. PPARA שימש ככפתור ראשי שהגביר את הייצור של חלבון אחר, AIFM2, על ידי קשירה לפרומוטור שלו והגברת השעתוק. במקום לשנות ישירות את גן AIFM2, PDHA1 פעל דרך PPARA, והקים מסלול רב‑שלבי מהמיון המטבולי לשינוי בבקרת הגנים.
בניית מגן מפני נזק מונע‑ברזל
AIFM2 ידוע כבלם פנימי על פרורפטוזיס: הוא מסייע בהגנה על שומנים בממברנות התא מפני חמצון הרסני. בתאי סרטן הערמונית העמידים, העלאת PDHA1 הגבירה רמות AIFM2, בעוד שניפוי PDHA1 הוריד אותן. מבחנים פונקציונליים הראו שאם מפחיתים PDHA1, מאפייני הפרורפטוזיס מתגברים — יותר סוגי חמצן ריאקטיביים, יותר נזק לשומנים, ירידה בפוטנציאל ממברנת המיטוכונדריה וקשירה אופיינית של כיווץ מיטוכונדריאלי — במיוחד כאשר התאים נחשפו ל‑erastin, חומר המעודד פרורפטוזיס. ביטוי יתר של AIFM2 היפך השפעות אלה, הציל את הישרדות התאים במצלחות ושחזר גרורות ריאתיות בעכברים, גם כאשר PDHA1 היה מדוכא. ממצאים אלו אישרו ש‑AIFM2 הוא אפקטור קריטי בסמכותו של PDHA1 לעמידות בפני פרורפטוזיס.
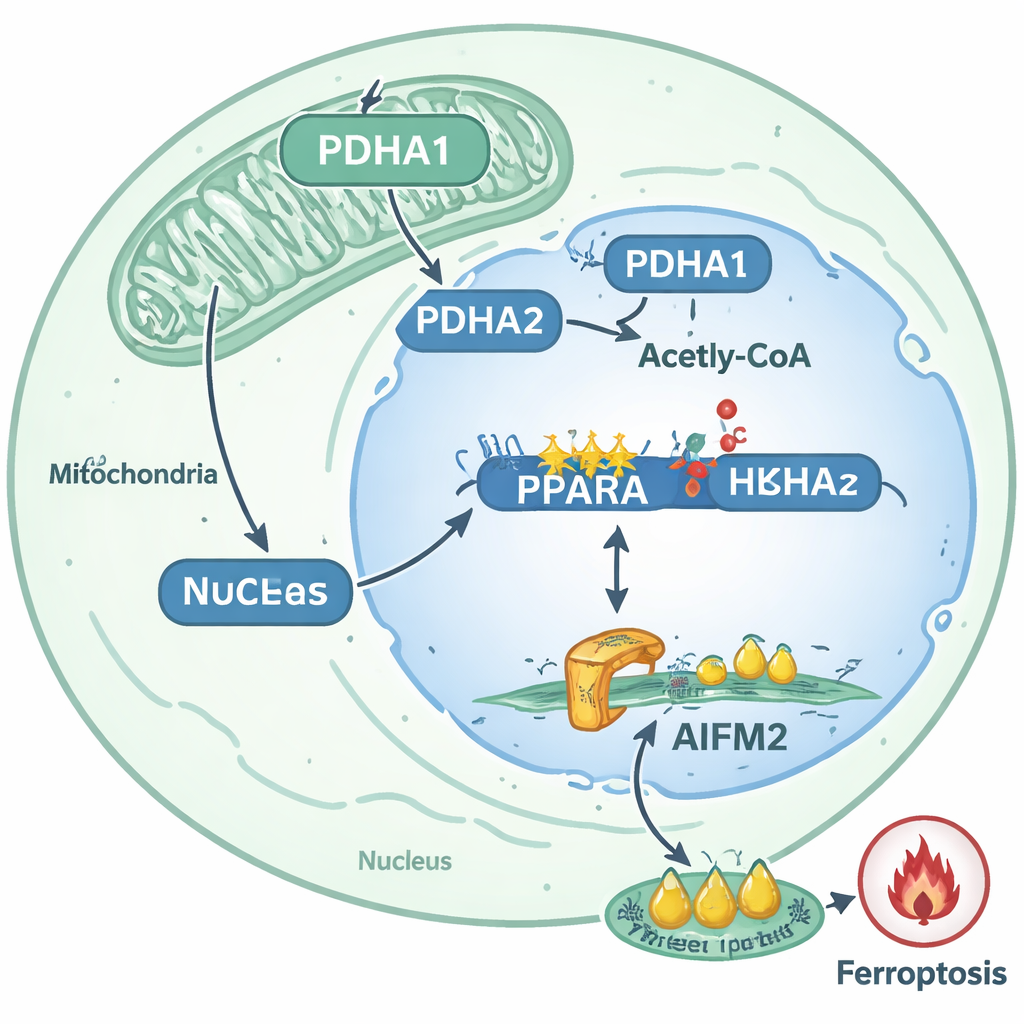
ממעגל מולקולרי לרעיונות טיפוליים
על ידי מיפוי האירועים הללו, המחקר מתאר מסלול ברור שבו תאי סרטן ערמונית מנותקים נעשים קשים יותר להשמדה: PDHA1 נודד לתוך הגרעין, מעלה אצטילציה של היסטונים באזור גן PPARA, מגדיל את פעילות PPARA, ובכך מעלה את רמות AIFM2 כדי לחסום פרורפטוזיס. מסלול זה מקושר בעוצמה להתנהגות גרורתית בגידולים של מטופלים ובמודלים חייתיים. עבור הקוראים שאינם מומחים, המסקנה היא שתאי סרטן מסוימים ממחזרים אנזים מטבולי סטנדרטי לכלי אפיגנטי שכתוב מחדש את פעילות הגנים ובונה מגן כימי‑ביולוגי נגד צורת מוות תאית עוצמתית. המחברים מציעים כי תרופות המכוונות את PDHA1, PPARA או AIFM2 — או טיפולים שמטרתם לעורר בכוונה פרורפטוזיס — עשויות יום אחד להיות משולבות כדי לשלול מתאי סרטן גרורתיים את יתרון ההישרדות הזה ולהפוך אותם לפגיעים הרבה יותר במהלך המסע הכי פגיע שלהם: הקפיצה מאיבר לאיבר.
ציטוט: Cong, Y., Chen, K., Ju, Y. et al. PDHA1 enhances resistance to ferroptosis in anoikis-resistant prostate cancer by upregulating AIFM2. Cell Death Discov. 12, 105 (2026). https://doi.org/10.1038/s41420-026-02958-7
מילות מפתח: גרורת סרטן הערמונית, פרוֹרְטוֹפְּטוֹזִיס, עמידות לאנואקיס, PDHA1, AIFM2