Clear Sky Science · he
שינוי חתימות מטבוליות כדי להפחית עמידות לקבוזנטיניב במודלים תאיים של לוקמיה מיאלואידית חריפה FLT3-ITD
מדוע זה חשוב לטיפול בסרטן
מmany תרופות מודרניות נגד סרטן מעוצבות להתמקד בחלבון בודד תקול בתאי הגידול. תרופות ממוקדות אלו יכולות לגרום להפוגות דרמטיות, אך לעתים קרובות הגידולים מוצאים דרכים להסתגל ולשוב לגדול. מאמר זה בוחן כיצד סוג של סרטן הדם, לוקמיה מיאלואידית חריפה (AML), מפתח עמידות לתרופה ממוקדת אחת — קבוזנטיניב — ואיך כיוונון מחדש של צריכת האנרגיה של תאי הסרטן עשוי לעזור לרופאים לעקוף עמידות זו.
תאי לוקמיה שלומדים להימנע מתרופה ממוקדת
החוקרים התמקדו בתאי AML שנושאים מוטציה במתג אותות הגדילה FLT3-ITD, הידוע כמניע מחלה אגרסיבית במיוחד. קבוזנטיניב, כדור שכבר משמש לטיפול בכמה גידולים מוצקים, יכול לחסום בחוזקה תאים של לוקמיה מונעת על‑ידי FLT3 במעבדה. כדי לדמות מה שקורה בחולים לאורך זמן, הצוות חשף בהדרגה שתי שורות תאי AML עם מוטציית FLT3 למנות גדלות של קבוזנטיניב עד שחלק מהתאים שרדו והתחילו לגדול שוב. אוכלוסיות תאים חדשות אלו, שנקראו Molm13‑XR ו‑MV4‑11‑XR, יכלו לשאת ריכוזי קבוזנטיניב גבוהים פעמים רבות יותר מאלו של תאי "האימא" המקוריים. הן גם הפכו לפחות רגישות לשתי תרופות מאושרות נוספות המכוונות ל‑FLT3, סוראเฟניב וקויזרטיניב, בעוד שנשארו פגיעות למעכב שונה, גילטריטיניב.
שינויים גנטיים שעוזרים לסרטן לשרוד
כשבדקו לעומק, המדענים מצאו שתאי הלוקמיה העמידים נשאו שינויים חדשים בגליון FLT3 שלהם. שתי שורות העמידות רכשו את אותה מוטציית נקודה, הנקראת D835Y, באזור קריטי בדומיין הקינאז של FLT3 — אתר חם ידוע לעמידות למספר תרופות. שורה אחת, MV4‑11‑XR, גם רכשה חסר לא שגרתי של 1.3 קילובסיסים שהסיר אקסון שלם מ‑FLT3, ומחק חלק מדומיין שחשוב לקשירת תרופות. שינויים אלה נראו כנבחרים במהלך חשיפה ארוכת טווח לקבוזנטיניב: גרסאות מוטנטיות של FLT3 הפכו לשכיחות הרבה יותר בתאים העמידים מאשר באוכלוסיית ההתחלה. במקביל, מסלולי איתות מרכזיים מתחת ל‑FLT3 — כגון ERK, STAT5 ו‑AKT — הופעלו בעוצמה רבה יותר, מה שתמך בצמיחה מהירה יותר ובהיווצרות קולוניות מוגברת בתאים העמידים.
תאי סרטן מחליפים מערכות דלק
הצוות שאל אז האם העמידות קשורה לא רק לגנטיקה אלא גם לאופן שבו התאים מממנים את עצמם. באמצעות רצפי RNA ומבחני מטבוליזם ייעודיים הם מצאו דפוס עקבי: תאים עמידים לקבוזנטיניב הסתמכו הרבה יותר על גליקוליזה — פירוק מהיר של גלוקוז בנוזל התא — גם כאשר החמצן היה זמין בשפע. תאים אלה לקחו יותר גלוקוז, ייצרו יותר לקטט, הציגו פעילות גבוהה יותר של אנזים מפתח בשם GAPDH, והגבירו את הביטוי של מספר גנים הקשורים לגליקוליזה. לעומת זאת, המיטוכונדריות של התאים — המבנים התומכים בייצור אנרגיה יעיל יותר — היו פחות פעילות ופחות שופעות. מדידות שימוש בחמצן הראו ששני נשימות המיטוכונדריה הבסיסית והשיא היו מוקטנות, ורמות המולקולות החמצוניות הפעילות בתוך התאים היו גבוהות יותר, מה שמעיד על מיטוכונדריות לחוצות ופחות מתפקדות.
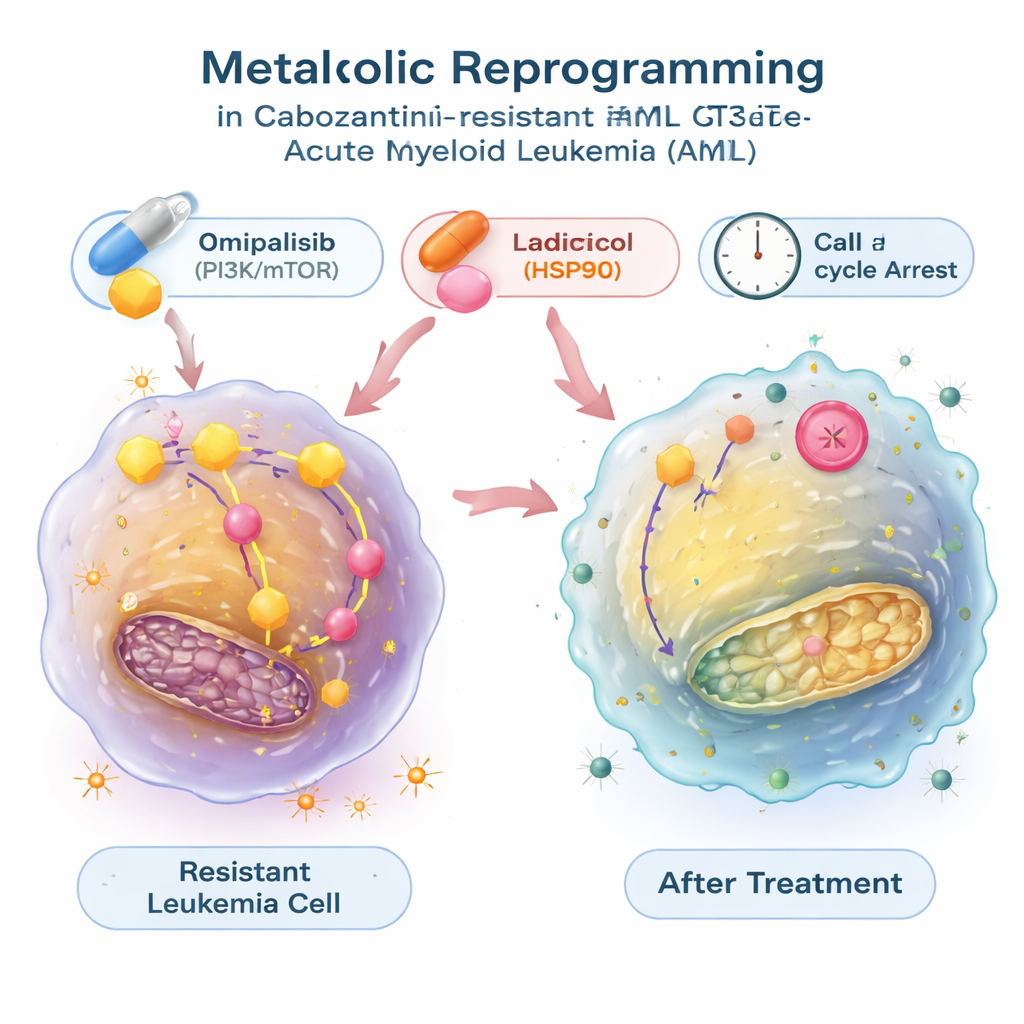
מציאת תרופות שמחזירות את מתג המטבוליזם
כדי לבדוק האם ניתן להפוך את המעבר האנרגטי הזה, החוקרים השתמשו במאגר ציבורי רחב שמקשר דפוסי ביטוי גנים עם השפעות של אלפי תרכובות. הם חיפשו תרופות שניבאו לנטרל את חתימת המטבוליזם של תאי הלוקמיה העמידים והתמקדו בשתיים: רדיקיקול, שחוסם חלבון צ'פרון הנקרא HSP90, ואומיפליסיב, שמעכב את מסלול האיתות PI3K/mTOR השולט בצמיחה ובמטבוליזם. במבחני מעבדה, שני המולקולות הללו לא רק האטו את צמיחת התאים העמידים אלא גם הקטינו את הגליקוליזה המופרזת שלהם, תוך החזרת ספיגת הגלוקוז ושחרור הלקטט לרמות נורמליות והורדת ביטוי גנים הקשורים לגליקוליזה. תרכובות אלה דחפו את תאי הלוקמיה לשלב מנוחה במחזור התא, ובמקרה של רדיקיקול גם גרמו למוות תאי מתוכנת משמעותי. בשילוב עם קבוזנטיניב, אומיפליסיב — ובמודל אחד גם רדיקיקול — פעלו בסינרגיה, והפכו את התאים העמידים לקלים יותר להשמדה.
מה משמעות הדבר לטיפולים עתידיים בלוקמיה
ללא‑מומחים, המסר הוא שתאי לוקמיה יכולים להימלט מתרופה ממוקדת לא רק על‑ידי מוטציה במטרה הישירה שלה אלא גם על‑ידי שינוי הדרך שבה הם מייצרים ומשתמשים באנרגיה. המחקר מראה שתאי AML העמידים לקבוזנטיניב מאמצים אסטרטגיית "שריפת סוכר" תוך הזנחת המיטוכונדריות שלהם. על‑ידי פגיעה במסלולים התומכים במטבוליזם המחודש הזה — באמצעות תרופות כמו אומיפליסיב או מעכבי HSP90 — ייתכן שניתן לשחזר רגישות לקבוזנטיניב ולתרופות דומות. אף על פי שממצאים אלה מקורם במודלים תאיים ולא בחולים, הם מצביעים על כך ששילוב בין תרופות ממוקדות לבין סוכנים המווסתים מטבוליזם עשוי להיות גישה מבטיחה לעיכוב או להתגברות על עמידות ב‑AML מוטנטי FLT3.
ציטוט: Fu, YH., Ng, K.M., Tseng, CY. et al. Modulating metabolic signatures to mitigate cabozantinib resistance in FLT3-ITD acute myeloid leukemia cell models. Cell Death Discov. 12, 98 (2026). https://doi.org/10.1038/s41420-026-02957-8
מילות מפתח: לוקמיה מיאלואידית חריפה, עמידות לתרופות, מוטציה ב‑FLT3, מטבוליזם של סרטן, קבוזנטיניב