Clear Sky Science · he
ליפוקלין‑2 אוסטאוציטרי מווסת היווצרות עצם באופן מקומי דרך פרופרוזה תלויה ברזל ודיכוי Wnt
כאשר תאי עצם מעצבים בשקט את בריאות הגוף כולו
רבים מאיתנו רואים בעצמות שלד נוקשה, אך הן חיות עם תאים שמתמידים בבניה ותיקון של השלד. המחקר הזה חושף כיצד חלבון קטן אחד שמיוצר בתאי עצם, ליפוקלין‑2, יכול להחליש עצמות בשקט מבפנים על ידי הפרעה לאופן שבו התאים מנהלים ברזל ואנרגיה. הבנת התהליך המוסתר הזה עשויה להוביל לטיפולים חדשים לאוסטאופורוזיס ולאובדן עצם הקשור להזדקנות.
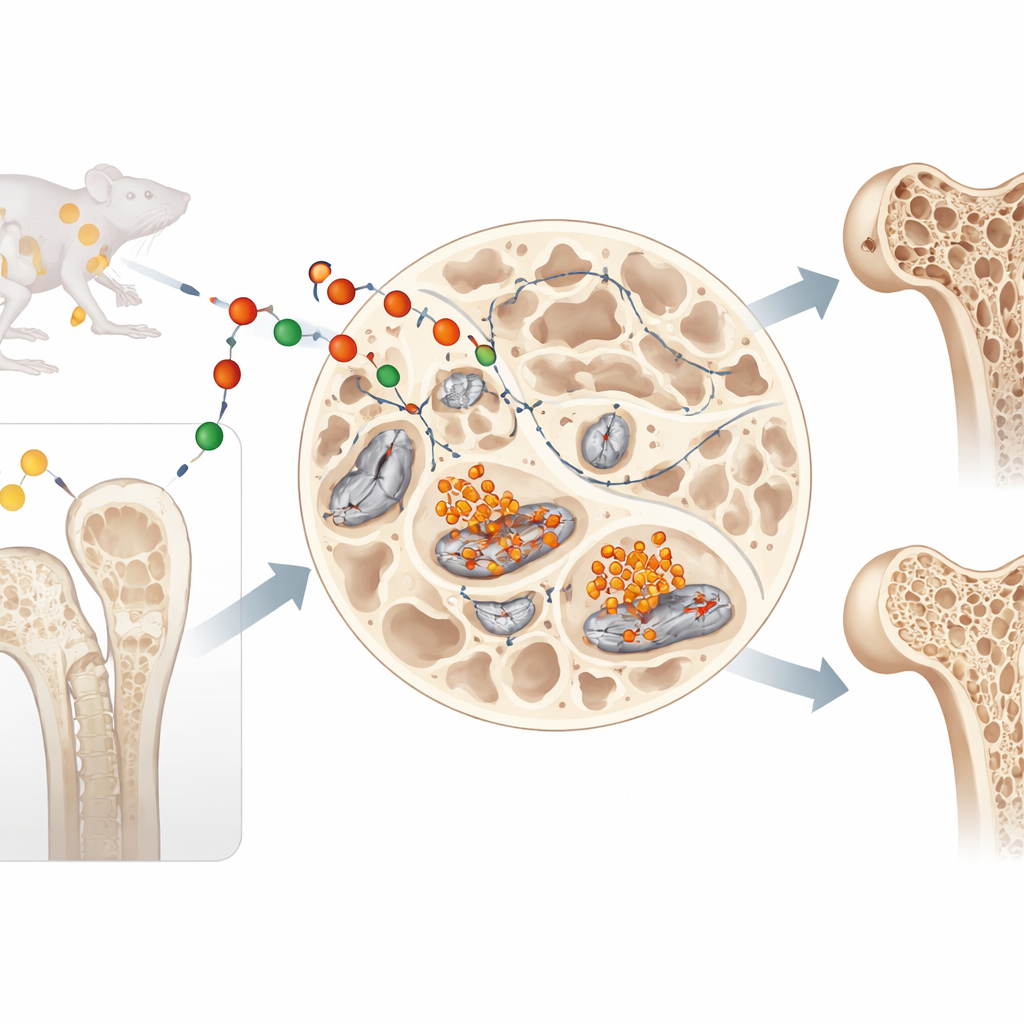
חלבון שליח עם חיים כפולים
ליפוקלין‑2 ידוע כהורמון נודד שנע בדם, מסייע בוויסות התיאבון ומשקל הגוף ומגן מפני זיהום על ידי קשירת ברזל. אך המחברים בחנו שאלה שונה: מה עושה ליפוקלין‑2 במקום בו הוא מיוצר, בתוך העצם עצמה? הם התרכזו באוסטאוציטים, התאים ארוכי־החיים הטמונים בתוך העצם החשים כוחות מכניים ומכוונים את שינוע העצם. הצוות מצא שאוסטאוציטים לא רק ממשיכים לייצר ליפוקלין‑2 ככל שהם בשלים, אלא אף מעלים את הייצור שלו, מה שמרמז על תפקיד מקומי משמעותי בתוך השלד.
עומס ברזל ומוות תאי דמוי חלודה
מכיוון שליפוקלין‑2 יכול לשנע ברזל, החוקרים בדקו האם הוא גורם להצטברות ברזל באוסטאוציטים. בתרבית תאי עצם, הוספת ליפוקלין‑2 גרמה להצטברות ברזל בתוך התאים, להגברת מולקולות חמצון מזיקות ולנזק כבד לממברנות עשירות בשומנים. אלה סימני ההיכר של צורת מוות תאי שזוהתה לאחרונה הנקראת פרורפטוזה, שבה הברזל פועל בדומה לחלודה ומצית תגובות כימיות הרסניות. חסימת הברזל בעזרת קומפלקס כילי מנעה לחלוטין את הנזק ואת המוות התאי, ואישרה שהתהליך תלוי ברזל.
קולטן השער והנזק המיטוכונדריאלי
כדי להבין כיצד ליפוקלין‑2 מספק את מטענת הברזל לאוסטאוציטים, הצוות פנה לקולטן ספציפי על פני התא, SLC22A17. כשצמצמו את הביטוי של קולטן זה בתאים הדומים לאוסטאוציטים, ליפוקלין‑2 כבר לא איפשר כניסת ברזל, לחץ חמצוני או מוות פרורפטוטי, גם בתנאי עומס ברזל. המחקר גם הראה שליפוקלין‑2 מחליש את תחנות הכוח של התא: המיטוכונדריה. עודף ליפוקלין‑2 גרם לדליפת פוטנציאל ממברנת המיטוכונדריה ולהפחתת ייצור האנרגיה, בעוד שהסרת ליפוקלין‑2 השיבה את תפקוד המיטוכונדריה. בעצמות עכברים החסרות ליפוקלין‑2 באוסטאוציטים, גנים התומכים בנשימה מיטוכונדריאלית ובבקרת האיכות הופעלו, מרמזים שהתאים היו עמידים אנרגטית יותר.
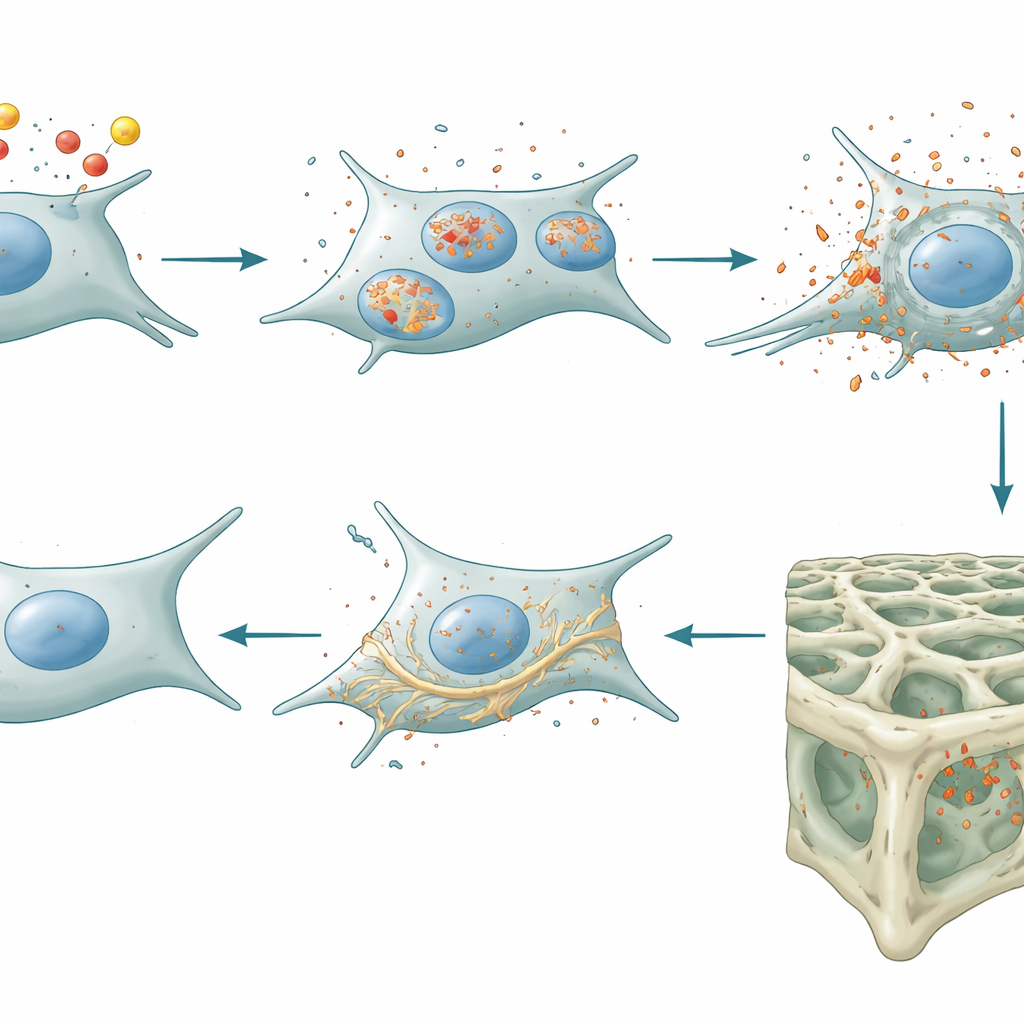
מלחץ תאי לעצם חלשה יותר, וכיצד הסרת הבלם עוזרת
החוקרים בדקו לאחר מכן עכברים חיים מהונדסים שבהם ליפוקלין‑2 הוסר ספציפית בתאי השלד בשלב מאוחר ובאוסטאוציטים. בעלי החיים האלה הצטברו פחות ברזל בתוך תאי העצם והפגינו הגנות אנטי‑חמצוניות חזקות יותר שמנוגדות לפרורפטוזה. חשוב מכך, הם ייצרו פחות משני חלבונים מרכזיים—סקלרוסטין ו‑DKK1—שבעבר שימשו כבלמים על מסלול ה‑Wnt/β‑קטנין, מנוע עיקרי של היווצרות עצם. כשהבלמים האלו נחלשו, האותות המעודדים אוסטאובלאסטים בוני עצם עלו. סריקות מיקרו‑CT וניסויים עם סימון עצם אישרו את התוצאה: עכברים ללא ליפוקלין‑2 אוסטאוציטרי בנו יותר עצם ספוגית (טרבקולארית) וחיבורים טובים יותר, בעיקר על ידי הגברת היווצרות העצם ולא על ידי האטת פירוקה. למרות השינויים בשלד, משקל גופם, בקרת הסוכר בדם, המטבוליזם ורמות הפעילות נשארו תקינים, מה שמראה שההשפעה מקומית לעצם ולא אפקט הורמונלי כללי.
מה המשמעות לשמירה על עצמות חזקות
באופן תמציתי, עבודה זו מראה שליפוקלין‑2 בתוך תאי העצם פועל כמו מתג מקומי שמעלה את רמות הברזל, מעביר עומס על המיטוכונדריה, מפעיל פוטנציאל לנזק פרורפטוטי ומדכא מסלול גדילה מרכזי — יחד מגבילים יצירת עצם חדשה. כאשר הבלם הפנימי הזה מוסר, האוסטאוציטים נשארים בריאים יותר, משדרים יותר אותות בוני עצם והעצם הטרבקולארית נעשית צפופה ומחוברת יותר מבלי להפריע למטבוליזם הכללי. מכיוון שרמות ליפוקלין‑2 וחוסר האיזון של ברזל עולים עם ההזדקנות ודלקות כרוניות, מיקוד במערכת הליפוקלין‑2‑קולטן עשוי להציע דרך חדשה להגן על העצמות מפני "החלדה" מבפנים החוצה.
ציטוט: Khanal, V., Carroll, M., Moradi, F. et al. Osteocytic Lipocalin-2 regulates bone formation locally through iron-dependent ferroptosis and Wnt suppression. Cell Death Discov. 12, 113 (2026). https://doi.org/10.1038/s41420-026-02956-9
מילות מפתח: בריאות העצם, אוסטאוציטים, חילוף חומרים של ברזל, פרורפטוזה, אותות Wnt