Clear Sky Science · he
אוסטאופונטין שמקורו בסרטן המעי הגס משנה מאקרופאגים למצב M2 פרו-מטסטטי דרך ציר PI3K/AKT/CSF1-CSF1R
מדוע זה חשוב לאנשים עם סרטן המעי
מרבית המקרים של מוות מסרטן המעי הגס (כולל המעי והחלחולת) נגרמים לא על ידי הגידול המקורי אלא על ידי הפיזור שלו לאיברים אחרים. מחקר זה בוחן כיצד תאי הסרטן "מדברים" עם תאי חיסון סמוכים כדי לסייע להתפשטות הגידול. על ידי חשיפת אות מרכזי שתאי הסרטן משדרים כדי לתכנת מחדש תאי חיסון ממלחם לעוזר, העבודה מצביעה על אסטרטגיות טיפול חדשות שייתכן ויכולות להאט או לעצור מטסטזות בסרטן המעי המתקדם.
חלבון דביק עם צד אפל
החוקרים התמקדו בחלבון בשם אוסטאופונטין, או OPN, המיוצר הן על ידי תאי הסרטן והן על ידי סוגים מסוימים של תאי חיסון בתוך הגידול. OPN נקשר זמן רב לתוצאות גרועות במגוון סרטן, אך לא היה ברור בדיוק כיצד הוא מקדם פיזור בסרטן המעי הגס. בניתוח מאגרי מטופלים גדולים ודגימות גידול, הצוות מצא שרמות OPN גבוהות יותר ברקמת סרטן המעי בהשוואה לרקמה תקינה, במיוחד בחולים עם מחלה מתקדמת ומטסטזות מרוחקות. חולים שלגידוליהם היו רמות OPN גבוהות בדרך כלל חוו הישרדות נמוכה יותר, מה שמעיד כי OPN קשור בסרטן אגרסיבי וקשה לטיפול.
זה לא רק תאי הסרטן עצמם
להפתעתם, כאשר המדענים אילצו תאי סרטן מעי במעבדה לייצר יותר או פחות OPN, התאים עצמם לא הפכו ליותר פולשניים או ניידים באופן משמעותי. הגידול, ההיגררות והיכולת להתנחל דרך ממברים מלאכותיים השתנו מעט מאוד. מציאות זו אתגרה את הרעיון המקובל ש-OPN פועל בעיקר על ידי חיזוק ישיר של יכולות תאי הסרטן. במקום זאת, הצוות בחן את השכונה של הגידול — הסביבה המיקרוסקופית שלו — במיוחד קבוצה של תאי חיסון הנקראים מאקרופאגים, שיכולים לתקוף גידולים (מצב "M1") או לתמוך בהם (מצב "M2").
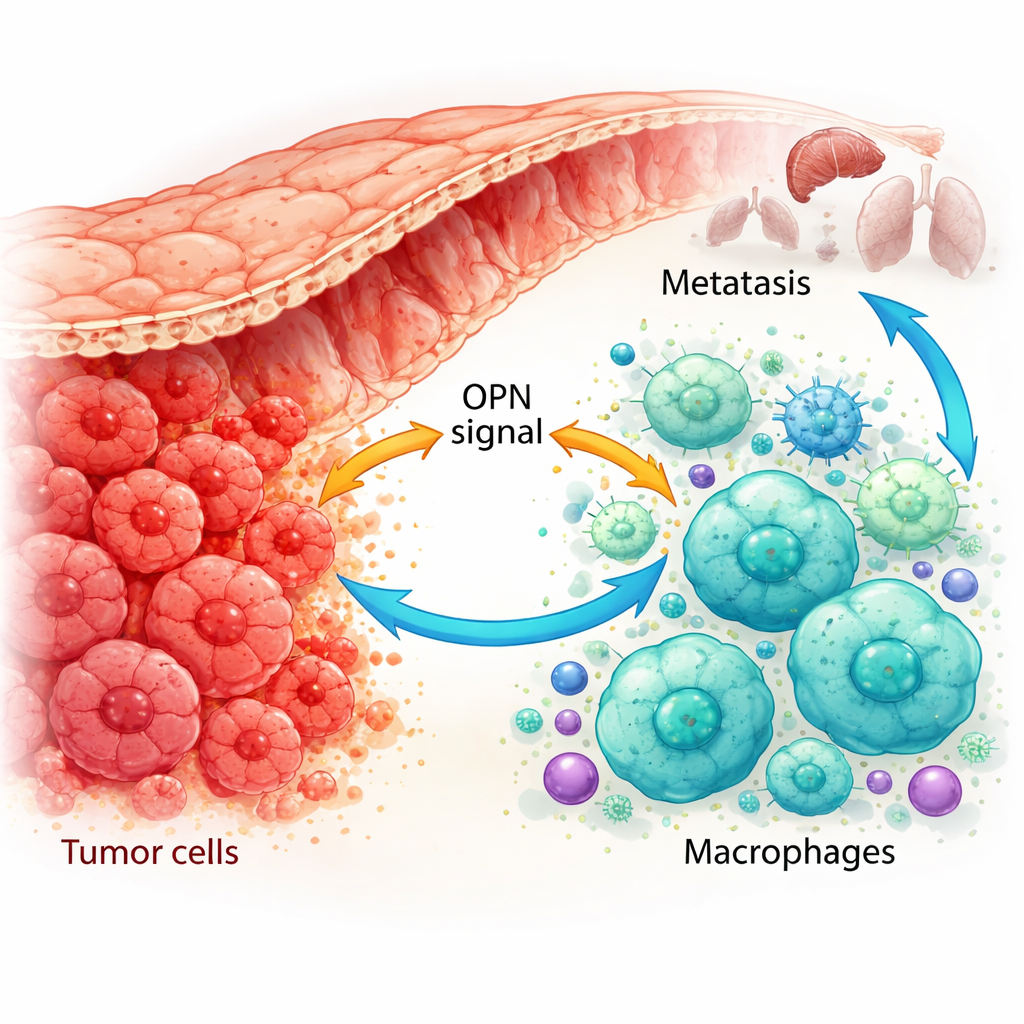
כיצד תאי החיסון מתוכנתים להיות עוזרים של הגידול
באמצעות מיפוי גנטי בודד-תאיים וצביעה מתקדמת של רקמות חולים, הראו החוקרים כי OPN מיוצר לא רק על ידי תאי סרטן אלא גם על ידי מאקרופאגים המקושרים לגידול. בגידולים שכבר התפשטו, גם תאי הסרטן וגם תת-סוג מסוים של מאקרופאגים היו עשירים ב-OPN. מאקרופאגים אלו נטו להיות במצב דמוי M2, התומך בגידול, והיו שכיחים יותר כאשר רמות OPN בגידול היו גבוהות. במודלים של עכבר, גידולים שמונו לייצר יותר OPN משכו אליהם יותר מאקרופאגים דמויי M2 וגדלו מהר יותר, בעוד גידולים עם OPN מופחת הכילו פחות מאקרופאגים אלו וגדלו לאט יותר. ממצאים אלה מצביעים על כך ש-OPN הוא מגייס ותכנתן עוצמתי של מאקרופאגים בסביבת הגידול.
שרשרת האיתות החבויה: מ-OPN אל המטסטזה
כדי לפענח את שרשרת האירועים המולקולרית, גדלו החוקרים מאקרופאגים אנושיים יחד עם תאי סרטן של המעי המייצרים כמויות שונות של OPN. הם מצאו שתאי סרטן עם רמות OPN גבוהות דחפו את המאקרופאגים לכיוון מצב M2 ועודדו תנועה דו-כיוונית: מאקרופאגים נדדו לכיוון הגידול, ותאי הגידול הפכו לפולשניים יותר בתגובה לאותות מהמאקרופאגים. בחקירה מעמיקה יותר גילו המדענים ש-OPN מפעיל תוואי איתות בתוך המאקרופאגים בשם PI3K/AKT. הפעלת תוואי זה גורמת למאקרופאגים לשחרר כמויות גדולות של מולקולה נוספת, CSF1, ולהגביר את הביטוי של הקולטן המתאים לה, CSF1R, על פני השטח שלהם. CSF1 פועל בלולאה שמחזקת עוד יותר את המצב ה-M2 הפרו-מטסטטי וממשיכה למשוך מאקרופאגים אל תוך הגידול.
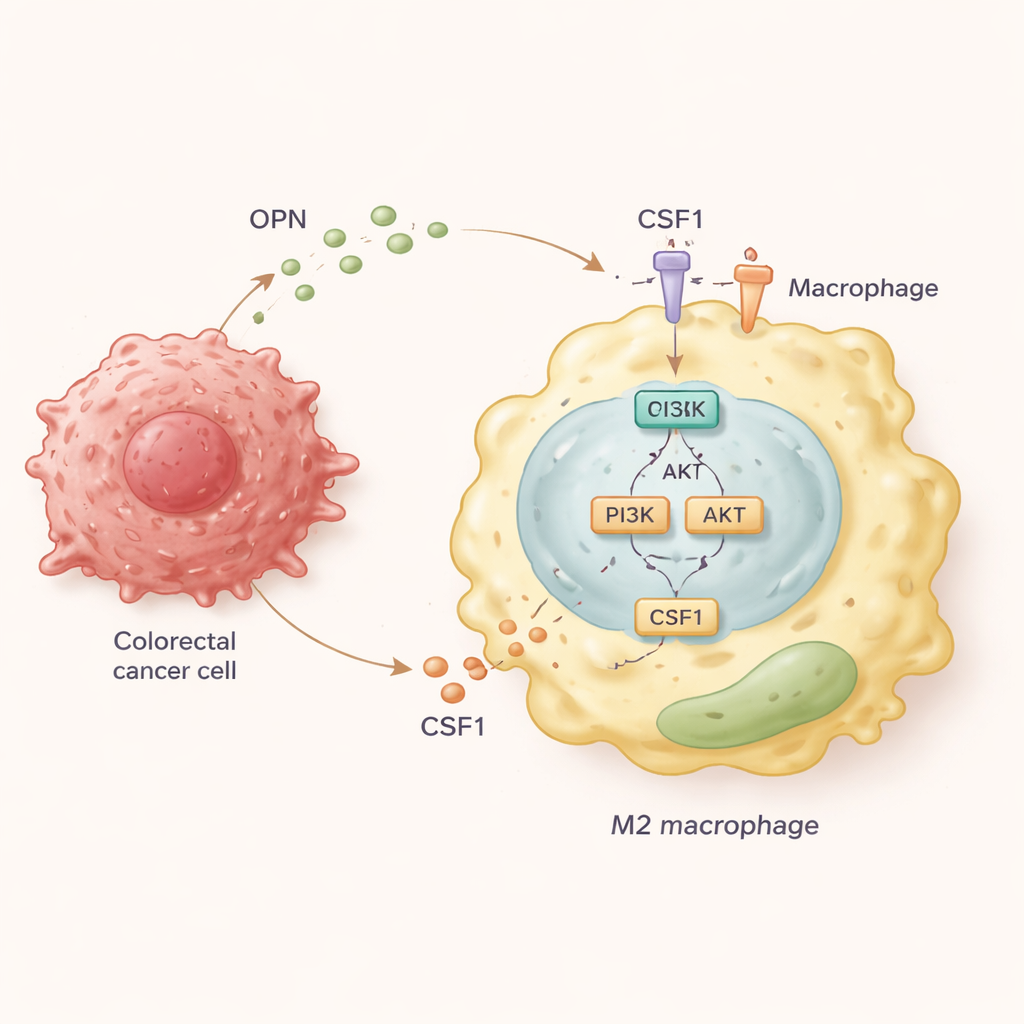
חסימת הלולאה כדי להאט את הפיזור
במודלים של עכבר לסרטן המעי שהתפשט בתוך הבטן, ניסו החוקרים תרופה החוסמת את CSF1R בשם PLX3397. בעכברים עם גידולים עשירים ב-OPN התפתחו נודולים מטסטטיים רבים, אך טיפול בחוסם CSF1R הקטין משמעותית הן את מספר המטסטזות והן את נוכחות המאקרופאגים דמויי M2 בגידולים. תאי הגידול הציגו צמיחה פחותה וסימנים מוגברים לתלוי תכנותי של מוות (אפופטוזיס). חשוב לציין כי התרופה פגעה בעיקר במאקרופאגים התומכים בגידול מבלי לשבש באופן ניכר את סוג המאקרופאגים הדלקתי יותר, מה שמרמז על דרך יחסית ממוקדת להחליש את מערכת התמיכה של הגידול.
מה המשמעות לטיפולים עתידיים
לקריאה לא מקצועית, המסר העיקרי הוא שחלק מהסרטןי המעי מצליחים להתפשט לא רק כי תאי הסרטן אגרסיביים, אלא כי הם חוטפים תאי חיסון סמוכים והופכים אותם לשותפים למעשה. במחקר זה, ה-OPN שמקורו בתאי הסרטן מתפקד כמתג ראשי שמחדש את תכנות המאקרופאגים דרך ציר האיתות PI3K/AKT ו-CSF1/CSF1R, ויוצר קרקע פורייה למטסטזות. על ידי שבירת השרשרת—ובפרט בחסימת שלב ה-CSF1R—החוקרים הצליחו להפחית את פיזור הגידול בעכברים. ממצאים אלה מציעים כי מדידת רמות OPN עשויה לסייע בזיהוי חולים שעשויים להרוויח מתרופות שמטרתן מאקרופאגים, וכי שילוב של תרופות אלה עם טיפולים קיימים או אימונותרפיות עשוי להציע תקווה חדשה לאנשים עם סרטן המעי המתקדם.
ציטוט: Liang, X., Qin, F., Yuan, Z. et al. Colorectal cancer-derived osteopontin rewires macrophages into a pro-metastatic M2 state via the PI3K/AKT/CSF1-CSF1R axis. Cell Death Discov. 12, 92 (2026). https://doi.org/10.1038/s41420-026-02945-y
מילות מפתח: סרטן המעי הגס, אוסטאופונטין, מאקרופאגים המקושרים לגידול, מטסטזה, עיכוב CSF1R