Clear Sky Science · he
מיקוד אותות NXPH4/ALDH1L2 מדכא עמידות לאנזלוטמיד בסרטן הערמונית
מדוע זה חשוב לחולים עם סרטן הערמונית
רבים מהגברים עם סרטן ערמונית מתקדם מסתמכים על תרופה חזקה שמשביתה הורמונים, אנזלוטמיד. בתחילה היא לעתים קרובות יעילה — מצמצמת גידולים ומאטה את ההתקדמות של המחלה. אך ברוב המטופלים, בסוף הסרטן מוצא דרך לעקוף את התרופה ומתחיל לצמוח שוב. המחקר הזה חוקר כיצד מתרחש הבריחה הזו ומצביע על נקודת פגיעה חדשה בגידולים עמידים — מה שעשוי להציע דרך להאריך ולהעצים את ההשפעה של טיפולים קיימים.
טיפול שכיח נגד מחלה עיקשת
צמיחת סרטן הערמונית קשורה בקשר הדוק להורמונים גבריים, האנדורוגנים, שפועלים דרך חלבון שנקרא קולטן לאנדרוגן. אנזלוטמיד מתוכנן לשתק את הקולטן הזה והוא טיפול סטנדרטי כשהגידולים מפסיקים להגיב לטיפולים מקובלים להורדת הורמונים. לצערנו, גידולים רבים מסתגלים והופכים למה שרופאים קוראים לו סרטן ערמונית עמיד להסרה הורמונלית. מחברי המאמר הזה ניסו לזהות אילו גנים מסייעים לתאי הסרטן לשרוד אנזלוטמיד, בתקווה שהחסימה של מסייעים אלה תחזיר את יעילות התרופה.
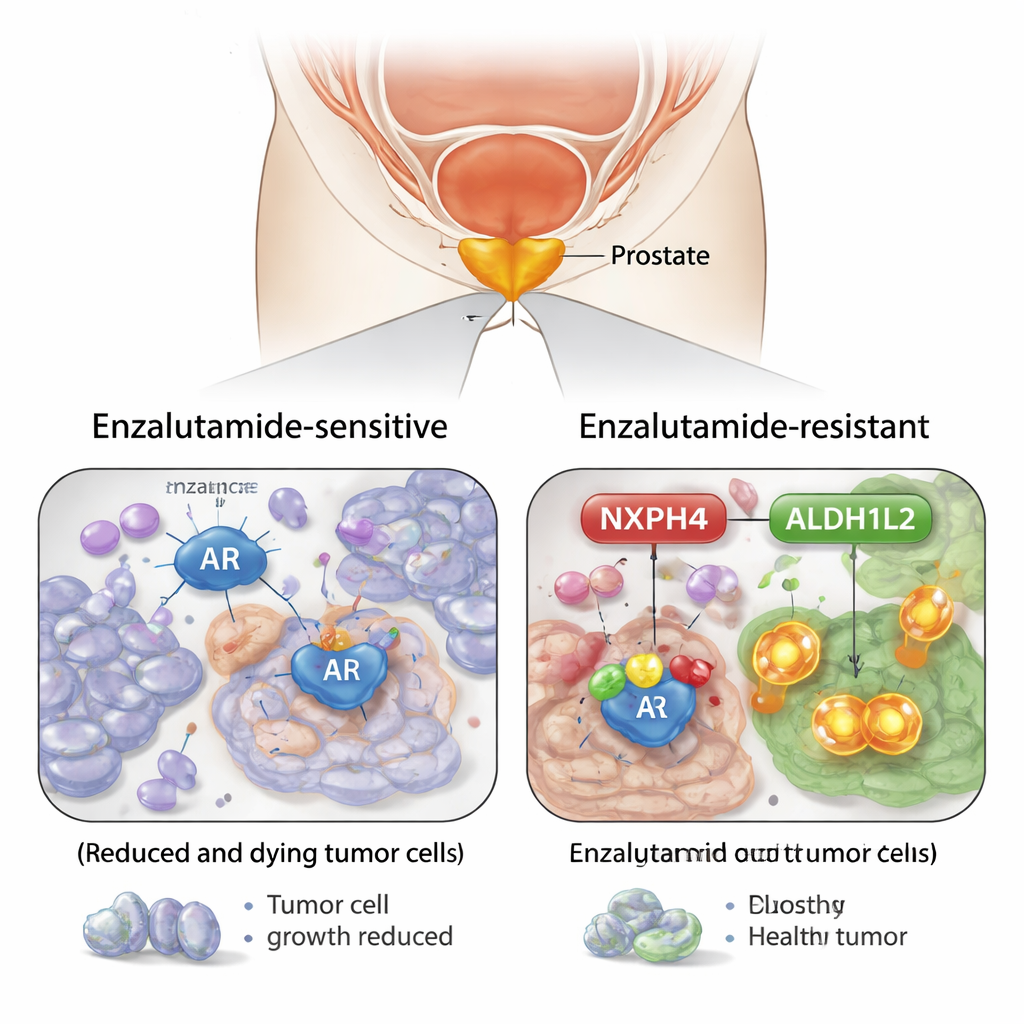
הארת מולקולה מסייעת מפתיעה
בהשוואה בין תאי סרטן ערמונית שהיו רגישים לאנזלוטמיד לתאים שפיתחו עמידות, הצוות זיהה חלבון בשם NXPH4 כשחקן מרכזי. תאים עמידים ייצרו הרבה יותר NXPH4, ורמותיו עלו בהדרגה כשהתאים נחשפו לאנזלוטמיד במשך הזמן. דגימות רקמה ממטופלים הראו את אותה תמונה: רמות גבוהות יותר של NXPH4 בגידולים אגרסיביים יותר ובסרטן שלא הגיב עוד לתרופה. כשהחוקרים הפחיתו את רמות NXPH4 בתאים עמידים, התאים הפכו לקלים יותר להשמדה על ידי אנזלוטמיד והפרישו פחות מושבות, הן במשטחי תרבית והן בעכברים. לעומת זאת, אילוץ הביטוי של NXPH4 בתאים הפך אותם לקשים יותר לטיפול.
כיצד ההורמונים מפעילים את NXPH4
המחקר גם בדק מדוע NXPH4 ככל כך שופע בגידולים אלה. התשובה שוב הובילה אל קולטן האנדורוגן. החוקרים הראו שכאשר תאים טופלו בהורמון דיהידרו-טסטוסטרון, רמות NXPH4 עלו. כאשר הוסיפו עוד קולטן אנדרוגן, NXPH4 עלה; וכאשר חסמו את הקולטן, NXPH4 ירד. ניסויי DNA מפורטים איששו כי קולטן האנדורוגן נקשר פיזית לאזור הבקרה של גן NXPH4 ומפעיל אותו. משמעות הדבר היא שמערכת מונעת-הורמונים שמזינה את צמיחת סרטן הערמונית גם מכינה את התאים עם NXPH4, ובכך יוצר קרקע שמאפשרת עמידות לתרופה בהמשך.
הפעלת בתי הכוח של התא
בהעמקה נוספת, הצוות מצא ש-NXPH4 משנה את הדרך שבה תאי הסרטן מנהלים אנרגיה ומתח בתוך המיטוכונדריה שלהם, בתי הכוח הזעירים של התא. תחת תנאים של חסימת הורמונים, חלק מ-NXPH4 נע אל המיטוכונדריה וקושר חלבון נוסף, ALDH1L2, שחשוב ליצירת NADPH — מולקולה מפתח שעוזרת לשלוט בריאקטיביות של מינים חופשיים של חמצן (ROS). בתאים עמידים, NXPH4 ו-ALDH1L2 יוצרים קומפלקס שמגביה את הנשימה המיטוכונדריאלית, שומר על פוטנציאל ממברנה, מעלה NADPH ומוריד רמות ROS. שילוב זה שומר על בריאות המיטוכונדריה ומאפשר לתאי הסרטן לעמוד בפני המתחים שהאנזלוטמיד גורם, במקום למות כפי שהיו אמורים בדרך כלל.
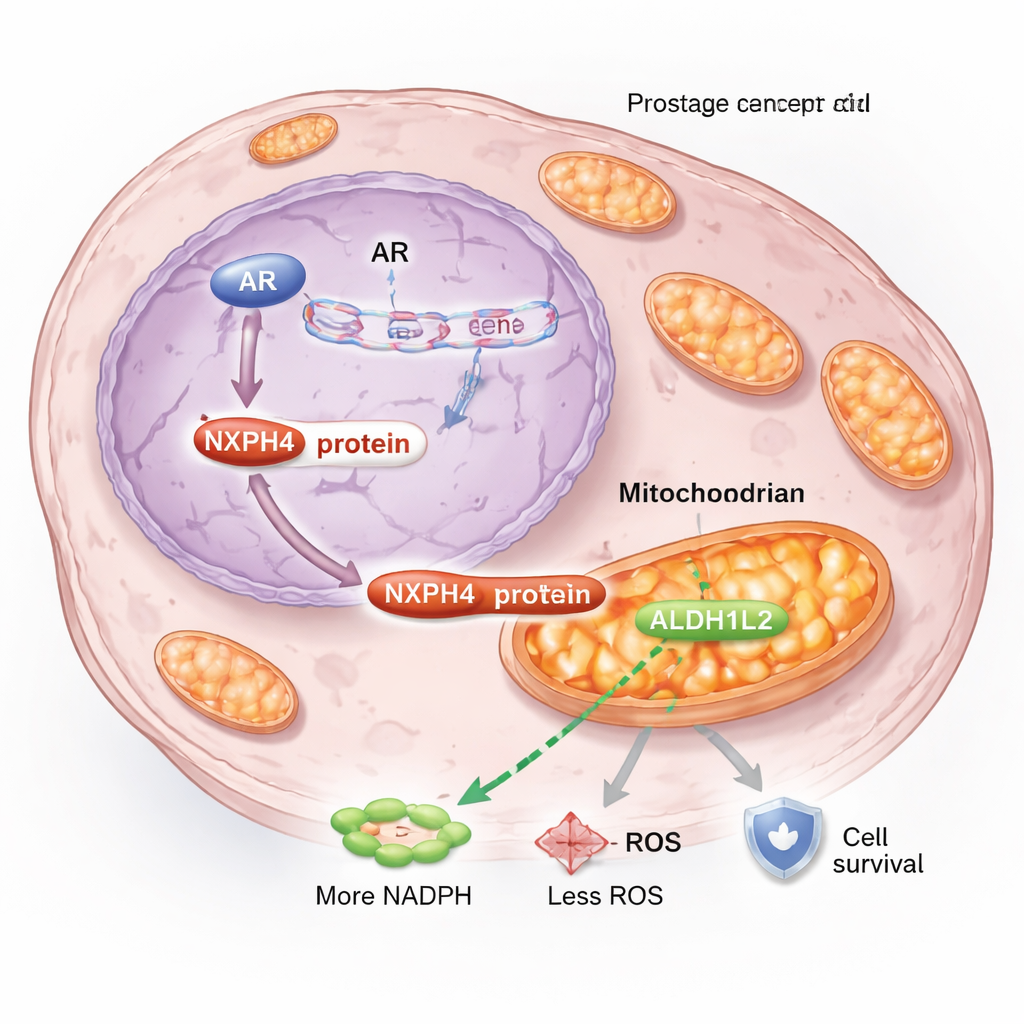
שבירת מעגל העמידות
כאשר החוקרים הפריעו למערכת התמיכה המיטוכונדריאלית הזו, התוצאות היו בולטות. השתקת NXPH4 בתאים עמידים הפחיתה פעילות מיטוכונדריאלית, העלתה מתח חמצוני, האטה את הצמיחה והפכה את התאים לפגיעים הרבה יותר לאנזלוטמיד. השתקת ALDH1L2 נתנה אפקט דומה ומחקה את יתרונות ההגנה של עודף NXPH4, מה שאישר ששני החלבונים עובדים יחד. במודלים בחולדות, גידולים חסרי NXPH4 גדלו לאט יותר, ושילוב של אובדן NXPH4 עם אנזלוטמיד כיווץ את הגידולים אף יותר מאשר כל גישה בנפרד. ממצאים אלה מצביעים על כך שהשיתוף פעולה בין NXPH4 ל-ALDH1L2 הוא לא רק תופעת לוואי של עמידות אלא כוח מניע מאחוריה.
מה זה יכול להצביע עבור טיפולים עתידיים
באופן פשוט, עבודה זו מראה שחלק מגידולי הערמונית שורדים אנזלוטמיד על ידי חיבור מחדש של אספקת האנרגיה שלהם. NXPH4, שמופעל על ידי קולטן האנדורוגן, משתף פעולה עם ALDH1L2 בתוך המיטוכונדריות כדי לשמור עליהן פעילות, להגן מפני נזק חמצוני ולעזור לתאי הגידול לעבור את הטיפול בחסימת הורמונים. מיקוד ב-NXPH4, או בממשק בינו לבין ALDH1L2, עשוי להחליש את מעגל ההישרדות הזה. אמנם תרופות הפוגעות ב-NXPH4 עדיין אינן קיימות, המחקר מדגיש את הזוג מולקולות זה כיעד חדש ומבטיח. בעתיד, שילוב אנזלוטמיד עם תרופות המפריעות לאיתות NXPH4‑ALDH1L2 עשוי לסייע למטופלים להקדים את סרטן הערמונית העמיד למשך זמן ארוך יותר.
ציטוט: Sun, X., Zhang, Y., Zhang, W. et al. Targeting NXPH4/ALDH1L2 signaling suppresses enzalutamide resistance in prostate cancer. Cell Death Discov. 12, 91 (2026). https://doi.org/10.1038/s41420-026-02944-z
מילות מפתח: סרטן הערמונית, עמידות לאנזלוטמיד, מטבוליזם מיטוכונדריאלי, NXPH4, ALDH1L2