Clear Sky Science · he
תאי גליובלסטומה הנמנעים ממות תאים המוּנעת על ידי כימורדיותרפיה מציגים תכנית גליקוליטית מפוצלת
מדוע מחקר סרטן המוח הזה חשוב
גליובלסטומה היא אחד מסוגי הסרטן הקטלניים ביותר במבוגרים, ובמרבית המקרים מתחדשת לאחר ניתוח, כימותרפיה והקרנה. המחקר שואל שאלה מרכזית: מה מיוחד בקבוצת התאים הקטנה של הגידול ששרדו את הטיפול ומאוחר יותר מחדש את המחלה? בעקיבה אחרי אופן הטיפול בסוכר של התאים לאורך זמן, החוקרים חושפים אסטרטגיית הישרדות מוסווית שיכולה להסביר מדוע הטיפולים הקיימים נכשלו כל כך לעתים קרובות — ומציעים דרכים חדשות לנתק את מקור החיים של הגידול.
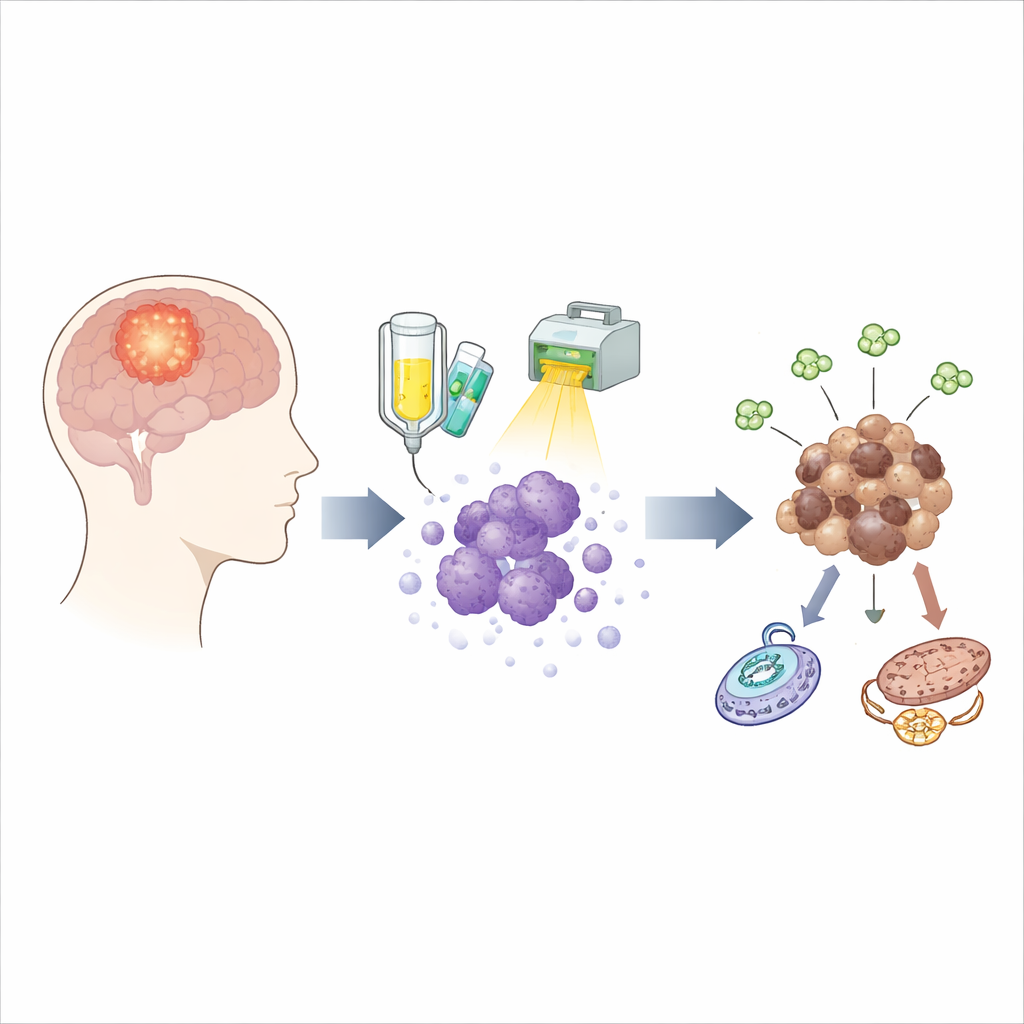
הניצולים המוסתרים לאחר הטיפול
הטיפול הסטנדרטי בגליובלסטומה משלב תרופה בשם טמוזולומיד עם הקרנות. בעוד שילוב זה הורג את מרבית תאי הגידול, מיעוט עקשן שורד ויכול לזרוע גידול חדש חודשים לאחר מכן. כדי לתפוס ניצולים אלו בפעולה, הצוות השתמש בתאי גידול שנלקחו ישירות מעשרה מטופלים שונים וחשף אותם ללוח טיפול שנועד להידמות ככל הניתן למה שמקבלים בחדר הטיפולים. הם דגמו תאים חיים בנקודות זמן שונות במהלך ואחרי הטיפול, ולמדו גם גידולים תואמים שגודלו בעכברים, מה שאפשר להם לעקוב אחר השינויים בניצולים לאורך זמן במקום רק להשוות גידולים לפני ואחרי הישנות.
כיצד תאי הגידול משנים את אופן השימוש שלהם בסוכר
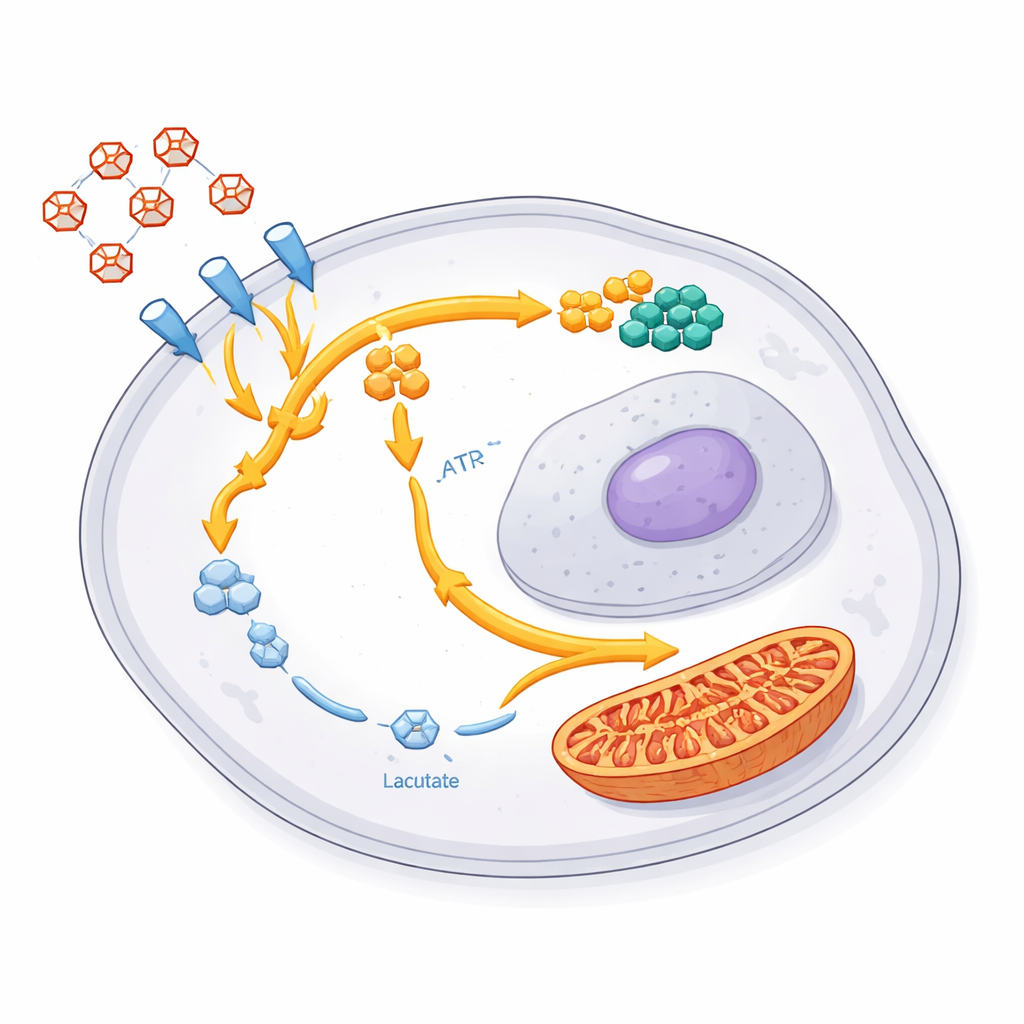
רקמת המוח צורכת חלק מרשים מסך הסוכר של הגוף, ותאי גליובלסטומה רעבים במיוחד לו. החוקרים מצאו שבמהלך ההתקדמות של הטיפול, התאים ששרדו משכו עוד יותר גלוקוז מהסביבה. ואולם, באופן מפתיע, הם לא פשוט שרפו את הדלק הנוסף בקצב מהיר יותר. במקום זאת הקטינו תוצר לוואי טיפוסי של פירוק מהיר של סוכר—חומצה לקטית. מדידות של חלבונים מרכזיים הראו דפוס מפוצל בולט: רכיבים שמכניסים סוכר לתא ומתחילים לפרק אותו עלו ברמות, בעוד אלו המטפלים בשלבים המאוחרים ויצירת הלקטט ירדו. התכנית ה"המפוצלת" הזו אומרת שהסוכר נכנס ומתחיל לעבור עיבוד, אך נתיב היציאה הרגיל ללקטט סגור חלקית.
ניתוב הדלק לבוני מבנים ולתחנות כוח
לאן הולך הסוכר המוסט? בעזרת גלוקוז מסומן ומדידות מתקדמות של מטבוליטים, הצוות הראה שהתאים ששרדו מנווטים חלק ניכר מפחמן זה לשתי יעדים עיקריים. אחד הוא נתיב צדדי שנקרא נתיב הפנטוזי־פוספט, שמייצר חומרי גלם להכנת אבני הבניין של DNA ו‑RNA. בתאים אלה רבות מרכיבי הנוקלאוטידים והגנים הקשורים הוגברו, מה שמצביע על דחיפה חזקה לשיקום ולהתכוננות לצמיחה מחודשת. היעד השני הוא תחנות הכוח של התא — המיטוכונדריה. אנזימים של מעגל האנרגיה המיטוכונדריאלי עלו, ועבודה קודמת מאותו צוות הראתה ייבוא מוגבר של דלק שמקורו בסוכר אל תוך מבנים אלו. יחד הדבר חושף רה־חיווט מתואם: פחות תסיסה בזבזנית ללקטט, יותר השקעה בתיקון, בחומרי בנייה ובייצור אנרגיה גמיש.
ספר משחק הישרדות משותף בין גידולים ובחיות
גידולי גליובלסטומה שונים במידה רבה מחולה לחולה, מה שמקשה על טיפולים אחידים. למרות המגוון הזה, כל אחד מעשרת המודלים שמקורם בחולים הראה את אותו המהלך הבסיסי לאחר כימורדיותרפיה: העלאה בשלבים המוקדמים של עיבוד הסוכר, ירידה בשלבים המאוחרים ובייצור לקטט, ועליה בפעילות המיטוכונדריאלית. באופן חשוב, אותו חתימת מטבוליזם הופיעה גם בגידולי מוח של עכברים שגודלו מתאים של מטופלים וטופלו בגרסאות מותאמות של הטיפול הסטנדרטי. גידולים חוזרים בבעלי החיים הללו נשאו עדיין את תוכנית הסוכר המותאמת, מה שמעיד שזהו לא אפקט חולף אלא תכונה יציבה של תאים שמצליחים לשרוד את הטיפול ולבנות מחדש את הסרטן.
משמעות הדבר לטיפול בעתיד
בהירות לציבור הרחב: תאי גליובלסטומה ששרדו אינם פשוט "מסתתרים" מהטיפול; הם מיישרים מחדש באופן פעיל את אופן השימוש שלהם בסוכר כדי להישאר בחיים. הם שואבים יותר גלוקוז, נמנעים מהפיכתו לפסולת, ובמקום זאת מנווטים אותו להכנת אבני DNA ולהפעלת המיטוכונדריה — מה שעוזר להם לתקן נזקים, לשמור על מצב גמיש בדומה לתאי גזע, ולבסוף לצמוח מחדש. חשיפת מצב הישרדות מטאבולי משותף זה מציעה רעיונות טיפוליים חדשים: פגיעה בשלבי עיבוד הסוכר המוקדמים, בנתיב צדדי ליצירת נוקלאוטידים, או בתלות המיטוכונדריאלית של התאים הללו עשויה להשלים את הכימורדיותרפיה הרגילה ולצמצם את מספר הניצולים שיכולים להחזיר את המחלה.
ציטוט: Martell, E., Kuzmychova, H., Chawla, U. et al. Glioblastoma cells that evade chemoradiotherapy-induced cell death exhibit a bifurcated glycolytic program. Cell Death Dis 17, 348 (2026). https://doi.org/10.1038/s41419-026-08646-9
מילות מפתח: גליובלסטומה, מטבוליזם של סרטן, שימוש בגלוקוז, עמידות לטיפול, נתיב הפנטוזי פוספט