Clear Sky Science · he
ציר HNF4α-HKDC1 מארגן שינוי מטבולי לקידום נדידה ומטסטזות בסרטן הקיבה המתקדם
מדוע זה חשוב לחולים
רוב המיתות מסרטן הקיבה אינן נובעות מהגידול הראשוני עצמו, אלא מכיוון שתאי הסרטן נודדים לאזורים מרוחקים בגוף ומקימים שם מושבות. מאמר זה חושף "מַפְעִיל" מולקולרי נסתר שמסייע לתאי סרטן הקיבה לשנות את ניצול הדלק שלהם ולהפוך לניידים יותר. עוד יותר חשוב — הוא מצביע על תרופה מאושרת על‑ידי ה‑FDA שעשויה להיות מועמדת לשימוש חוזר כדי לכבות מתג זה ולהאט או למנוע את התפשטות המחלה.
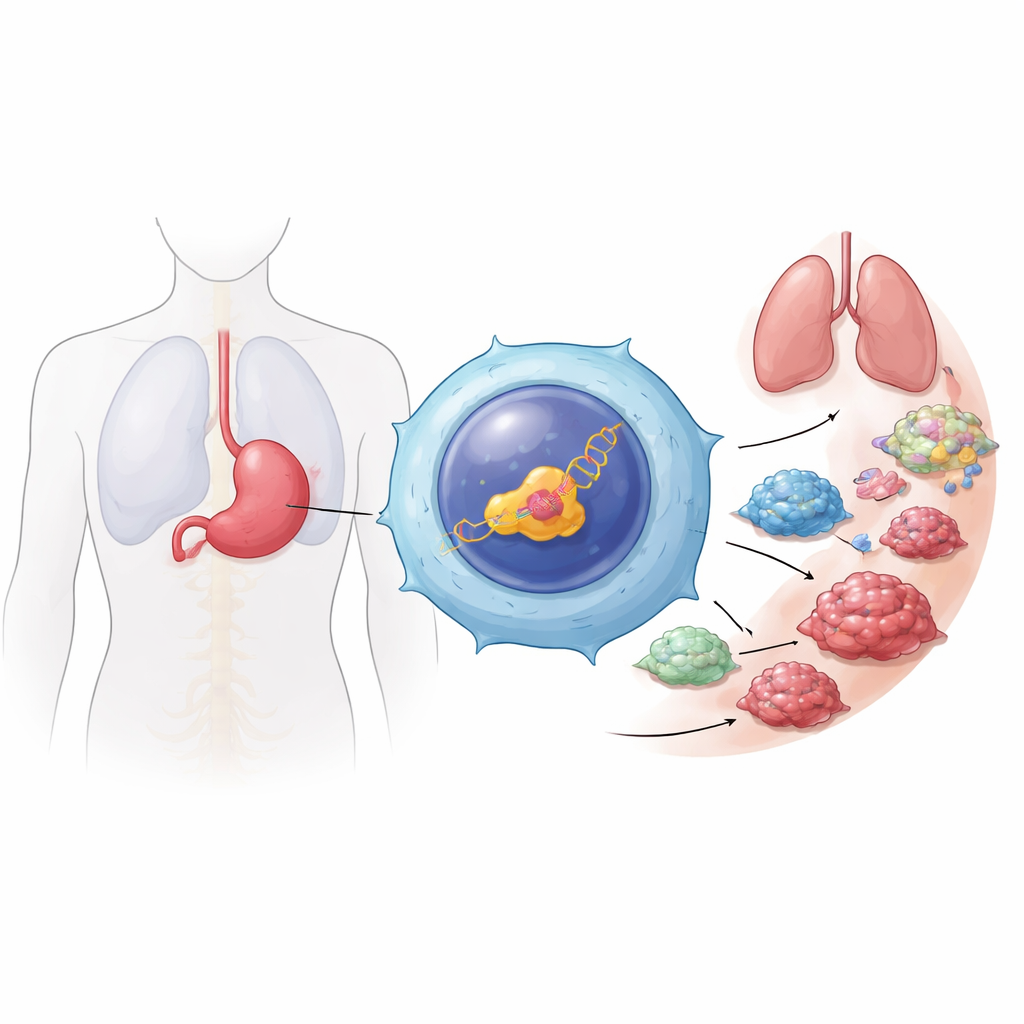
מהפך מסוכן בסרטן הקיבה
סרטן הקיבה הוא סוג הסרטן החמישי השכיח ביותר בעולם והוא מתגלה לעיתים קרובות בשלב מאוחר, לאחר שכבר התפשט. החוקרים התמקדו במטסטזות — השלב שבו תאי הגידול ניתקים, נעים דרך חלל הבטן או זרם הדם ומתיישבים באתרים חדשים. בעזרת כרייה של מאגרי נתונים ציבוריים רחבים ובחינת דגימות רקמה של חולים הם מצאו שגרסה מסוימת של בקרה גנטית בשם HNF4α, המופעלת על‑ידי מאיצה P2 (P2‑HNF4α), קיימת בשפע במיוחד במטסטזות מרוחקות ביחס לגידולים ראשוניים ולרקמות סמוכות שאינן סרטניות. גרסה זו נמצאה בעיקר בתוך תאי הגידול ולא בתאים תקינים מסביב, מה שמרמז על קשר הדוק להתנהגות הס invasive של הסרטן.
מתג מאסטר שמגביר תנועה תאית
כדי לבדוק קשר סיבתי, החוקרים שינו את רמות P2‑HNF4α בקו תאים של סרטן קיבה אנושי המייצג תתי‑סוגים מולקולריים עיקריים של המחלה. כשהקטינו את HNF4α בתאים שמבטאים אותו בדרך רגילה, התאים הפכו לפחות מסוגלים לנוע ולחדר דרך ממברנות מלאכותיות או לסגור פציעות במנות תרבית. כאשר אילצו תאים עם רמות נמוכות של HNF4α לייצר יותר מאיזופורמה מייצגת של P2‑HNF4α, אותם תאים הפכו לניידים ולחודרנים הרבה יותר, גם במבחני סֶפֶרוֹיד תלת‑ממדיים המדמים גידולים אמיתיים. בעכברים, תאים מהונדסים המייצרים P2‑HNF4α בכמויות גבוהות יצרו הרבה יותר נודולים גרורתיים בחלל הבטן, מה שמראה שפקטור זה מקדם באופן פעיל התפשטות באורגניזמים חיים.
דלק להתפשטות דרך שינוי שימוש באנרגיה
תאי סרטן לעיתים קרובות מעצבים מחדש את עיבוד החומרים המזינים שלהם כדי לתמוך בצמיחה ובתנועה. בשילוב של רצף RNA ופרופיל מטבוליטים, הצוות גילה שכיבוי HNF4α מדכא מסלול מרכזי לייצור אנרגיה: הגליקוליזה, פירוק הגלוקוז. רמות של כמה אנזימים גליקוליטיים ומוצרי ביניים שלהם ירדו, כמו גם מדדים של תפוקת אנרגיה כגון צריכת חמצן, ייצור חומציות וייצור ATP. ניתוחים נוספים בחנו אנזים אחד, HKDC1, שמראה הקשר החזק והקבוע ביותר ל‑HNF4α. HKDC1 יושב בשלב הראשון של עיבוד הגלוקוז ועוזר להפנות סוכר הן לייצור לקטט והן לנשימה המיטוכונדריאלית — שני מוצאים שמספקים יחד אנרגיה ויוצרים סביבה כימית המקדמת תנועה תאית.
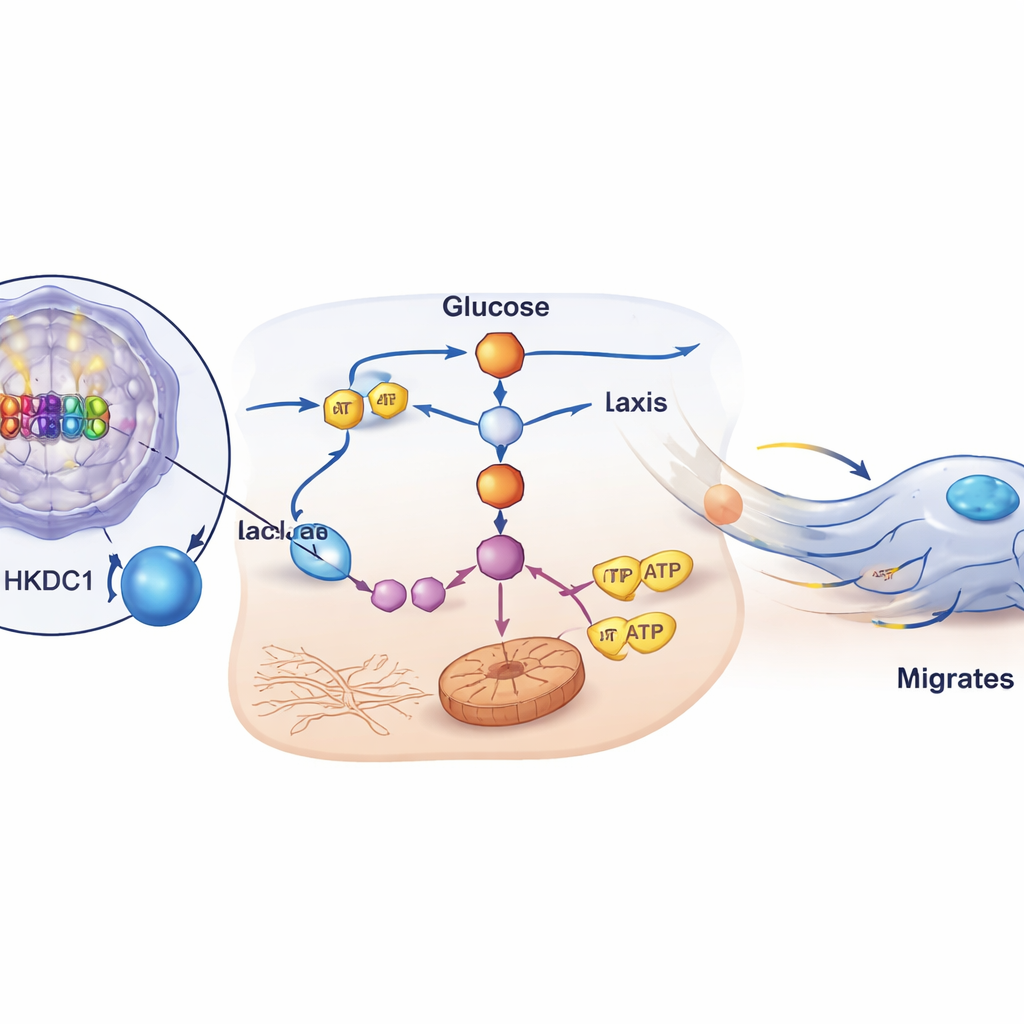
קישור מולקולרי ישיר ומעורב מרכזי
המדענים הראו כי P2‑HNF4α אינו רק מתאם עם HKDC1; הוא מפעיל את הגן הזה ישירות. באמצעות נתוני קשירה על‑רמות גנום, מבחני דו‑שלט (reporter) לקווי DNA ובדיקות קשירה חלבון–DNA הם מיפו אתרי מגניפיקטור ספציפיים באזור משפר (enhancer) של גן HKDC1 שבהם HNF4α יושב ומפעיל שעתוק. כאשר HKDC1 הוקטן בתאים, יכולתם לנוע וליצור מטסטזות פריטונאליות בעכברים צנחה משמעותית, אף על פי שהישרדותם לטווח הקצר לא הושפעה. באופן קריטי, שחזור HKDC1 בתאים שבהם HNF4α הושתק החזיר את הפעילות הגליקוליטית, ייצור האנרגיה וההתנהגות הנודדת, והוספת תוצרי מטבוליזם כמו לקטט או α‑קטוגלוטרט גם החזירו את התנועה. יחד, התוצאות האלה מעלות את HKDC1 כמאפשר מרכזי יורד דרךו P2‑HNF4α מתכנת מחדש את המטבוליזם כדי להניע גרורה.
כיבוי המתג בעזרת תרופה קיימת
מכיוון ש‑HNF4α משתייך למשפחה של חלבונים שהם לעתים קרובות מטרות טיפוליות, הצוות בדק האם תרופה מאושרת יכולה לחסום את הציר המקדם‑גרורה הזה. קודם לכן הם זיהו את חומצה מיקופנולית, הצורה הפעילה של תרופת השתל שמיקופנולאט מופטיל (MMF), כנוגד HNF4α בסרטן ריאות. כאן, טיפול ב‑MMF הקטין את רמות HKDC1 ואת הנדידה של שורות סרטן קיבה שמבטאות HNF4α גבוה, אך כמעט ולא השפיע על תאים עם HNF4α נמוך. במודלים של עכברים, MMF צמצם באופן משמעותי את המטסטזות הבטניות והוריד את הביטוי של HKDC1 — אך רק כאשר לגידולים היה P2‑HNF4α גבוה. ממצאים אלה רומזים ש‑HNF4α יכול לשמש גם כיעד טיפולי וגם כמבחן‑ביומרקר לבחירת החולים שיותר סביר שייהנו מאסטרטגיות מבוססות MMF.
מה משמעות הדבר לטיפול עתידי
במילים פשוטות, המחקר מזהה מערכת בקרה מולקולרית של דלק — P2‑HNF4α הפועל דרך HKDC1 — המסייעת לתאי סרטן הקיבה להגביר את המכשור האנרגטי שלהם ולהיות טובים יותר בהתפשטות. בכך שהוא מראה שתרופה קיימת יכולה להפריע למערכת זו ולהפחית גרורות במודלים פרה‑קליניים, הוא פותח נתיב ריאליסטי להתפתחות טיפולים חדשים לסרטן קיבה מתקדם. אם מחקרים קליניים עתידיים יאשרו את הממצאים, בדיקת פעילות HNF4α בגידולים עשויה לכוון את השימוש ב‑MMF או בסוכנים קשורים לצמצום או למניעת התפשטות קטלנית של מחלה זו.
ציטוט: Xu, X., Wu, H., Shang, J. et al. HNF4α-HKDC1 axis orchestrates a metabolic rewiring to promote migration and metastasis in advanced gastric cancer. Cell Death Dis 17, 347 (2026). https://doi.org/10.1038/s41419-026-08627-y
מילות מפתח: גרורת סרטן הקיבה, HNF4A, HKDC1, מטבוליזם סרטני, מיקופנולאט מופטיל