Clear Sky Science · he
ארגון מטבולי בידי GGCT: הסתה של גלוטמין לביוסינתזה של גלוטתיון תוך חיזוק אנאפלירוזת הגלוקוז לצורך התרבות הגידולית
מדוע זה חשוב לטיפול בסרטן
תאי סרטן גדלים במהירות, ולכן הם צורכים כמויות עצומות של דלק וחייבים להגן על עצמם באופן מתמיד מפני תוצרי לוואי רעילים של המטבוליזם שלהם. המחקר הזה חושף כיצד אנזים שלא היה מוכר מאוד, GGCT, מסייע לגידולים בכבד ובפרוסטטה להסיט באופן חכם שני מזונות נפוצים — גלוטמין וגלוקוז — כך שיוכלו גם לתדלק צמיחה וגם לשמור על מולקולות מזיקות המכונות מינים מגיבים של חמצן תחת שליטה. הבנת הטריק המטבולי הזה יכולה לפתוח דרכים חדשות להרעיב גידולים או להכריע את מניעת ההגנה שלהם.
כיצד תאי הגידול מאזנים דלק והגנה
תאי גידול תלויים במידה רבה בגלוטמין, חומצת אמינו שמשמשת תפקיד כפול: ניתן לפרק אותה כדי להזין את מחזור ייצור האנרגיה המרכזי של התא, והיא גם מספקת אבני בניין לגלוטתיון, נוגד חמצון עוצמתי שמנטרל מינים מגיבים של חמצן. המחברים אישרו תחילה שרמות הגלוטמין גבוהות יותר בגידולי כבד לעומת רקמה סמוכה בריאה, וכי תאי סרטן שגדלו עם יותר גלוטמין מתחלקים מהר יותר הן בתאיות והן בעכברים. כשהגלוטמין נדיר, התאים מאטים, חלבוני מחזור התא המרכזיים יורדים, והגידולים בחיות מצטמצמים — בחלקם מכיוון שההגנה האנטי‑חמצונית נחלשת ומינים מגיבים של חמצן מצטברים.
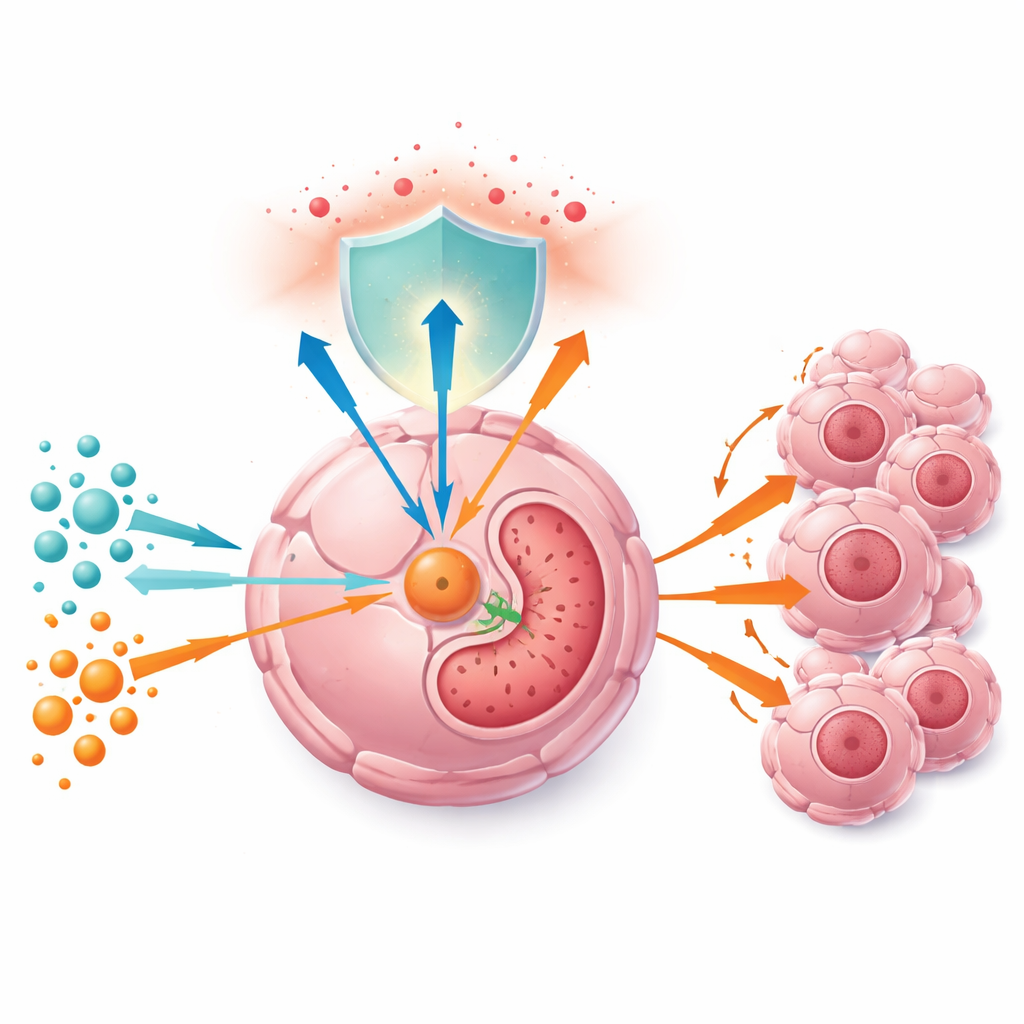
מתג מטבולי שמסתתר מול העיניים
בהסתכלות על מדגמי מטופלים ומסדי נתונים גדולים של סרטן, הקבוצה מצאה שהאנזים GGCT שורר בתדירות גבוהה יותר בגידולים של הכבד והפרוסטטה לעומת רקמות תקינות, ורמות GGCT גבוהות מנבאות תוצאה גרועה יותר. בדגימות גידול ותאים בתרבית, רמות GGCT עולות בקורלציה עם ריכוז הגלוטמין, דבר המרמז שהגידולים "קוראים" את זמינות הגלוטמין דרך חלבון זה. החוקרים פירקו שרשרת בקרה: גלוטמין שומר על גורם הצמיחה c‑Myc פעיל, אשר מדכא RNA קטן רגולטורי בשם miR‑29b‑3p; כאשר miR‑29b‑3p נמוך, GGCT משתחרר מהמגבלה שלו ומצטבר. בתת‑זמינות גלוטמין השרשרת הזו מתהפכת, miR‑29b‑3p עולה, הודעות ה‑GGCT נפרקות מהר יותר ורמת האנזים יורדת.
הסטת גלוטמין וקליטת יותר גלוקוז
כדי לבדוק מה GGCT עושה בפועל בתוך התא, המחברים הפחיתו או הגבירו את רמותיו ומדדו גם את התנהגות התאים וגם מאות מטבוליטים. השתקת GGCT עצרה את התאים במחזור החלוקה, הקטינה את המושבות שלהם והורידה באופן חד את רמות הגלוטתיון בעוד שמיני חמצן ריאקטיביים עלו; הוספת נוגד חמצון כימי הצילה חלקית את הצמיחה. תחת המיקרוסקופ, המיטוכונדריה הפכו למוארכות באופן חריג ופחות יעילות בצריכת חמצן, אף שהתאים ניסו לפצות בכך שהגבירו גליקוליזה, השלב הראשון בפירוק הסוכר. פרופיל מטבולי מפורט הראה שמתאּרכים של מחזור האנרגיה המרכזי ירדו כאשר GGCT הוסר ועלו כשהוא הוגבר.
מעקב אחר מסלול אטומי הפחמן
הצוות עקב אחר אטומי גלוטמין וגלוקוז ממוסמנים כשהם זורמים דרך מטבוליזם הגידול. כאשר GGCT הובע בכמות גבוהה, פחות גלוטמין ממוסמן הגיע למחזור האנרגיה, ויותר הוסט ליצירת גלוטתיון חדש, שתמך בהגנה האנטי‑חמצונית. בו בזמן, גלוקוז מסומן תרם ביתר שאת למחזור, מפצה על ההסחה של הגלוטמין. צורת מוטנטית של GGCT שהייתה חסרת פעילות אנזימטית רגילה לא יכלה להניע את השינויים הללו או לקדם התרבות, מה שמראה כי הפעילות הקטליטית של GGCT חיונית. באופן משמעותי, אספקת פירובט נוספת או שינוי נקודת הכניסה למחזור האנרגיה השיבו את רמות האנרגיה התאית אך לא הורידו את המינים המגיבים של חמצן, מה שמעיד ש‑GGCT שולט בעיקר באיזון החמצון‑חיזור דרך גלוטתיון, לא באמצעות שינויים פשוטים באספקת האנרגיה.
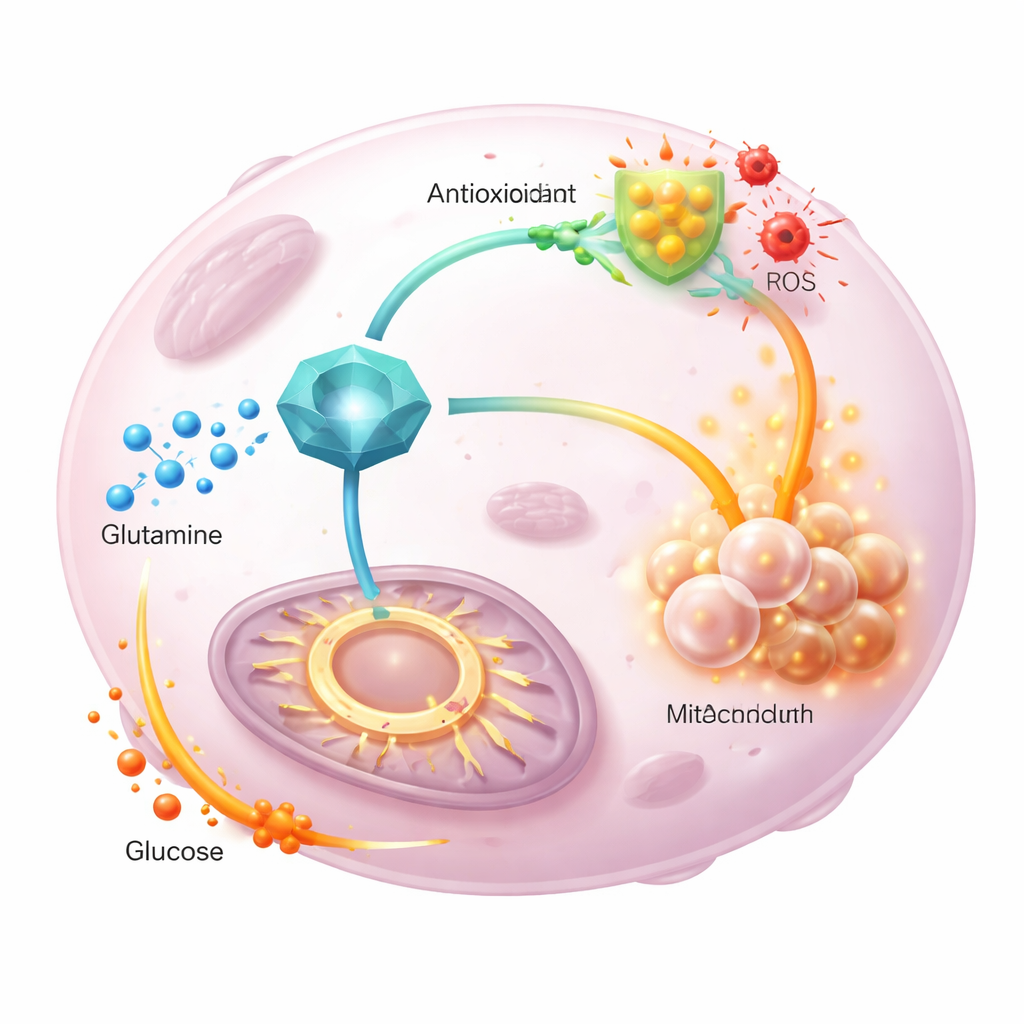
מה משמעות הדבר לטיפולים עתידיים
בהרכבה, הממצאים מציבים את GGCT כמתאם מרכזי שמאפשר לגידולים לפצל את המשימות של הגלוטמין: הוא מוליך חלק גדול יותר של המזון הזה לייצור נוגדי חמצון בעוד שהוא מושך גלוקוז אל מחזור האנרגיה לשמירה על חלוקת התאים. במודלים של בעלי חיים, דיכוי GGCT האט את גדילת הגידול, הקטין את גלוטתיון והגביר את הלחץ החמצוני, ותופעות אלה ניתנו להפיכה חלקית בעזרת תרופת נוגד חמצון. לצופה שאינו מומחה, המסר הוא שחלק מסוגי הסרטן שורדים באמצעות שימוש ב‑GGCT כמפסק מטבולי; תרופות שמנטרלות מפסק זה עשויות להחליש בו‑זמנית את ההגנה של הגידול מפני נזק חמצוני ולהפריע לשימוש הגמיש שלו במזונות, ובכך להפוך טיפולים סטנדרטיים ליעילים יותר.
ציטוט: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
מילות מפתח: מטבוליזם של סרטן, גלוטמין, גלוטתיון, לחץ חמצוני, אנזים GGCT