Clear Sky Science · he
שינוי תכונה לאדיפוגני מתכנת מחדש תאי PDAC בעלי EMT גבוה למצב דמוי אדיפוציט לאחר מיטוזה ומגביל גרורות
הפיכת תאי סרטן תוקפניים לשומן חסר־פגע
סרטן הלבלב הוא אחד מסוגי הסרטן הקטלניים ביותר, בעיקר משום שהוא מתפשט מוקדם ומגיב בקושי לטיפולים סטנדרטיים. המחקר חוקר רעיון שונה באופן מרשים: במקום לנסות להרוג או להרעיב את תאי הגידול, מה אם נוכל לשדל את תאי הסרטן המסוכנים ביותר בלבלב להתמיין לתאים דמויי שומן שאינם מתחלקים ואינם נודדים בגוף? העבודה מתארת כיצד החוקרים דחפו תאי סרטן לבלב אגרסיביים לתוך מצב יציב דמוי תאי שומן, שהאט גדילת גידולים והפחית פיזור בעכברים, ברמז לגישה חדשה לשליטה במחלה ההרסנית הזו.
למה סרטן הלבלב כל כך קשה לעצירה
אדנו־סרטן צינוריות הלבלב, הצורה העיקרית של סרטן הלבלב, בעל תחזית ירודה: רק כשחלק ממונה אחד מתוך שמונה חולים שרד חמש שנים אחרי האבחנה. חלק מהבעיה הוא שרבים מתאי הגידול במחלה זו נמצאים במצב משתנה שנקרא EMT, שמקנה להם ניידות מוגברת, חדירות לעמקים רקמתיים ועמידות לתרופות. ניסיונות לחסום את האותות הרבים שמניעים מצב זה הביאו תועלת מוגבלת. במקביל, הלבלב והגידולים בו מראים נטייה מפתיעה לצבור תאי שומן, מה שמעורר את השאלה האם הפלסטיות הסמויה הזו של זהות התאית ניתנת לניצול. הכותבים הניחו שאם תאי סרטן עם EMT גבוהים כבר מוכנים לשינוי, אולי ניתן להפנותם לזהות שקטה ודמוי־שומן במקום לזהות חודרת.
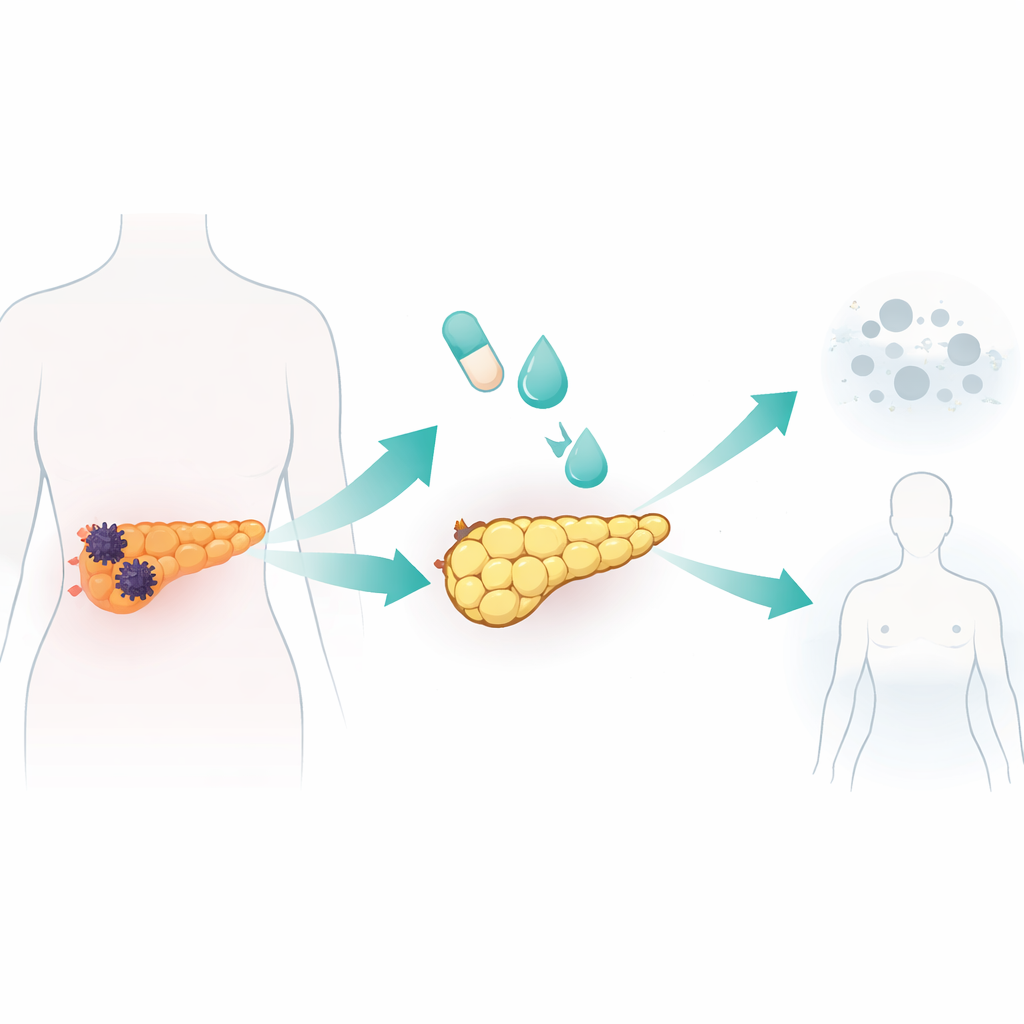
תכנות מחדש של תאי סרטן לתאי דמויי שומן במעבדה
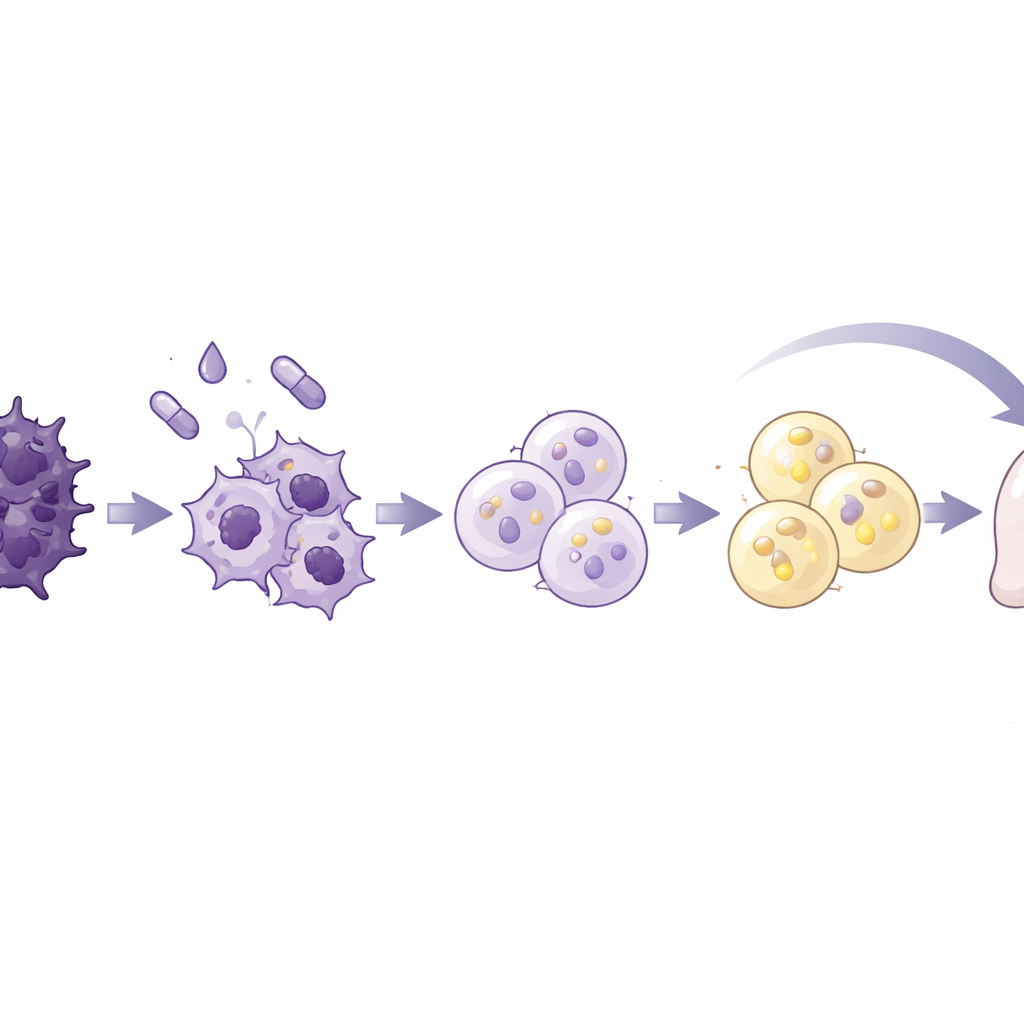
הקבוצה בחנה קוקטייל סטנדרטי ליצירת תאי שומן, שכבר שימש במחקרים קודמים על ביולוגיית שומן וסרטן השד, על שבע שורות תאי סרטן לבלב אנושיות ושורת תאי לבלב נורמלית אחת. התערובת שילבה אינסולין וסטרואיד יחד עם רוזיגליטזון, תרופה שמפעילה רגולטור מרכזי של יצירת שומן, וכן חלבון איתות בשם BMP2 כדי לשחרר את הפלסטיות התאית. אחת משורות הסרטן, בשם AsPC-1, התגברה במיוחד על הטיפול. במשך עשרה ימים התאים הללו הפכו לגדולים ועגולים יותר ומולאו בטיפות שומן — סימני ההיכר של תאי שומן. הם הפעילו גנים וחלבונים טיפוסיים של תאי שומן בשלים והראו מטבוליזם שומני פעיל, כולל הפרשת אדיפונקטין ופירוק מאגרי השומן בתגובה לאות מתאים. באופן מכריע, התאים המומרו הפסיקו להתחלק, נעצרו בשלב מוקדם של מחזור התא, ונעו ופעלו בפחות חדירה בהשוואה לתאי סרטן לא מטופלים.
כיבוי תוכנית הסרטן עמוק בתוך התא
כדי להבין מה התרחש ברמה המולקולרית, החוקרים ניתחו את אריזת ה‑DNA ופעילות הגנים בתאים המומרים. הם מצאו הידוק נרחב של הכרומטין, קומפלקס ה‑DNA וחלבונים השולט בגישה לגנים, יחד עם ירידה כללית בביטוי הגנים — שתי תכונות של תאים שאינם מתחלקים. גנים התומכים ב‑EMT, בחדירה ובגרורות, כולל אנזימים המפרקי מטריצה ומווסתי EMT מרכזיים, דוכאו בחוזקה, בעוד גנים הקשורים לשומן הוגברו. חתימת הגנים הכוללת השתנתה ממזהות מזנצימלית, ניידת מאוד, לזו שהדימה במידה רבה תאי שומן בשלים. אותות הקשורים לצמיחת תאים ולתגובה לנהג EMT מרכזי, TGF‑beta, נחלשו, בעוד מסלולים הקשורים לטיפול בליפידים ולהדבקות תאית התחזקו. שינויים אלה מציעים שהתאים לא רק הושרו קלות, אלא עברו תכנות מחודש יסודי.
מבחן האסטרטגיה בעכברים
המדענים בדקו האם המרה כפויה לדמוי־שומן יכולה לעזור לשלוט בגידולים בחיות חיות. הם השתילו תאי סרטן לבלב אנושיים ללבלב או לטחול של עכברים כדי לדמות גידולים ראשוניים וגרורות כבד. עכברים שטופלו ברוזיגליטזון ו‑BMP2 פיתחו גידולים לבלביים קטנים יותר והציגו טיפות שומן עשירות וסימני תאי שומן בתוך הגידולים, יחד עם רמות נמוכות יותר של גנים הקשורים ל‑EMT וחדירה. במודל הגרורתיות, הטיפול לא שינה את נביטת הגידולים הראשונית, אך לאורך זמן האט את התרחבות העומס הגידולי בכבד בהשוואה לבעלי החיים שלא טופלו. חשוב לציין כי רקמת הלבלב השכנה הנורמלית לא הראתה המרה ברורה לדמוי־שומן, ומצב הדמוי־שומן בגידולים נמשך לפחות חודש לאחר הפסקת התרופות, מה שמרמז על דרגה של עמידות וספציפיות.
מה המשמעות של זה לטיפול בסרטן בעתיד
המחקר תומך בקונספט מעורר מחשבה: עבור סרטןי לבלב בעלי פלסטיות גבוהה ועשירים ב‑EMT, ייתכן שאפשר "להמיר במקום להרוג" — להפנות תאי גידול מסוכנים ונודדים לתאים יציבים שאינם מתחלקים ודמויי־שומן, שפחות יכולים להתפשט. למרות שמדובר בעבודה בשלבי־התחלה בתאים ובמודלים של עכברים, ושלא כל סוגי סרטן הלבלב מגיבים באותה מידה, זה פותח אפיק טיפולי חדש שפועל על ידי שינוי זהות התאית במקום רק חסימת אותות גדילה. בעתיד, גישות טרנסדהיפרנציאציה כאלה עשויות להשתלב עם תרופות ממוקדות או אימונותרפיות כדי להחזיק את סרטן הלבלב במצב שקט וניתן לניהול ולהפחית את הסיכון לגרורות קטלניות.
ציטוט: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
מילות מפתח: סרטן הלבלב, פלסטיות תאית, טרנסדהיפרנציאציה, מעבר אפיתלי-בנכייני (EMT), תאי דמוי אדיפוציט