Clear Sky Science · he
עיכוב קינאזת וירוציניה־קשורה 2 חושף פגיעות במטבוליזם הגלוטתיון בסרטן הלבלב
מדוע זה חשוב לסרטן הלבלב
סרטן הלבלב נחשב לאחד הסרטנים הקטלניים ביותר, בין היתר משום שטיפולים מקובלים לרוב אינם יעילים. מחקר זה חושף חולשה נסתרת בגידולים מסוימים בלבלב: תלות במעין "מגן" תאים מפני תוצרי חמצון רעילים. על ידי הבנת מתי המגן הזה פגיע, וכיצד גן הסרטנים VRK2 מחזק אותו, החוקרים מציעים דרכים חדשות להרוג תאי סרטן באופן סלקטיבי תוך שמירה על רקמות בריאות.
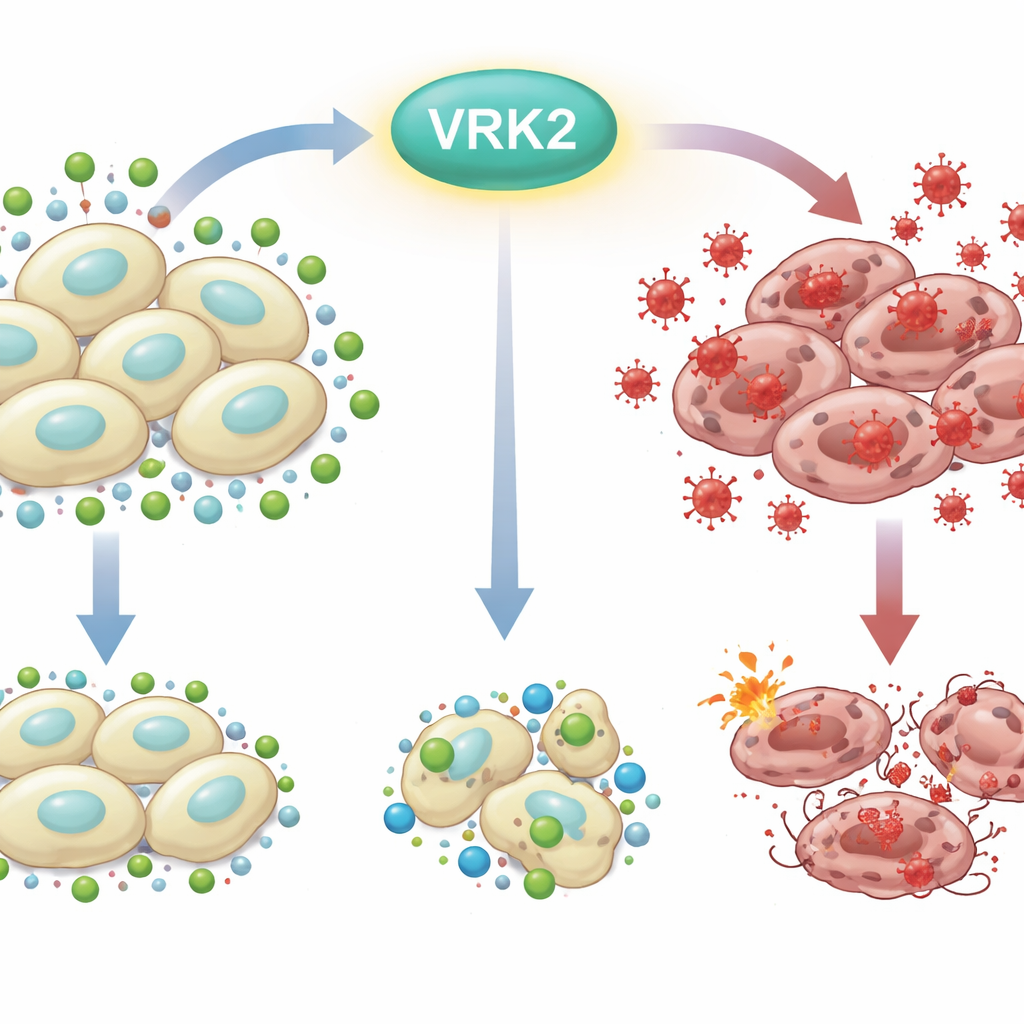
בעיית החלודה התאית
כל תא נלחם ללא הפסקה ב"חלידה מבפנים" הנגרמת על־ידי סוגי חמצן פעילות—צורות חמצן ריאקטיביות שעלולות לפגוע ב‑DNA, בשומנים ובחלבונים. כדי לשרוד משתמשים התאים בהגנות כימיות, כאשר הגלוטתיון משמש כאחת המגינות החשובות ביותר. תאי סרטן הלבלב, החיים בתנאים קשים וצומחים במהירות, נסמכים במידה רבה על טריקים מטבוליים כדי לשמור על מלאי גלוטתיון מספיק. שיבוש האיזון בין חמצונים מזיקים לנוגדי חמצון מגנים יכול לדחוף תאי סרטן מעבר לקצה ולהוביל למותם.
מציאת נקודת תורפה נסתרת
החוקרים התחילו בכיבוי VRK2, גן המקדם סרטן שאותו קישרו בעבר לתוצאות גרועות בסרטן הלבלב, ואז בדקו 281 תרכובות המכוונות מטבוליזם. הם גילו שתאים חסרי VRK2 היו רגישים במיוחד לתרופות החוסמות יצירת גלוטתיון. בתאים עם חוסר ב‑VRK2 ירדו רמות הגלוטתיון בעוד שהחמצון הריאקטיבי זינק, מה שהוביל למות התאים. אספקת נוגדי חמצון נוספים או מולקולות הדומות לגלוטתיון הצילה אותם, ואישרה שהחולשה המרכזית נבעה מהיכולת המוחלשת שלהם לנטרל לחץ חמצוני.
כיצד VRK2 מסייעת לתאים לחמוש
בהמשך שאל הצוות מדוע VRK2 משנה את מטבוליזם הגלוטתיון. הם התמקדו בחלבון ממברנלי מוביל בשם SLC7A11, שנמצא בממברנת התא ומוביל פנימה ציסטין, חומר־בניין הדרוש ליצירת גלוטתיון. באופן מפתיע, VRK2 לא שינתה את כמות SLC7A11 שהופקה בתא באופן כולל; במקום זאת היא नियंत्रת האם אותו נשא מגיע בהצלחה לפני שטח התא. בתאים בריאים עם VRK2 פעילה, SLC7A11 נוסע מהרשת האנדופלסמטית לגולג'י ואז לממברנה. VRK2 מחזקת את היסעים האלה על‑ידי שינוי כימי של חלבון מיון מטענים בשם Sec24C, שעוזר לטעון את SLC7A11 לתוך וזיקולות הובלה. כאשר VRK2 נעדרת או נחסמת, SLC7A11 נתקעת בתוך התא, פחות נשאים מגיעים לפני השטח והמגן של הגלוטתיון נחלש.
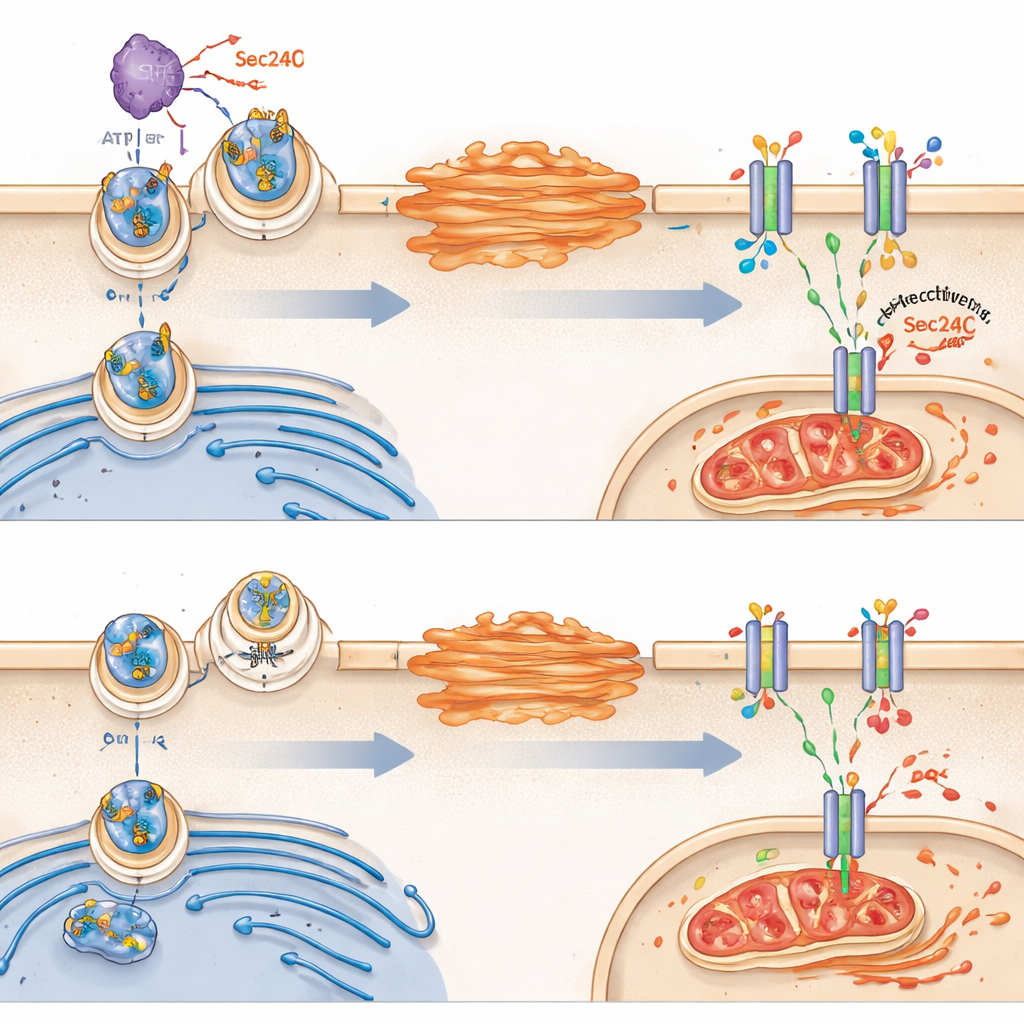
מגן שבור לפרורפטוזיס
בלי מספיק SLC7A11 בממברנה, תאים חסרי VRK2 מתקשים לייבא ציסטין ולשמור על גלוטתיון. זה משאיר אותם פגיעים במיוחד לצורת מוות תאי התלויה ברזל הקרויה פרורפטוזיס, המתאפיינת בחמצון בלתי נשלט של שומני הממברנה ונזק מיטוכונדריאלי. המחקר הראה שתרופות החוסמות יצירת גלוטתיון גרמו לסימני פרורפטוזיס בתאים חסרי VRK2, כולל מיטוכונדריות מעוותות והצטברות תוצרי חמצון שומניים. חסימת הפרורפטוזיס, אבל לא סוגי מוות תאי אחרים, הגנה על תאים אלה, מה שמדגיש שהתורפה שלהם היא חוסר יכולת להכיל נזק חמצוני.
הנחיית בחירות טיפול מותאמות
לבסוף, החוקרים עברו למודלים חיים ולתאים שמקורם ישירות בחולים. גידולים עם רמות VRK2 נמוכות הצטמצמו בטיפול בתרופה המכוונת גלוטתיון, בעוד שגידולים בעלי הבעה גבוהה של VRK2 היו עמידים במידה רבה. עם זאת, כאשר לגידולים עם VRK2 גבוהה נתנו גם תרכובת החוסמת VRK2, הם חזרו להיות רגישים לעיכוב גלוטתיון. הדבר מרמז שרמות VRK2 יכולות למיין חולים לקבוצות: אלה שהגידולים שלהם פגיעים באופן טבעי לטיפולים המכוונים גלוטתיון, ואלה שעשויים להרוויח מאסטרטגיה דו‑שלבית שמכבה קודם את VRK2 ואז תוקפת את מטבוליזם הגלוטתיון.
מה זה אומר עבור מטופלים
בהירות—עבודה זו מראה שחלק מסרטני הלבלב שורדים באמצעות שימוש ב‑VRK2 כדי לשמור על מגן נוגדי חמצון חזק. בלעדיה, המגן דק; ובנוסף להוצאה של גלוטתיון, תאי הסרטן קרסים תחת הלחץ החמצוני. מדידת VRK2 בגידולים יכולה לכן לסייע לרופאים לקבוע מי הסביר להפיק תועלת מתרופות המפריעות למטבוליזם הגלוטתיון, ומי עשוי להזדקק קודם לצעד המכוון VRK2. למרות שיש צורך בניסויים נוספים בבני אדם, המחקר מצייר דרך ברורה לעבר טיפולים מותאמים יותר מבוססי מטבוליזם עבור סרטן שזקוק בדחיפות לאופציות טובות יותר.
ציטוט: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
מילות מפתח: סרטן הלבלב, מטבוליזם גלוטתיון, VRK2, פרורפטוזיס, SLC7A11