Clear Sky Science · he
טרימתילציה של ליזין 36 על היסטון H3 על ידי SETD2 מעצבת נוף אפיגנטי בתאי גזע מעיים כדי לתאם מטבוליזם שומני ולהחליש הזדקנות תאית
מדוע תאי גזע מעיים חשובים ככל שמתבגרים
עמוק בשכבת הרירית של המעיים שלנו, תאי גזע זעירים עובדים ללא הפסקה כדי לחדש את הרקמה המסייעת בעיכול המזון ובקליטת החומרים המזינים. ככל שאנחנו מתבגרים, תאים אלה נשחקים, מה שהופך את המעי לרגיש יותר למחלות ולהחלמה איטית יותר. המחקר הזה בוחן כיצד תגיות כימיות עדינות על חלבוני האריזה של ה-DNA מסייעות לשמור על תאי הגזע המעיים צעירים, כיצד אובדן תגיות אלה מחריב את שריפת השומן בתוך התאים, ואיך תרופות נבחרות בקפידה עשויות יום אחד להאט את התדרדרות זו.
תאים מתבגרים בסביבה תובענית
המשטח הפנימי של המעי הוא אחת מהרקמות המתחדשות במהירות ביותר בגוף. תאי גזע הממוקמים בבסיס כיסים זעירים, הנקראים קריפטות, מתחלקים כדי להחליף מיליארדי תאים כל מספר ימים. עבודה מתמדת זו דורשת אספקת אנרגיה יציבה, רבות ממנה משילוב ושבירת שומנים. במקביל, תאי גזע אלה נשלטים על ידי קוד "אפיגנטי"—תגיות כימיות על חלבוני היסטון שמסייעות לקבוע אילו גנים פעילים ואילו מושתקים. המחברים התמקדו בסמן אחד כזה, הידוע כטרימתילציה של H3K36, הנוצרת על ידי האנזים SETD2, ובחנו האם שינויים בסמן זה עשויים להסביר מדוע תאי גזע מעיים מאבדים את החיוניות שלהם עם ההזדקנות.
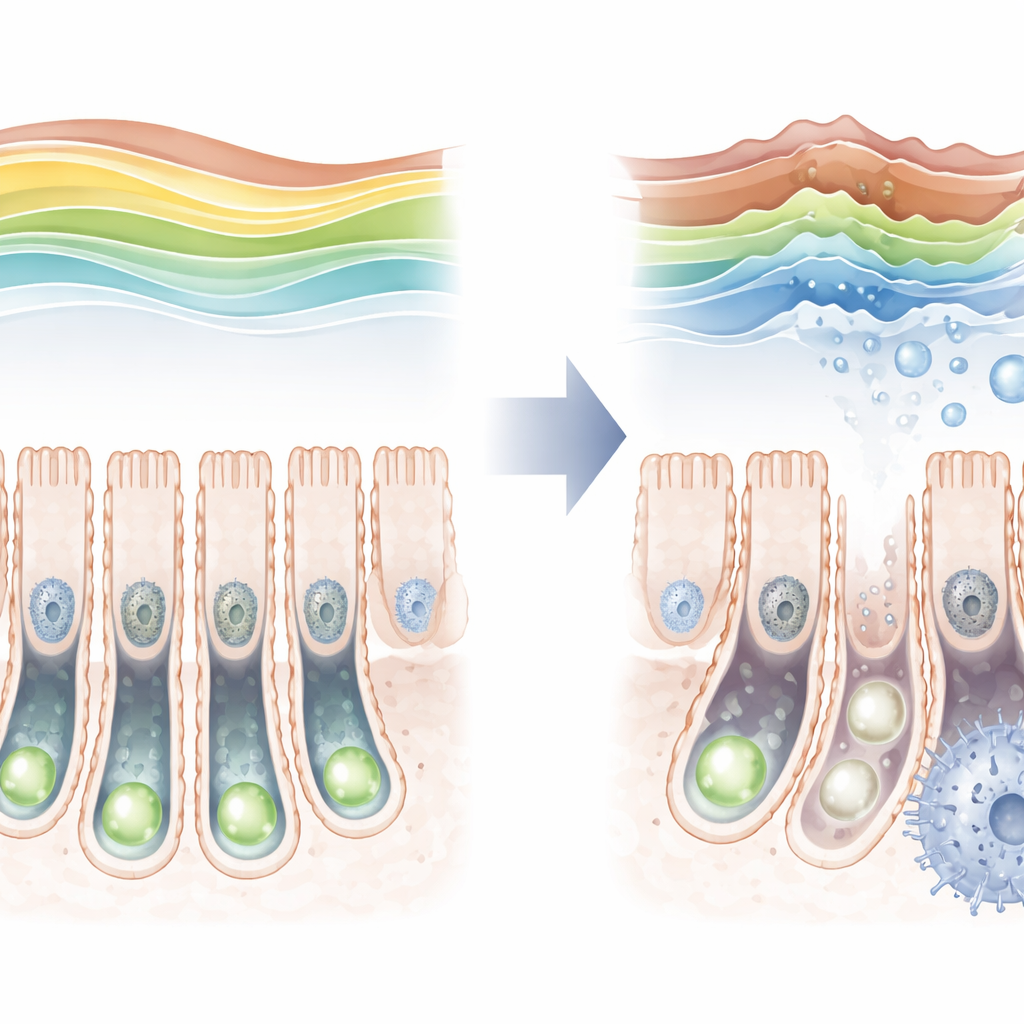
תג מגן שנחלש עם הגיל
על ידי בדיקה של מעיים בעכברים לאורך חיי הפרט, החוקרים מצאו שהטרימתילציה של H3K36 אינה קבועה. היא יחסית נמוכה מיד לאחר הלידה, עולה לשיא בבוגרים צעירים ואז יורדת שוב בגיל המבוגר. כאשר הסמן ירד בחיות מבוגרות, סימנים להזדקנות תאית עלו בתאי הגזע, מה שמעיד על קשר בין השניים. כדי לבדוק זאת ביתר ישירות, הצוות ייצר עכברים שבהם ניתן היה להשמיט את SETD2 אך ורק בתאי הגזע של המעי. כאשר האנזים הוסר, הסמן המגן כמעט נעלם, תאי הגזע התחלקו בתדירות נמוכה יותר, והם התקשו לייצר את המגוון המלא של סוגי התאים המתמחים של המעי.
כיצד שינויים אפיגנטיים מחריגים את שריפת השומן
אובדן סמן היסטון יחיד זה הצית שרשרת שינויים בתוך תאי הגזע. מדידות פעילות הגנים הראו כי גנים רבים המעורבים במחזור התא ובהעתקת DNA כבו, בעוד שגנים הקשורים ללחץ והזדקנות הודלקו. באופן בולט, האות החזק ביותר הצביע על הפרעה בטיפול בשומנים: גנים התומכים בדרך כלל בחמצון חומצות שומן—שריפת שומן מבוקרת להפקת אנרגיה—נחלשו, ושומנים החלו להצטבר בקריפטות. פרופיל המטבוליטים אישש כי חומצות שומן ארוכות-שרשרת הצטברו, אות לכך שדרכי עיבוד השומן המקובלות התקלקלו. במקביל, אריזת ה-DNA בגרעין השתנתה: אזורים רבים הפכו לחשופים יותר או לסגורים יותר, מה ששינה אילו גנים התא יכול להשתמש בהם בקלות.
מרנני כרומטין וצעדת ההזדקנות
כדי להבין כיצד שינויים באריזת ה-DNA נוצרים, המחברים מיפו אזורי כרומטין פתוחים ומכלול של תגי היסטון אחרים ברחבי הגנום. כאשר טרימתילציה של H3K36 אבדה, מקטעים גדולים של DNA צברו תגיות "פעילות" והפכו לנגישים יותר, במיוחד בסמוך לגנים הקשורים למטבוליזם והזדקנות. שחקן מרכזי במעבר הזה היה קומפלקס רמונקול הכרומטין SWI/SNF, המונע על ידי תת־יחידה מרכזית בשם SMARCA4. בתאי גזע חסרי SETD2, רמות SMARCA4 עלו, והקומפלקס נראה כמי שעוזר לפתוח אזורים שמניעים תוכניות הזדקנות. כאשר החוקרים הפחיתו את פעילות SMARCA4 באופן גנטי או בעזרת מעכב ממוקד, תאי הגזע החזירו חלק מיכולתם ליצור מיני-מעי בריא במבחנה, וסימני ההזדקנות ירדו—מה שמרמז כי רה-ארגון יתר דוחף תאים אלה למצב מותש וסננטי.
התעוררות מסלולי אנרגיה להצלת תאי גזע
מכיוון שהפרעת חמצון השומן עלתה כבעיה מרכזית, הצוות בדק האם חיזוק המסלול הזה יכול להתנגד להזדקנות תאי הגזע. הם השתמשו בתרופה שמפעילה את PPARα, רגולטור על של חמצון חומצות השומן. בארגנואידים שגודלו מתאי גזע חסרי SETD2, הטיפול הזה הגביר את הגדילה, השיב את המבנים המתפתחים האופייניים לתאי גזע בריאים והפחית הצטברות שומן. בעכברים חיים, ההתערבות הזו מילאה חלקית את מאגר תאי הגזע, הקטינה סמני הזדקנות ונורמלזה הצטברות השומנים בקריפטות המעי. ממצאים אלה מציבים את חמצון חומצות השומן כקשר חיוני בין בקרה אפיגנטית לבריאות תאי הגזע.
מה זה אומר להזדקנות בריאה
ביחד, העבודה מראה שסמן היסטון ספציפי, המתופקד על ידי SETD2, עוזר לשמור על נוף אפיגנטי מאוזן בתאי גזע של המעי. כאשר סמן זה נחלש, הכרומטין עובר רה-ארגון לא תקין, מסלולי שריפת השומן נחלשים, שומנים מצטברים והתאים נוטים להיסחף למצב של זקנה תאית, מה שמחליש את מערכת התיקון של המעי. על ידי עיכוב המכונה הרמונסטית המוגזמת או שיקום מטבוליזם השומן בעזרת תרופות ממוקדות, ייתכן שניתן לשמר את תפקוד תאי הגזע ואת בריאות המעי בגיל המבוגר. אמנם ממצאים אלה נובעים מעכברים, הם מהדהדים תבניות הנצפות בהפרעות מעיים אנושיות, ומעלים את האפשרות שטיפולים מטבוליים מכוונים בקפידה עשויים יום אחד לסייע בהתמודדות עם ירידה תלויה גיל בתאי הגזע המעי שלנו.
ציטוט: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
מילות מפתח: תאי גזע של המעי, אפיגנטיקה, חמצון חומצות שומן, הזדקנות תאית, SETD2