Clear Sky Science · he
RNA קשור ל‑Lamp2a שמופרש על‑ידי ADSCs מונע משוב ENO1–לקטילציה–גליקוליזה והתנהגות ממאירה של תאים בסרטן השד המשולש‑שלילי
מדוע זה חשוב עבור מטופלים
סרטן השד המשולש‑שלילי הוא אחד הצורות האגרסיביות ביותר של סרטן השד וחסר את המטרות ההורמונליות או של גורמי גדילה שעושות תת‑הסוגים אחרים ניתנים לטיפול בקלות יחסית. המחקר חושף כיצד גידולים אלו משנים את ניצול האנרגיה שלהם כדי לשרוד בסביבות עם חמצן נמוך ומתאר דרך יצירתית לתקוף את אותה תשתית. לקוראים, הוא מספק הצצה לאופן שבו הבנה של מטבוליזם הסרטן יכולה להוליד טיפולים חדשניים וממוקדים מאוד, השונים במידה ניכרת מכימותרפיה מסורתית.
כיצד גידולים אלה מזינים את עצמם
מחלות סרטניות רבות נשענות במידה רבה על דרך מהירה אך לא יעילה לייצור אנרגיה הנקראת גליקוליזה, שהופכת סוכר לתוצר לוואי שנקרא לקטט. בבדיקת דגימות מטופלים, מאגרי גנים ציבוריים ומספר קווי תאים של סרטן השד, החוקרים מראים שגידולים משולש‑שליליים נטוים יותר לגליקוליזה מאשר סוגי סרטן שד אחרים. אנזים מרכזי במסלול זה, ENO1, נמצא ברמות גבוהות במיוחד בגידולים אלה וקושר תוצאת הישרדות גרועה יותר. כאשר רמות ENO1 הופרעו בתאי משולש‑שליליים במעבדה, התאים עברו מהגליקוליזה לכיוון ייצור אנרגיה מיטוכונדריאלי תקין יותר, גדלו לאט יותר והיו פחות מסוגלים לחדור או ליצור מושבות.
לולאת משוב מסוכנת בתוך תאי הסרטן
בהעמקה, הצוות גילה שהלקטט עצמו מחזק את ENO1 ונועל את תאי הסרטן במעגל אלים. לקטט יכול לשנות חלבונים כימית בתהליך הנקרא לקטילציה. בתאים משולש‑שליליים, עודף לקטט הגדיל את לקטילציית ENO1, מה שחיזק את פעילותו ויציבותו של האנזים, האצה נוספת של הגליקוליזה וייצור עוד לקטט. בתנאי־חמצן נמוך—טיפוסיים לגידולים מוצקים—הלולאה הזו התחזקה, וסייעה לתאי הסרטן לעמוד בפני מוות תאי ולהמשיך להתחלק. חסימת פעילות ENO1 בעזרת מעכב מולקולרי קטן, או הפחתת ייצור הלקטט, החלישו את הלולאה, צימקו את הגליקוליזה והאטו את גדילת הגידול בעכברים.
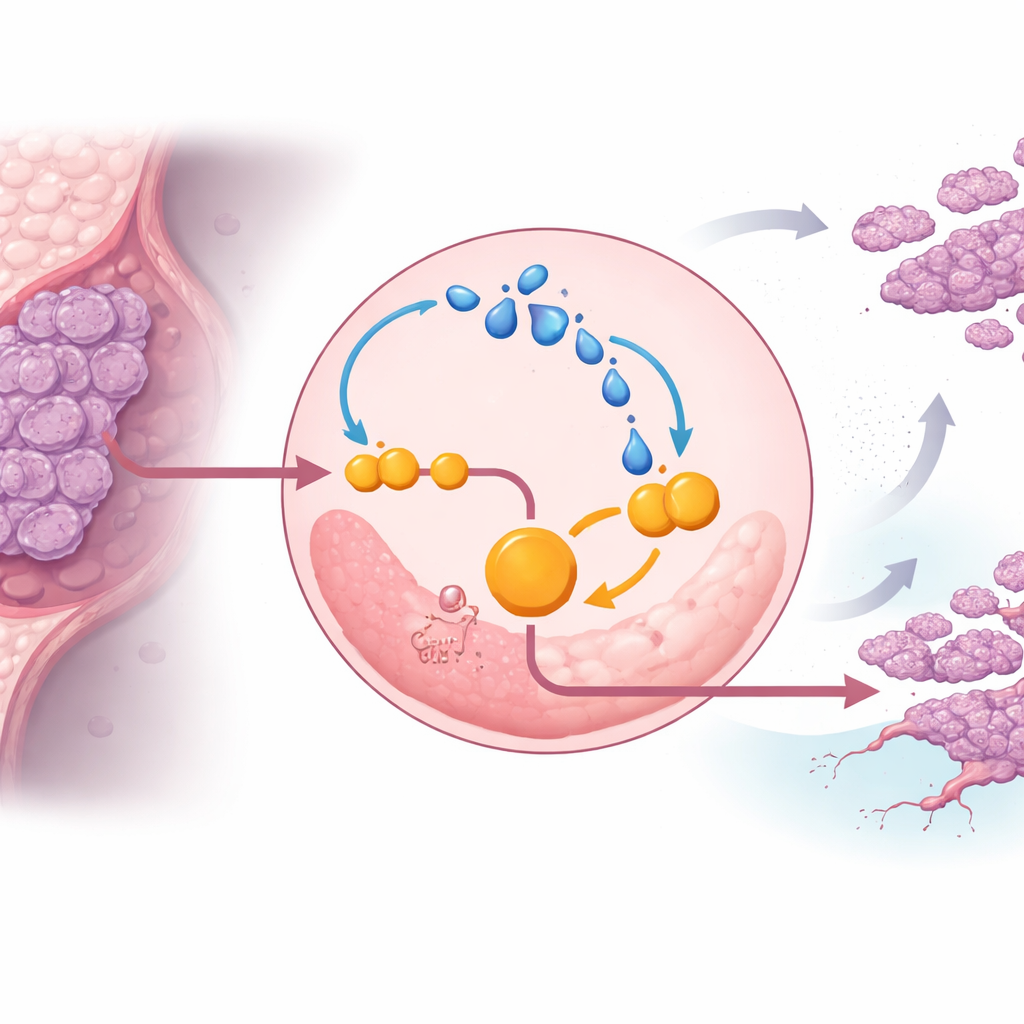
המנגנון המולקולרי שמגן על ENO1
המחקר זיהה נקודת בקרה ספציפית ב‑ENO1 שעושה את הלולאה הזו לאפשרית. חלבון ידוע בשם EP300 מוסיף תגי לקטיל מבוססי לקטט לכמה אתרי ליזין ב‑ENO1, כאשר אתר אחד, שכונה K262, מסתבר שהוא קריטי. כאשר אתר זה הונדס כך שלא יכול היה להיות לקטילט, ENO1 נשלח במהירות למרכזי המיחזור של התא — הליזוזומים — ופורק. ללא התג המגן הזה, תאים משולש‑שליליים איבדו חלק ניכר מדחיפת הגליקוליזה שלהם ומהיכולת ליצור גידולים ומטסטזות במודלים בחיה. זה בולט את לקטילציית ENO1 ב‑K262 כמתג מולקולרי שמגן על האנזים מפירוק ומקיים את המטבוליזם המעוות של הסרטן.
דרך חדשה לסמן את ENO1 להריסה
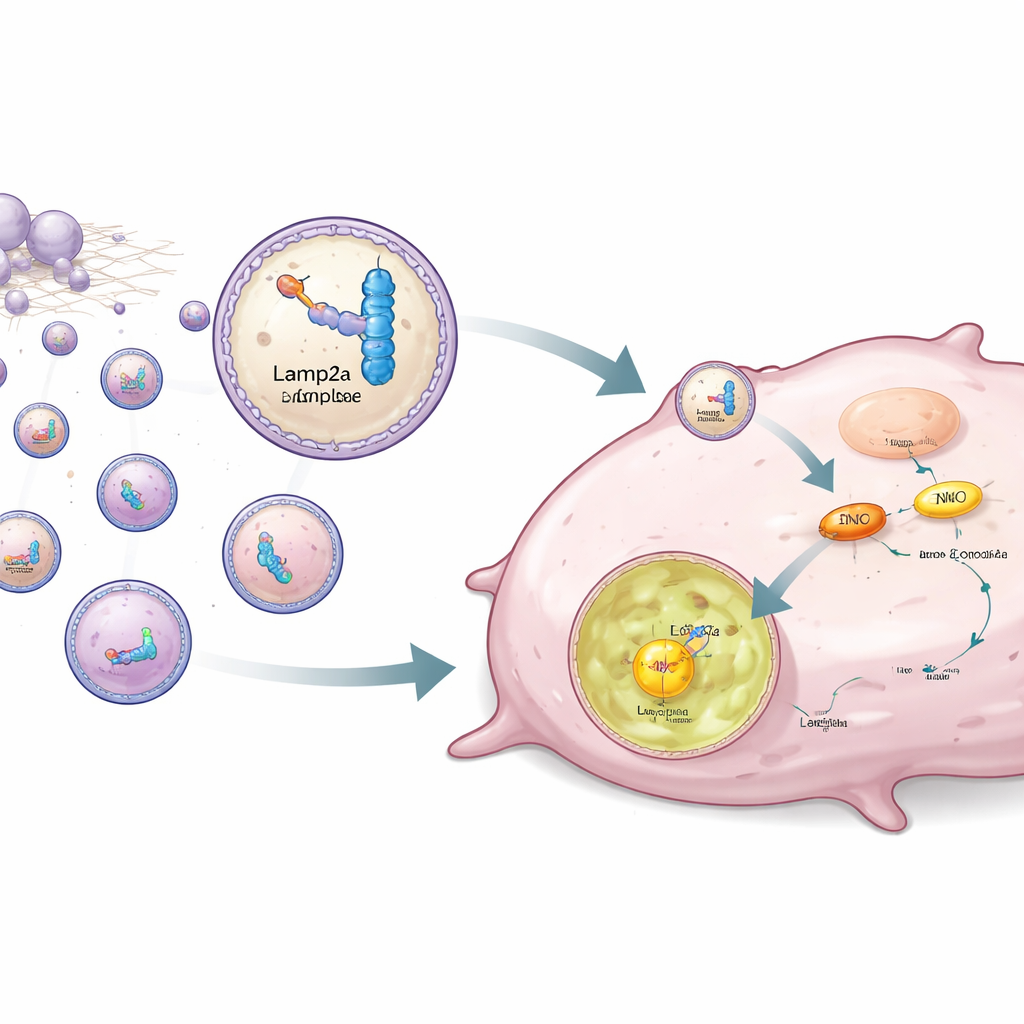
במקום להסתפק רק בחסימת ENO1, המחברים תכננו אסטרטגיה להסירו באופן סלקטיבי מתאי סרטן. ENO1 פועל גם כחלבון קשירת RNA, שמזהה רצפי RNA קצרים ספציפיים. הצוות הנדס מקטעים RNA סינתטיים שנקשרים חזק ל‑ENO1 וקשר אותם ל‑Lamp2a, חלבון ממברנת ליזוזום המעורב ברוסס חלבונים ממוקד. תאי גזע שמקורם בשומן אנושי עובדו גנטית כדי לייצר את צמד ה‑RNA–Lamp2a הזה ולחבילו בתוך שלפוחיות זעירות הנקראות אקסוזומים. כאשר אקסוזומים מהונדסים אלו נוספו לתאים משולש‑שליליים, חלק ה‑RNA התחבר ל‑ENO1, בעוד שחלק ה‑Lamp2a הדריך את כל המורכב אל הליזוזומים, שם ENO1 פורק גם אם נשא את אות הלקטילציה המאשרת יציבותו.
בדיקת גישת הרס ממוקד בבעלי חיים
כדי לקרב את הרעיון הזה לטיפול פרקטי, החוקרים גידלו את תאי הגזע הממושרים על תשתית ביורסקיבילית והשתילו את המבנה הזה מתחת לעור של עכברים, סמוך לגידולים משולש‑שליליים. מהמיקום הזה שחררו תאי הגזע ברצף אקסוזומים שנשאו את המורכבים הממוקדים ל‑ENO1. בגידולים של עכברים אלה נצפו רמות חלבון ENO1 נמוכות בהרבה, גליקוליזה מצומצמת, פחות תאים מתחלקים ועוד סממנים למוות תאי בהשוואה לבעלי החיים בביקורת. הגידולים גדלו לאט יותר והתנהגותם הממאירה דעכה באופן ברור, מה שמדגים כי הכוונת ENO1 לליזוזומים יכולה לרעב את הסרטן ממסלול החומרת דלק המועדף עליו.
מה זה יכול להשפיע על טיפול עתידי
לקהל שאינו מומחה, המסר המרכזי הוא שהעבודה הזו חושפת גם חולשה וגם זווית טיפולית חדשה אפשרית לסרטן השד המשולש‑שלילי. החולשה היא התלות של הגידול בלולאת אנרגיה מחזקת‑עצמה הבנויה סביב ENO1 ולקטט, במיוחד באזורים בעלי חמצן נמוך. זווית הטיפול היא מערכת הרס חלבוני ממוקדת שמשתמשת ב‑RNA מותאם אישית ואקסוזומים שמקורם בתאי גזע כדי לגרור את ENO1 למכונת ההיפטרות של התא. אמנם הדרך לשימוש קליני ארוכה, גישה זו ממחישה כיצד הבנה מעמיקה של הטריקים המטבוליים של הסרטן יכולה להשרות טיפולים מדויקים שמנסים לנטרל, במקום פשוט לרעול, תאים ממאירים.
ציטוט: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
מילות מפתח: סרטן השד המשולש‑שלילי, מטבוליזם של סרטן, אותות לקטט, רוסס חלבוני ממוקד, אנזים ENO1