Clear Sky Science · he
הפוספטאז Shp1 בוויסות יציבות חלבון CXCR2 ובהסתגלות פולשנית מתווכת IL8 בסרטן השד
מדוע מחקר זה חשוב לסרטן השד
סרטן השד נשאר אחת הסיבות המובילות למוות ממחלת הסרטן בנשים, בעיקר כי גידולים מסוימים הופכים לפולשניים ומתפשטים לאיברים מרוחקים. מחקר זה מפרק כיצד אות דלקתי שכיח בגידולים, הנקרא IL8, מתקשר עם תאי סרטן השד וכיצד "בלם" מולקולרי בשם Shp1 מסייע להכריע האם תאים אלה נשארים במקום או הופכים לאגרסיביים יותר. הבנת המשיכה־ולמבנה המולקולרי הזה עשויה לפתוח דרכים חדשות להאטה או עצירה של התפשטות סגנונות סרטן קשים לטיפול, במיוחד סרטן השד המשולש־שלילי.
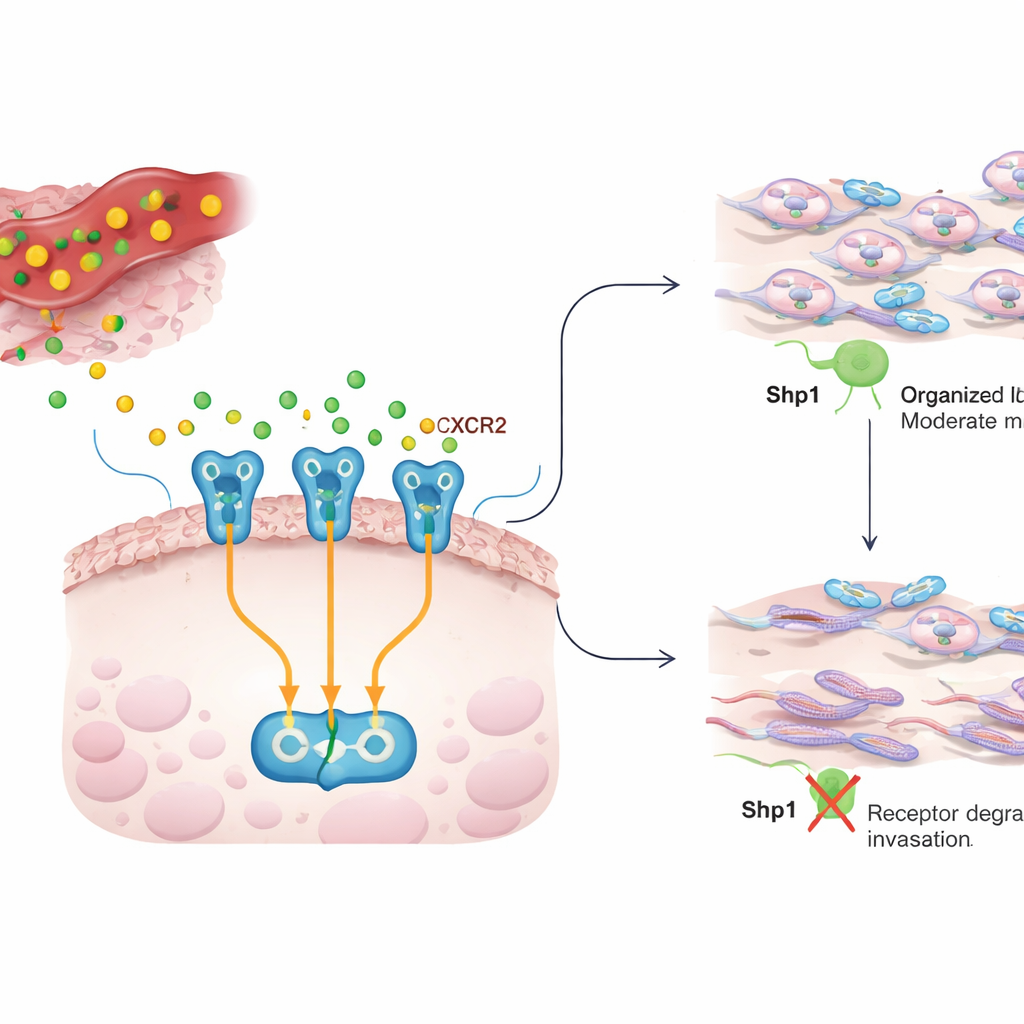
שיחה בין דלקת לתאי הסרטן
בתוך הגידול, תאי הסרטן מוקפים בתאי חיסון ותאים תומכים שמפרישים מוליכים כימיים, או ציטוקינים. IL8 הוא אחד מהמוליכים הללו ונמצא לעתים קרובות ברמות גבוהות בהרבה סוגי סרטן, שם הוא מאפשר צמיחה, היווצרות כלי דם ויכולת של תאי הסרטן לנוע ולחדור רקמות. IL8 משדר דרך קולטן על פני התא הנקרא CXCR2. כש‑IL8 נקשר ל‑CXCR2, מופעלים מספר מעגלים פנימיים שמארגנים מחדש את שלד התא, ועוזרים לתאים לזחול דרך רקמה ולהתפשט. העבודה הנוכחית שואלת כיצד נשמרת השליטה בשיחה הזו בין IL8 ל‑CXCR2, והאם Shp1 — אנזים שלרוב נתפס כבלם מדכא גידול לאותות גדילה — מעצב גם את ההתנהגות הפולשנית הזו.
תפקידו החבוי של Shp1 בתנועת התאים
החוקרים הסירו או חסמו כימית את Shp1 בקו תאי סרטן שד לומינלי נפוץ (MCF7) ומדדו עד כמה התאים מסוגלים לנוע ולחדור דרך ג'ל המדמה רקמה. בהעדר Shp1, התאים סגרו פצעים מהר יותר ונדחסו דרך הג'ל פי שניים עד שלושה ביעילות רבה יותר, מה שמראה כי Shp1 בדרך כלל מעכב תנועה. תוך שימוש בנתוני חולים, הם גם מצאו שנשים שלגידוליהן יש ביטוי נמוך יותר של Shp1 שרדו פחות זמן וחוו חזרה מוקדמת יותר של המחלה. ביחד, התוצאות מרמזות כי Shp1 מגביל את ההתנהגות האגרסיבית של תאי סרטן השד וכי אובדן הבלם הזה קשור לתוצאים גרועים יותר.
כיצד IL8 מדליק את המתג של Shp1 ומתכנת מחדש קולטן מרכזי
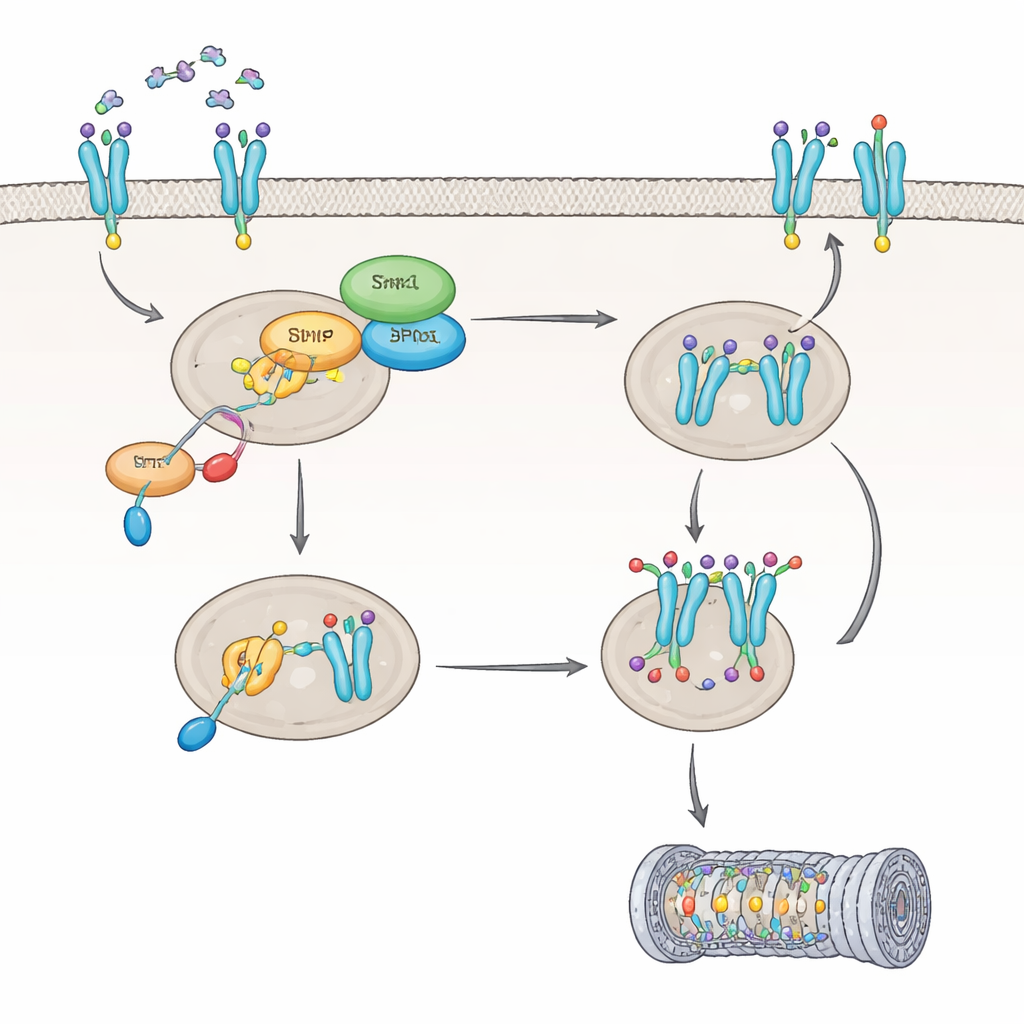
לאחר מכן הצוות חקר כיצד IL8 משפיע על Shp1 עצמו. הם גילו ש‑IL8 מפעיל חלבון בשם PKC, שמסמן את Shp1 באתר ספציפי, ומוריד את פעילותו האנזימטית בכ‑כ‑60 אחוז. כאשר Shp1 מושתק בדרך זו, אנזים אחר, PP2A, הופך לפחות פעיל, וקולטן CXCR2 נשאר במצב מנוצל מאוד שמשנה את גורלו בתוך התא. במקום להיות מנוקה וממוחזר חזרה למשטח התא, CXCR2 מסומן להשמדה, בעיקר דרך מערכת פירוק החלבונים של התא — הפרוטאוזום. שינוי מסוים על CXCR2, בחומצת אמינו שנקראת Ser347, התברר כחיוני לצירוף תגים אלה של פירוק. בתאים חסרי Shp1, CXCR2 סומן יותר ושבר מהר יותר, מה שהוביל לפחות קולטנים על פני המשטח ותגובה מוחלשת ל‑IL8 לאורך זמן.
סוגי סרטן שד שונים, חיבורים שונים
סרטן השד אינו מחלה אחת; הגידולים מקובצים לתת‑סוגים לומינלי, חיובי HER2, ומשולש‑שלילי על סמך דפוסי הקולטן שלהם. החוקרים בדקו את מעגל ה‑IL8–CXCR2–Shp1 בכמה קווי תאים המייצגים כל תת‑סוג. בתאים לומינליים ומשולש‑שליליים, IL8 הפעיל את קסקדת Shp1–PP2A–CXCR2, וחסימת Shp1 העלתה את הפולשנות הבסיסית וביטלה את ההשפעה הפרו‑פולשנית הטיפוסית של IL8. לעומת זאת, בתאים חיוביים ל‑HER2 הם עדיין הגיבו ל‑IL8, אך חסימת Shp1 כמעט ולא שינתה את התנהגותם, מה שמעיד שבגידולים אלה Shp1 מעורב באותות אחרים כגון HER2 ופחות זמין לוויסות CXCR2. ניתוחי ביטוי גנים בקנה מידה גדול תמכו בתמונה זו: קווי משולש‑שליליים נטו להראות רמות Shp1 נמוכות יותר, שינויים באותות הקשורים ל‑GPCR ורמות IL8 גבוהות יותר, תואם לפרופיל דלקתי אגרסיבי יותר.
משמעות הדבר לטיפולים עתידיים
ללא רקע מקצועי, המסר המרכזי הוא שהאנזים Shp1 משמש כבודק תנועה עבור קולטן ה‑IL8, CXCR2, וקובע האם הקולטן ממוחזר או נהרס ובהתאם כמה חזק תאי סרטן השד יגיבו לרמזים דלקתיים. בסוגי סרטן השד הלומינלי והמשולש‑שלילי, נקודת בקרה זו נראית חשובה במיוחד: כאשר רמות Shp1 נמוכות או פעילותו נחסמת, התאים נעשים פולשניים יותר ותוצאת המטופלים מחמירה. מאחר שניתן להגביר או למתן את Shp1 בעזרת תרופות קיימות מסוימות, מיקוד ציר Shp1–CXCR2, אולי בשילוב חסמי IL8 או CXCR2, עשוי להציע אסטרטגיה חדשה להגבלת חדירה ומטסטזות בתתי‑סוגים אגרסיביים של סרטן השד.
ציטוט: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
מילות מפתח: חדירת סרטן השד, אותות IL8, קולטן CXCR2, פוספטאז Shp1, סרטן השד המשולש־שלילי