Clear Sky Science · he
גורם שעתוק ZMYM3 מקדם גרורות בסרטן הכבד על-ידי העלאת CTTN ועידוד יצירת אינדופודיה
למה מחקר הסרטן הזה בכבד חשוב
סרטן הכבד הוא אחד הסרטנים הקטלניים ביותר בעולם, בעיקר מפני שהוא לעיתים קרובות מאובחן בשלב מאוחר ונוטה להתפשט. המחקר בוחן ברזולוציה תאית ובמבט לגרעין התא שאלה מהותית: מה גורם לגידולי כבד מסוימים להתנתק ולהחדיר חלקים אחרים של הגוף ביעילות כה גבוהה? על-ידי גילוי מנגנון מולקולרי מרכזי שמניע את התפשטות זו, המחקר מצביע על דרכים חדשות שבעתיד עשויות לסייע לרופאים לחזות אילו מטופלים נמצאים בסיכון הגבוה ביותר ולעצב טיפולים שיעצרו או יאיטי את היווצרות הגרורות.
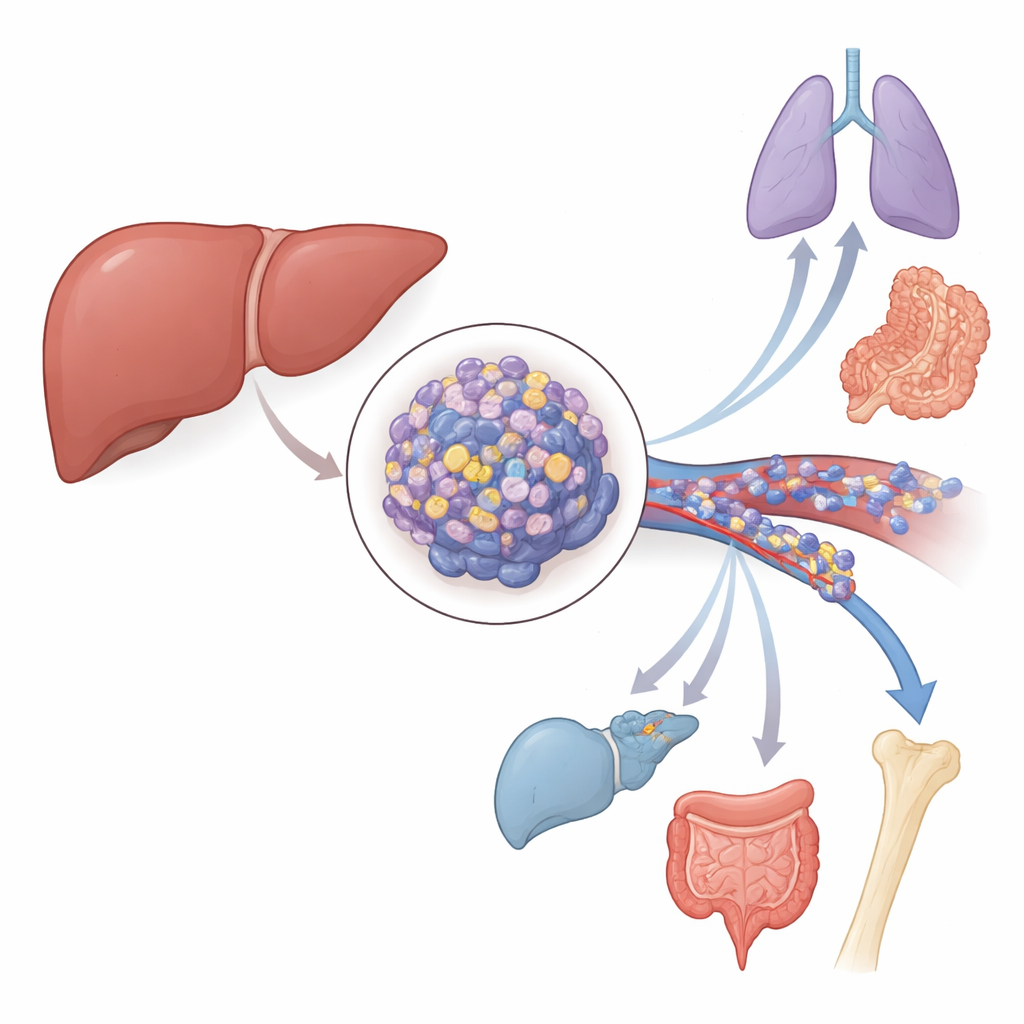
מצבר פנימי נסתר בתוך גידולי הכבד
החוקרים התרכזו בקרצינומה הפוקאלית של הכבד (hepatocellular carcinoma), הסוג השכיח ביותר של סרטן ראשוני בכבד. בניתוח מאגרי נתונים ציבוריים רחבי היקף ובמבחן של דגימות רקמה של מטופלים, הם מצאו כי הגן ZMYM3 דלוק בעוצמה רבה יותר בגידולים מאשר ברקמת הכבד הבריאה הסמוכה. מטופלים שהגידולים שלהם הפגינו רמות גבוהות של ZMYM3 נטו להישרדות כוללת נמוכה יותר ולתקופות חופשיות ממחלה קצרות יותר. הצוות בחן גם קרשי דם מיוחדים (טרומבים) שנוצרו מתאי הגידול בכלי הדם הטרלי (הווריד השערי), כלי דם מרכזי מנקז את הכבד. בטרומבים אלו, שקשרו לפוטנציאל חדירה גבוה, רמות ZMYM3 היו אף גבוהות יותר מאשר בגידולים הראשוניים, מה שמקשר את הגן ישירות ליכולת הסרטן לחדור לכלי דם ולהתפשט.
איך ZMYM3 הופך תאי סרטן לאגרסיביים יותר
כדי להתקדם מעבר למקושרים סטטיסטיים, המדענים שינו את רמות ZMYM3 בקווי תאי סרטן כבד. כאשר הורידו את ZMYM3, התאים גדלו לאט יותר, יצרו פחות מושבות והיו בעלי סבירות גבוהה יותר לעבור תכנות מוות תאי (אפופטוזה). כאשר הגבירו את ZMYM3, הופיע ההיפוכוּת: תאים התחלקו מהר יותר, התנגדו למוות והיו טובים יותר בנודדות ובחדירה דרך מחסומים מלאכותיים במעבדה. במודלים עכבריים, גידולים מהונדסים עם רמות מוגברות של ZMYM3 גדלו גדולים יותר מתחת לעור ויצרו יותר נקודות גרורה בריאות לאחר הזרקה למחזור הדם. יחד, הניסויים הללו מראים ש-ZMYM3 אינו רק סימן אלא מקדם פעיל של גדילה והתפשטות סרטן הכבד.
חדירה בעזרת "רגליים" זעירות
מאפיין בולט של תאים ממאירים אגרסיביים הוא יכולתם לגדל בליטות זעירות עשירות באקטין שחודרות וממוססות את רקמת הסביבה. מבנים אלה, שנקראים אינדופודיה, פועלים כמו פטישים תאיים, ועוזרים לתאי הגידול לכרוס את הרשת התומכת שסביב האיברים ולהחליק לכלי הדם. באמצעות פרופיל ביטוי גנים, הדמיה של שלד התא ובדיקות פונקציונליות, החוקרים הראו כי ZMYM3 מגביר הפעלה של רבים מהגנים הקשורים לאינדופודיה ולתכנית שינוי צורה רחבה יותר המוכרת כהיפרקפלת אפיתליאלית–מזנכימלית (EMT), שמקנה לתאים ניידות גבוהה יותר. כאשר רמות ZMYM3 היו גבוהות, תאי סרטן הכבד יצרו יותר אינדופודיה ושחררו את התקשרויותיהם לשכנים; כאשר צמצמו את ZMYM3, המבנים וההתנהגויות החודרות הללו פחתו.
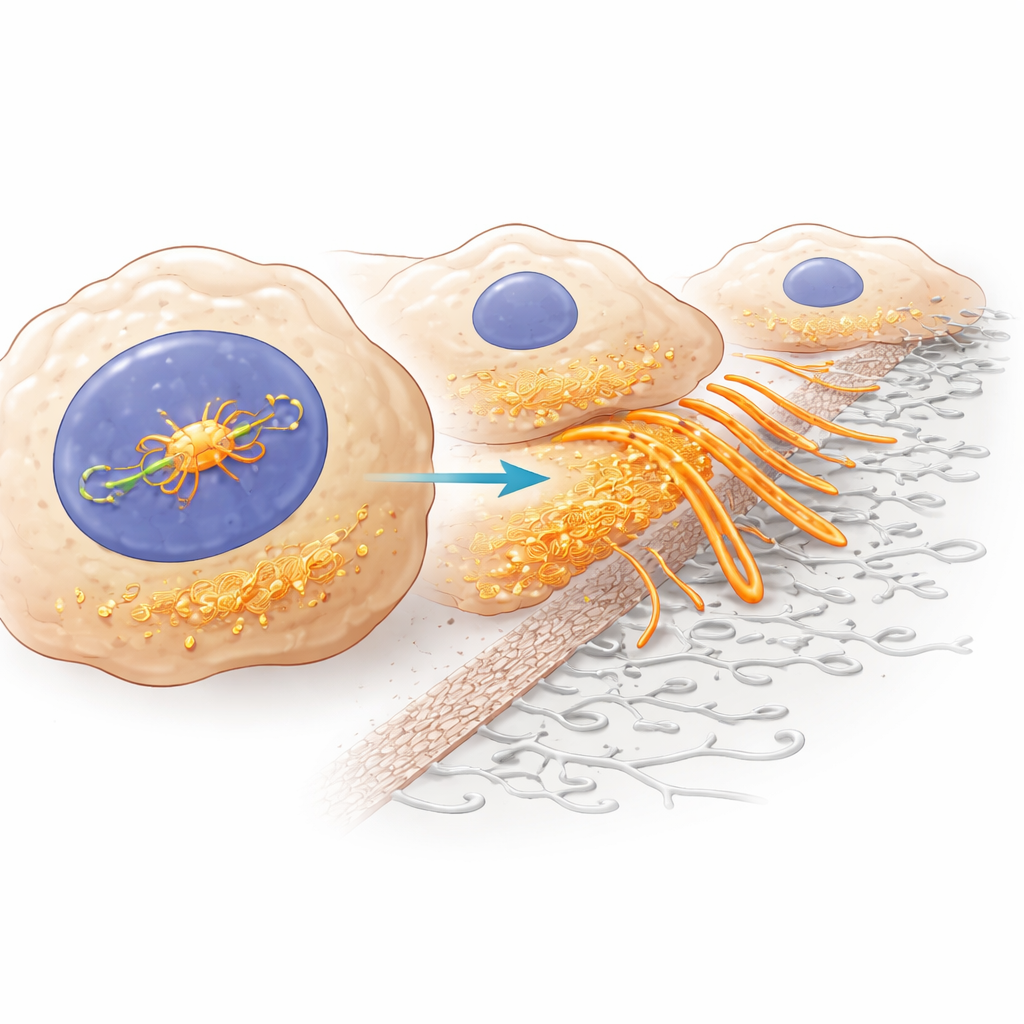
השותף המרכזי: חלבון מסגרת שנקרא קורטקטין
בהעמקה במנגנון, הצוות השתמש בטכניקה שממפה היכן חלבונים נקשרים ל-DNA ברחבי הגנום. הם גילו כי ZMYM3 נקשר ישירות לאזור הבקרה של גן אחר, CTTN, המקודד לקורטקטין — מאורגן מרכזי של האינדופודיה. הפעלת אזור זה מעלה את ייצור הקורטקטין. בנתוני מטופלים, קורטקטין גם הוא נצפה ברמות מוגברות בגידולי כבד וקושר לתוצאות גרועות, ורמותיו עלו וירדו בקורלציה עם ZMYM3. כאשר החוקרים השקו ירידה בקורטקטין בתאים שהיו מייצרים ZMYM3 בכמות מופרזת, תאי הסרטן איבדו חלק גדול מהצמיחה המוגברת, ההישרדות, הנדידה ויכולת החדירה שלהם. ממצא זה מצביע על כך שחלק ניכר מההשפעה של ZMYM3 מועבר דרך הגברת קורטקטין ובכך חיזוק האינדופודיה.
מה משמעות הדבר עבור מטופלים
באופן פשוט ובר-השגה, המסקנה היא שמחקר זה מזהה "מאיץ" מולקולרי — ZMYM3 — שעוזר לתאי סרטן הכבד לגדול, להתנגד למוות ולחפור את דרכם לכלי דם ולאיברים מרוחקים. הוא עושה זאת בעיקר על-ידי הדלקת גן נוסף, CTTN, שמצייד את התאים ב"רגליים" חודרות וחזקות יותר. מאחר שרמות גבוהות של ZMYM3 וקורטקטין מקושרות לחזרת המחלה ולהישרדות גרועה, הן יכולות לשמש כסימנים מזהירים לזיהוי מטופלים בסיכון גבוה יותר לגרורה. בטווח הארוך, תרופות שמפריעות לציר ZMYM3–קורטקטין, או לעצירת יצירת אינדופודיה עצמה, עשויות להציע דרכים חדשות להאט את התפשטות הקרצינומה ההפטוציאלית ולשפר תוצאות.
ציטוט: Zeng, F., Zhang, Z., Hu, T. et al. Transcriptional factor ZMYM3 promotes hepatocellular carcinoma metastasis by upregulating CTTN and inducing invadopodia formation. Cell Death Dis 17, 294 (2026). https://doi.org/10.1038/s41419-026-08506-6
מילות מפתח: סרטן כבד, גרורות, ZMYM3, קורטקטין, אינדופודיה