Clear Sky Science · he
אותות ROR1-PI3K/AKT מניעים עמידות מותאמת לחסימת מחזור התא בסרטן השחלות עם מוטציות ב-TP53
מדוע המחקר הזה חשוב לבריאות נשים
סרטן השחלות הוא אחד הסרטנים הקטלניים ביותר בנשים, במידה רבה מאחר שהגידולים לעיתים קרובות מפתחים עמידות לכימותרפיה. המחקר הזה שואל שאלה קריטית: כאשר תרופות חזקות נועדו לדחוף תאי סרטן לטעויות חלוקה קטלניות, כיצד עדיין תאים אלה מוצאים דרכים לשרוד, והאם נתיב ההימלטות הזה עצמו יכול להפוך לנקודת תורפה? על ידי מעקב אחרי תאי סרטן השחלות במשך שבועות עד חודשים של טיפול, החוקרים חושפים מערכת בקרה מרכזית בתוך התאים שמחליטה האם להמשיך להתחלק או להסתגר ולתקן נזק — ומגלים דרך חדשה לתקוף גידולים שכבר למדו לעמוד בפני תרופות סטנדרטיות. 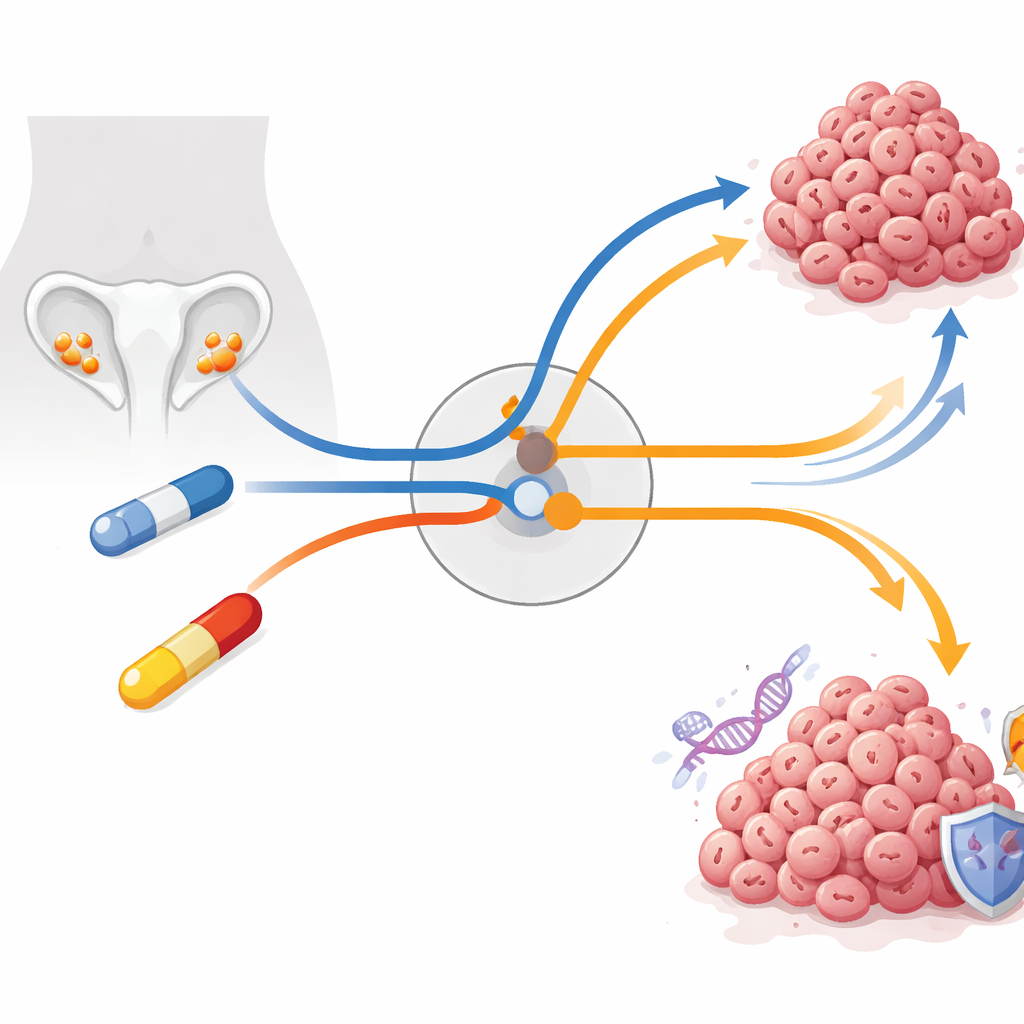
שתי תרופות נפוצות, נתיב הימלטות משותף
הצוות התמקד בקרצינומה סרוזית בדרגה גבוהה של השחלה, הצורה האגרסיבית והנפוצה ביותר של המחלה, שלרוב נושאת מוטציות בגן ה"שומר הגנום" TP53. מכיוון ש-TP53 פגום, גידולים אלה תלויים בצורה יוצאת דופן בבקרות מאוחרות יותר במחזור התא. שתי תרופות הנמצאות בשימוש נרחב או בבחינה בהקשר זה מנצלות חולשה זו: adavosertib, מעכב WEE1 הניסיוני שמדחיק תאים פגועים לחלקה מוקדמת, ו-paclitaxel, כימותרפיה מרכזית שמקפיאה את השלד הפנימי הנדרש להפרדת הכרומוזומים. בתיאוריה, שתיהן אמורות להוביל את תאי הסרטן ל"קטסטרופת מיטוזה" — כשל חלוקה קטלני. ובכל זאת, במרפאה ובמעבדה, הגידולים מסתגלים לעתים קרובות. החוקרים יצרו מודלים של תאים עמידים לטווח ארוך על ידי העלאת מינונים לאט במשך חודשים, אשר מדמה טוב יותר את מה שקורה בחולים מאשר ניסויים קצרים במינונים גבוהים.
כיצד תאי סרטן משנים את עצמם כדי לשרוד
באמצעות הדמיה מתקדמת ו"צביעת תאים" (Cell Painting) — טכניקה שמצבעת מבנים תאיים רבים בו זמנית — המדענים ראו שהתאים העמידים לא פשוט נראו כמו בעבר. רבים מהם הכילו גרעינים מרובים, שלד פנימי משופר, והפכו לצבירים צפופים יותר ולספירואידים תלת־ממדיים קטנים ומפוזרים יותר, סימנים של שינוי צורה חלקי הידוע כהמרת אפיתל–מזנכימה. שינויים פיזיים אלה רמזו שהתאים חיברו מחדש את הדרכים שבהן הם נעים, מתחלקים ומתקשרים. במקביל, רצפי RNA חד־תאיים מפורטים הראו שכל תרופה וקו תאים פיתחו דפוס משלהם של גנים וכרומוזומים ששונו. על אף המגוון הגנטי הזה, עלה נושא עקבי: פעילות של מסלול גדילה והישרדות שמתרכז ב-PI3K ו-AKT עלתה במודלים העמידים, לעתים בליווי מסלולי איתות קשורים כגון MAPK ו-NF-κB.
מתג תאי בין "עקיפה מהירה" ל"תיקון איטי"
בחקירה מעמיקה יותר, החוקרים מצאו שמערכת PI3K/AKT פועלת כמתג שמחליף את תאי הסרטן בין שתי אסטרטגיות הישרדות. במצב "עקיפה מהירה", פעילות גבוהה של PI3K/AKT מכבה את החלבון הבלם FOXO3 ומחלישה את נקודות הבקרה של מחזור התא, מה מאפשר לתאים להמשיך להתחלק ולהתחמק מהשפעות קטלניות של adavosertib או paclitaxel. במצב מנוגד של "תיקון איטי", פעילות PI3K/AKT נמוכה יותר, FOXO3 נשאר פעיל בגרעין, והתאים מאטים את שכפולם, מפעילים תוכניות תיקון DNA ומשפרים יציאת תרופות. באופן מרשים, חשיפה קצרה מוקדמת לתרופות עוררה שחרור חד של פעילות PI3K/AKT בכל המודלים; עמידות לטווח ארוך אז התייצבה לאחד משני המצבִים — עקיפה מהירה או תיקון איטי — בהתאם לרקע הגנטי של הסרטן ולאיתות הקודם. זה מראה שהמרכז האותי הזה יכול לתמוך בדרכי הימלטות שונות מאוד.
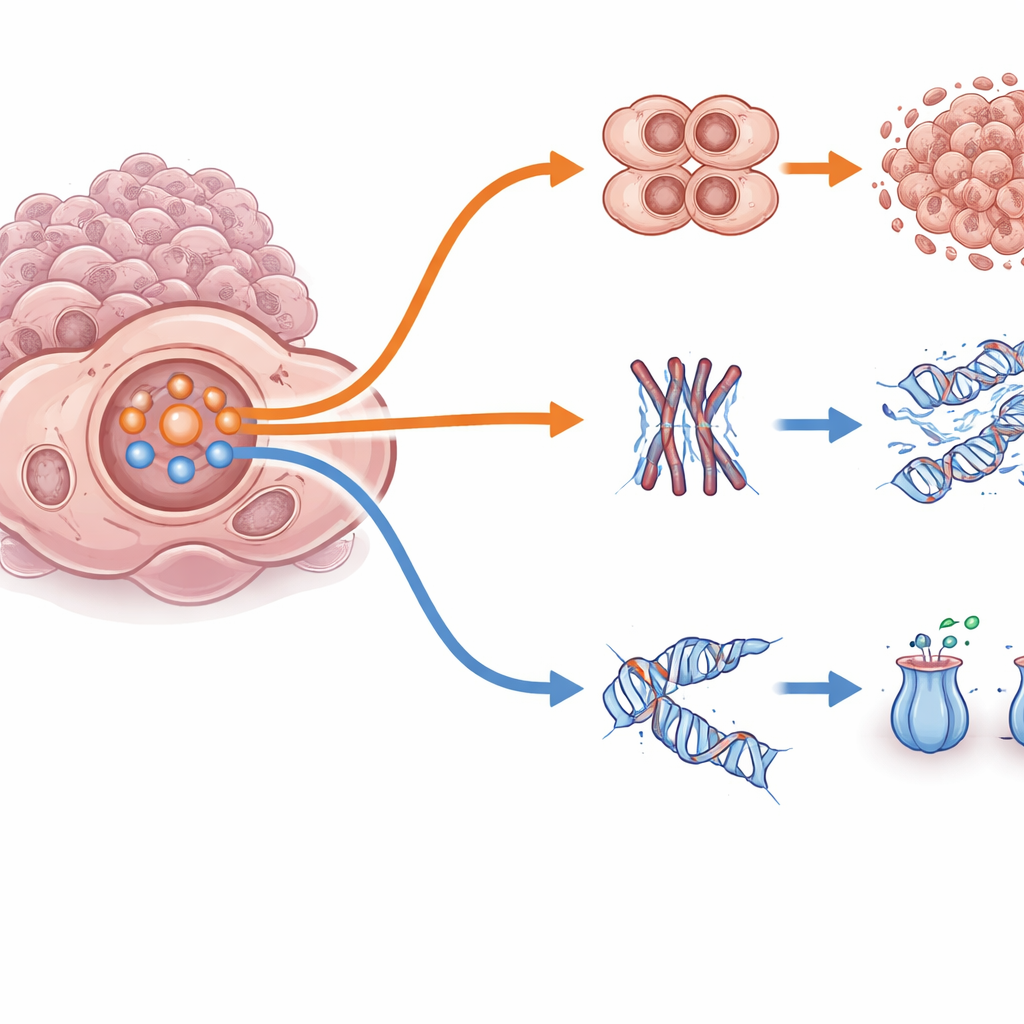
הפיכת אות עמידות למטרה טיפולית
שחקן על־זרם מרכזי במרכז הזה הוא ROR1, חלבון קולטן שבדרך כלל נדיר ברקמות בוגרות תקינות אך מוגבר בכמה סוגי סרטן. במודלים רבים של סרטן שחלות עמיד, רמות ROR1 עלו לצד פעילות PI3K/AKT. הצוות הראה כי כוונון של ROR1 כלפי מעלה או מטה יכול לשנות עד כמה תאים רוכשים עמידות ל-adavosertib או paclitaxel, בדרך התלויה בהקשר. החשוב מכל — הם בחנו את zilovertamab-vedotin, קונזוגט של נוגדן-תרופה המגיע עד ל-ROR1 ומעביר מטען רעיל. בקווי תאים ובאורגנואידים תלת־ממדיים ממקור מטופלים, גידולים עם ROR1 גבוה ועמידות ל-adavosertib היו פגיעים במיוחד לסוכן זה, ושילובו עם adavosertib לעתים הגביר את ההרג התאי. חלק ממודלים עמידים ל-paclitaxel היו פחות רגישים, ככל הנראה משום שחיזקו גם את יכולתם להוציא תרופות.
מה משמעות הדבר לטיפול עתידי בסרטן השחלות
עבודה זו מנסחת מחדש את נושא העמידות לתרופות בסרטן השחלה עם מוטציות ב-TP53 — לא כאירוע אקראי אלא כתשובה מתואמת הנשלטת על ידי מתג איתות מרכזי. בזיהוי ציר PI3K/AKT–FOXO3 ו-ROR1 כקשרים מרכזיים, המחקר מצביע על אסטרטגיות פרקטיות: לשלב תרופות המכוונות מיטוזה כמו adavosertib ו-paclitaxel עם טיפולים שחוסמים את מרכז העמידות או מנצלים את ROR1 על תאים עמידים. מאחר ש-ROR1 נעדר ברוב הרקמות הבריאות, שילובים כאלה עשויים לתקוף בצורה סלקטיבית גידולים חוזרים וחסינים לתרופות תוך שמירה על תאים נורמליים. למרות שתוצאות אלה מבוססות על מודלים מעבדתיים ותרביות מטופלים ולא על ניסויים קליניים הושלמו, הן מציעות מפת דרכים ברורה לתכנון טיפולים חכמים ועמידים יותר לנשים המתמודדות עם קרצינומה סרוזית בדרגה גבוהה של השחלה.
ציטוט: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
מילות מפתח: סרטן השחלות, עמידות לתרופות, מסלול PI3K AKT, תרפיית נוגדן נגד ROR1, מעכבי מחזור התא