Clear Sky Science · he
דיכוי אוטופגיה מונע על ידי mTOR מגדיר פגיעות מטבולית בסרטן השד HR+/HER2− העמיד ל־CDK4/6
מדוע זה חשוב לחולות סרטן השד
נשים רבות עם סרטן שד מתקדם חיות כיום זמן רב יותר הודות לתרופות שנקראות מעכבי CDK4/6, שמאטות את קצב חלוקת התאים הסרטניים. לצערנו, רוב הגידולים בסופו של דבר לומדים להתחמק מהתרופות הללו. המחקר שואל שאלה תקווה: כאשר סרטן השד הופך לעמיד למעכבי CDK4/6, האם הוא מפתח חולשה חדשה שיכולים רופאים לנצל בעזרת תרופות מטבוליות קיימות ופשוטות יחסית, כמו מטפורמין או דיכלורואצטט (DCA)?
כאשר תרופות שמכוונות את מחזור התא מפסיקות לעבוד
רופאים מטפלים לעתים קרובות בסוג השכיח ביותר של סרטן השד — מחלה חיובית לקולטן הורמונלי ושלילית ל‑HER2 — בעזרת טיפול הורמונלי יחד עם מעכבי CDK4/6 כמו פאלבוסיצליב או ריבוציצליב. תרופות אלה פוגעות בחלבונים שמניעים את התאים בחלוקת התא. עם הזמן, עם זאת, תאים סרטניים מסוימים מסתגלים והופכים לעמידים מאוד, וממשיכים לגדול גם בנוכחות מינונים גבוהים של התרופות. החוקרים שיחזרו בעיה זו במעבדה על‑ידי חשיפת גידולי שד בתרבית (T47D ו‑MCF7) לכמויות הולכות וגדלות של מעכבי CDK4/6. הם הגיעו לשתי קבוצות של שורדים: תאים בעלי עמידות חלקית וקבוצה קטנה יותר של קלונים עמידים מאוד שלא הגיבו יותר לטיפול.
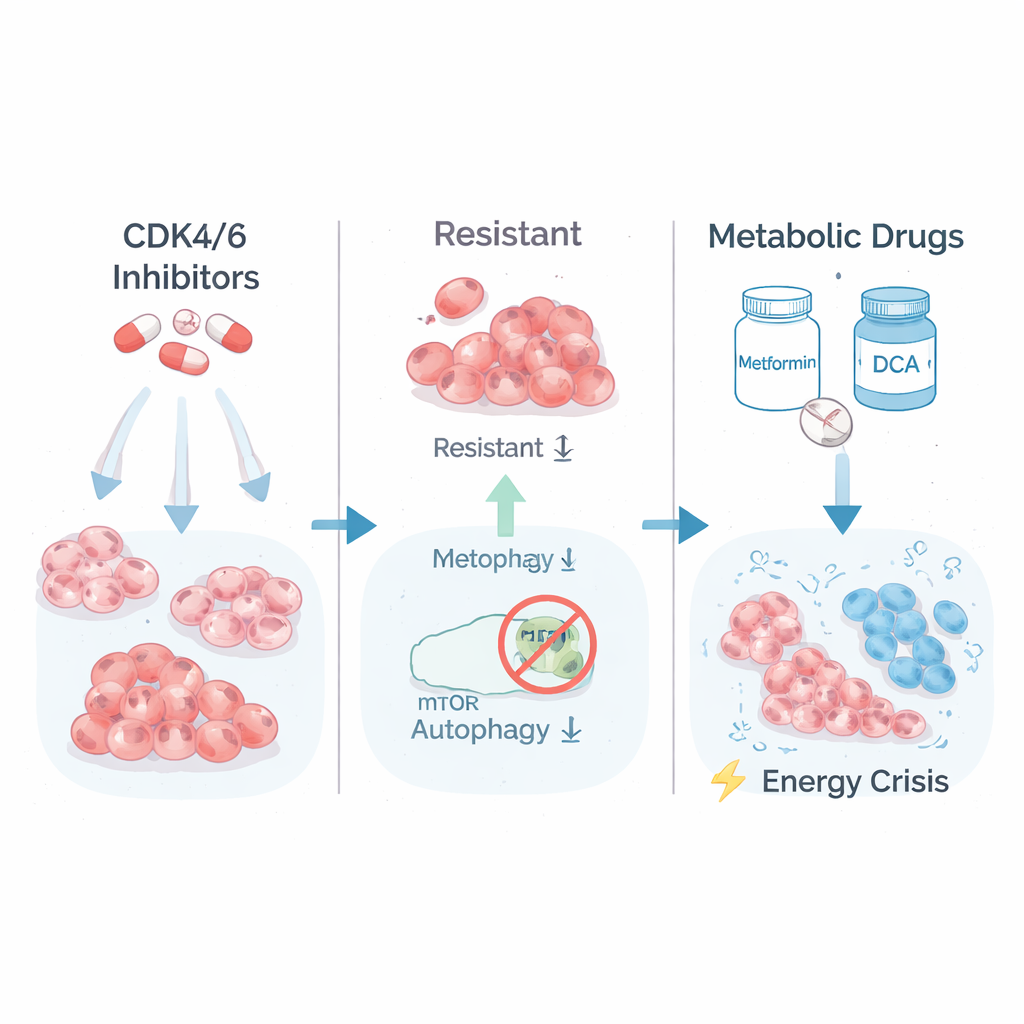
חולשה נסתרת בשימוש האנרגיה של הגידול
כדי להבין מה הבדיל את התאים העמידים מאוד, הצוות בדק אילו גנים הופעלו או דוכאו. הם מצאו שהתאים העמידים ביותר הגבירו מסלולים המעורבים בשריפת סוכר (גליקוליזה) ובאותות גדילה המווסתים על‑ידי קומפלקס חלבוני שנקרא mTORC1. במילים אחרות, תאים אלה חיו בקצב גבוה, בוערים דלק בקצב מהיר כדי להמשיך לגדול. החוקרים לאחר מכן בדקו האם מטבוליזם "באגז מלא" זה יכול להסתובב כנגד התאים. הם טיפלו בתאים העמידים ובתאים ההוריים במטפורמין, תרופה נפוצה לסוכרת שמלחיצה את תחנות האנרגיה של התא, ו‑DCA, שמכריחה תאים לעבד דלק ביעילות גבוהה יותר. באופן בולט, הקלונים העמידים ביותר הפכו לפגיעים ביותר: הצמיחה ארוכת הטווח שלהם בתרביות התמוטטה תחת הטיפול המטבולי, בעוד שהתאים ההוריים ותאים בעלי עמידות חלקית הושפעו הרבה פחות.
חסימת "ניקיון עצמי" והתמוטטות אנרגטית
מדוע תאי הבריחה האלה רגישים כל כך ללחץ אנרגטי? התשובה נמצאה בתהליך הישרדות בסיסי אחר: אוטופגיה, מערכת ה"מיחזור והניקיון" הפנימית של התא. בדרך כלל, כשהאנרגיה יורדת, תאים מפרקים וממיחזרים רכיבים פנימיים כדי להישאר בחיים. החוקרים הראו שבקלונים העמידים מאוד, mTORC1 היה פעילות יתר והטיל מעצור כימי על ULK1, שעתוק מפתח לאתחול האוטופגיה. באמצעות מבחן דיווח רגיש הראו שהם איבדו את היכולת להפעיל או להגביר אוטופגיה כראוי, אפילו כשדחפו אותם עם תרופות מטבוליות. כתוצאה מכך, מטפורמין ו‑DCA יצרו משבר אנרגיה חמור: חיישנים של אנרגיה נמוכה נדלקו, ייצור השומן הופסק וסמנים למוות תאי בלתי הפיך הופיעו, באופן ספציפי בתאים העמידים מאוד.
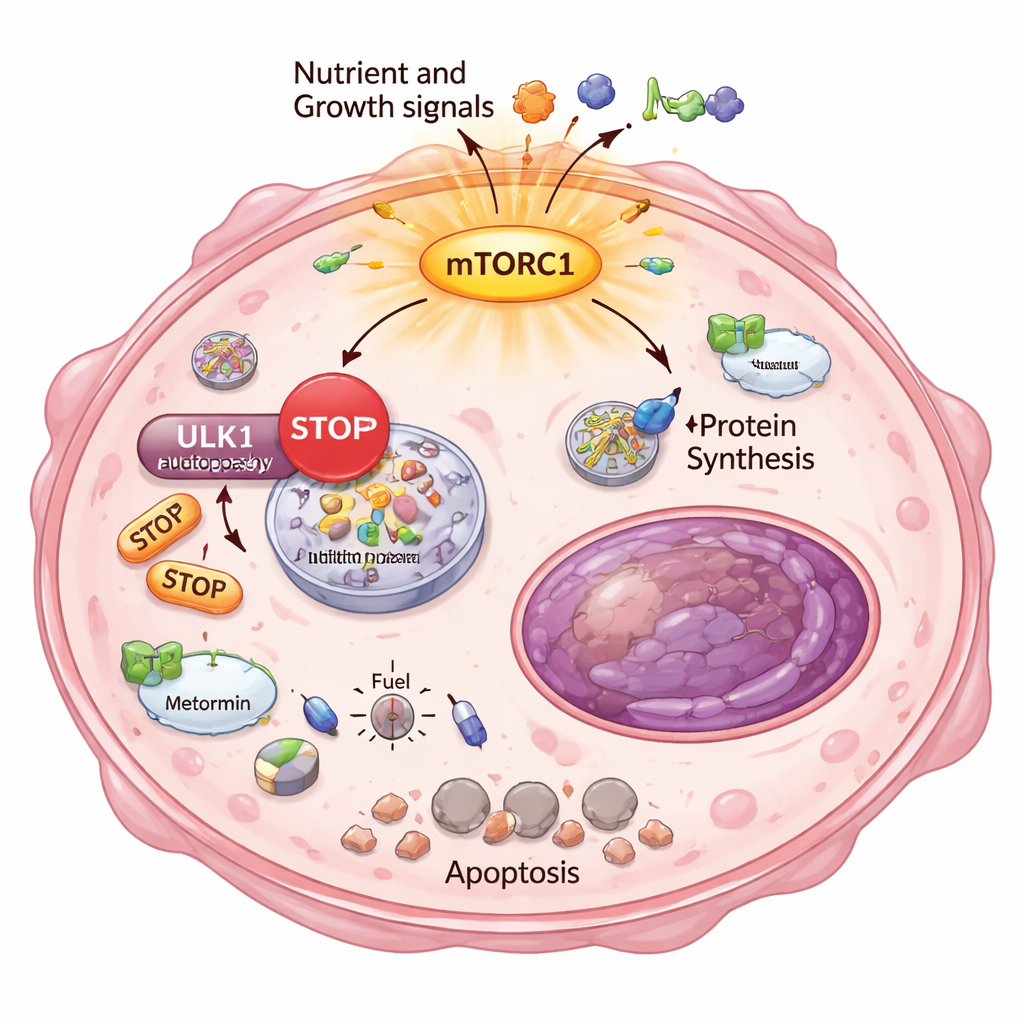
ראיות מתוך גידולים של מטופלות אמיתיות
מודלים מעבדתיים אינם תמיד משקפים את מה שקורה בחולות, לכן הצוות פנה לדגימות גידול של סרטן השד מהאדם. הם צבעו למעלה ממאה גידולים לסמן של פעילות mTORC1 (4E‑BP1 מזורחן) ול‑p62, חלבון שמצטבר כאשר האוטופגיה נחסמת. גידולים עם פעילות גבוהה של mTORC1 נטו להכיל יותר p62, מה שתומך ברעיון שתבנית של "אות גדילה מופרזת יחד עם מיחזור לקוי" קיימת בסרטן השד האמיתי, לא רק בשורות תאים. זה מצביע על כך שאחוז מסוים של מטופלות עשוי לשאת גידולים עם אותה חולשה מטבולית שנצפתה במעבדה.
מה זה יכול לעזור בטיפולים עתידיים
למי שאינו מומחה, המסר המרכזי הוא שכאשר סרטן השד מתפתח כדי להתחמק ממעכבי CDK4/6 רבי עוצמה, הוא עלול גם לצייר את עצמו לפינה מטבולית. על‑ידי הפעלה קבועה של אותות גדילה וכיבוי של המיחזור התאי, גידולים אלה הופכים תלויים מאוד באספקת אנרגיה קבועה. המחקר מראה שניתן לנצל תצורה זו בעזרת תרופות מטבוליות כמו מטפורמין ו‑DCA, שכבר ידועות היטב במחלות אחרות. חשוב להבין שהמחברים מציעים שמבחנים פשוטים רקמתיים לפעילות mTORC1 וסמנים של אוטופגיה יכולים לסייע לזהות חולות שהגידולים העמידים שלהן מוכנים לסוג זה של מתקפה מטבולית, ולקדם טיפולים מצילי‑אישיים אחרי כישלון מעכבי CDK4/6.
ציטוט: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
מילות מפתח: סרטן השד, עמידות למעכבי CDK4/6, mTOR, אוטופגיה, טיפול מטבולי