Clear Sky Science · he
HIF2α־מושרש ליזיל אוקסידאז מגן על היריון מוצלח על ידי עיצוב מחודש של קולגנים בממשק עוברי–אימהי
למה הרחם חייב להתכונן להגעת אורח חדש
לפני שהריון יכול להתבסס, העובר המוקדם חייב לבצע מעשה יוצא דופן: לשקוע בדופן הרחם ולבנות מערכת תמיכה—השלייה. מאמר זה בוחן כיצד רקמת האם מעצבת את עצמה באופן שקט כדי לקבל את העובר, ומתמקד באיך רמות חמצן נמוכות ובאנזים מעט מוכר מסייעים להכין את רירית הרחם. הבנת הריקוד המעודן הזה עשויה להסביר מדוע חלק מההריונות נכשלים בשלב מוקדם ולהציע דרכים חדשות למניעת בעיות פוריות וסיבוכי הריון.
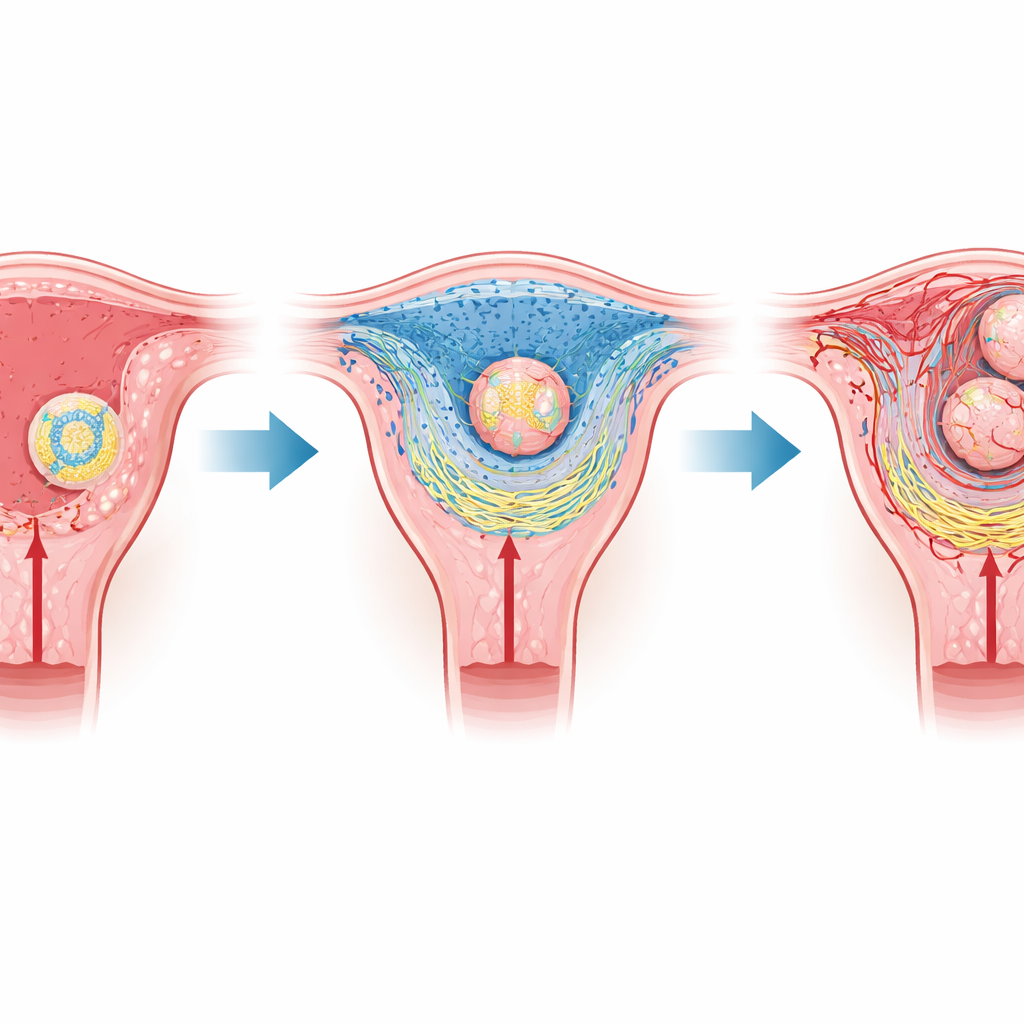
מפגש עדין בין אם לעובר
ביצורים יונקים כמו עכברים ובני אדם, השלב המוקדם של ההיריון תלוי בהשתרשות, כאשר העובר מתחבר ואז חודר לרירית הרחם. העובר עטוף בקליפה של תאים מיוחדים שיתפתחו מאוחר יותר לשלייה, בעוד רקמת האם משתנה לשכבה מרופדת הנקראת דצידה. הקרוב ביותר לעובר נמצא אזור דק הידוע כזון הדצידה הראשוני, אשר חסר כלי דם ולכן מכיל מעט חמצן. מחקרים קודמים הראו כי הכיס הטבעי בעל רמת החמצן הנמוכה מסייע להפעיל את ההשתרשות, אך לא היה ברור איך תנאי פיזי פשוט כזה יכול לארגן מחדש רקמות שלמות.
חמצן נמוך כמו מפסק חבוי
המחקר השתמש בטכניקה חזקה שנקראת טרנסקריפטומיקה מרחבית, שממפה פעילות גנים ישירות על חתכי רקמה, כדי לחקור רחמים של עכברים בימים שבהם העוברים מצמדים וחודרים. הם התמקדו בחלבון הנקרא HIF2α, הנדלק במצבי חמצון נמוך ופועל כמפסק גנטי. בעכברים תקינים, תאים באותו אזור של הדצידה הראשוני הראו פעילות חזקה של גנים הקשורים לחמצן נמוך ולבניית החומר התומך סביבם, כולל קולגנים היוצרים את המטריקס החוץ־תאי. כאשר HIF2α הוסר רק ברחם, סידור סוגי התאים נראה במבט כללי מפתיע כתקין. אך ברזולוציה גבוהה רשת הקולגן היתה מבולגנת, המשטח האפיתליאלי לא נפתח כראוי, ותאי העובר נאבקו לחדור לתוך רקמת האם.
אנזים שמצליב את השלד
בהעמקה, הצוות זיהה שחקן מרכזי במורד הזרם של HIF2α: ליזיל אוקסידאז, או Lox, אנזים שמגיב כימית לצלבים בסיבי הקולגן ועוזר להקשיח ולייצב את הרקמה. בהריונות תקינים, רמות Lox עלו באופן חד סביב העוברים בדיוק כשהם התחילו לחדור. ברחמים חסרי HIF2α, הביטוי של Lox ירד וסיבי הקולגן נראו מפורקים במקום ליצור רשת צפופה. כדי לבדוק את חשיבות Lox ישירות, החוקרים הנדסו עכברים שבהם Lox הוסר רק ברחם. נקבות אלה נכנסו להריון פחות לעתים, נשאו פחות עוברים, ולעתים קרובות הראו סימני אובדן עובר ודימומים בשלבים מאוחרים יותר של ההריון, אף על פי שהשלבים הראשוניים של הצמדות והעיבוי הרקמתי נראו בתחילה תקינים.
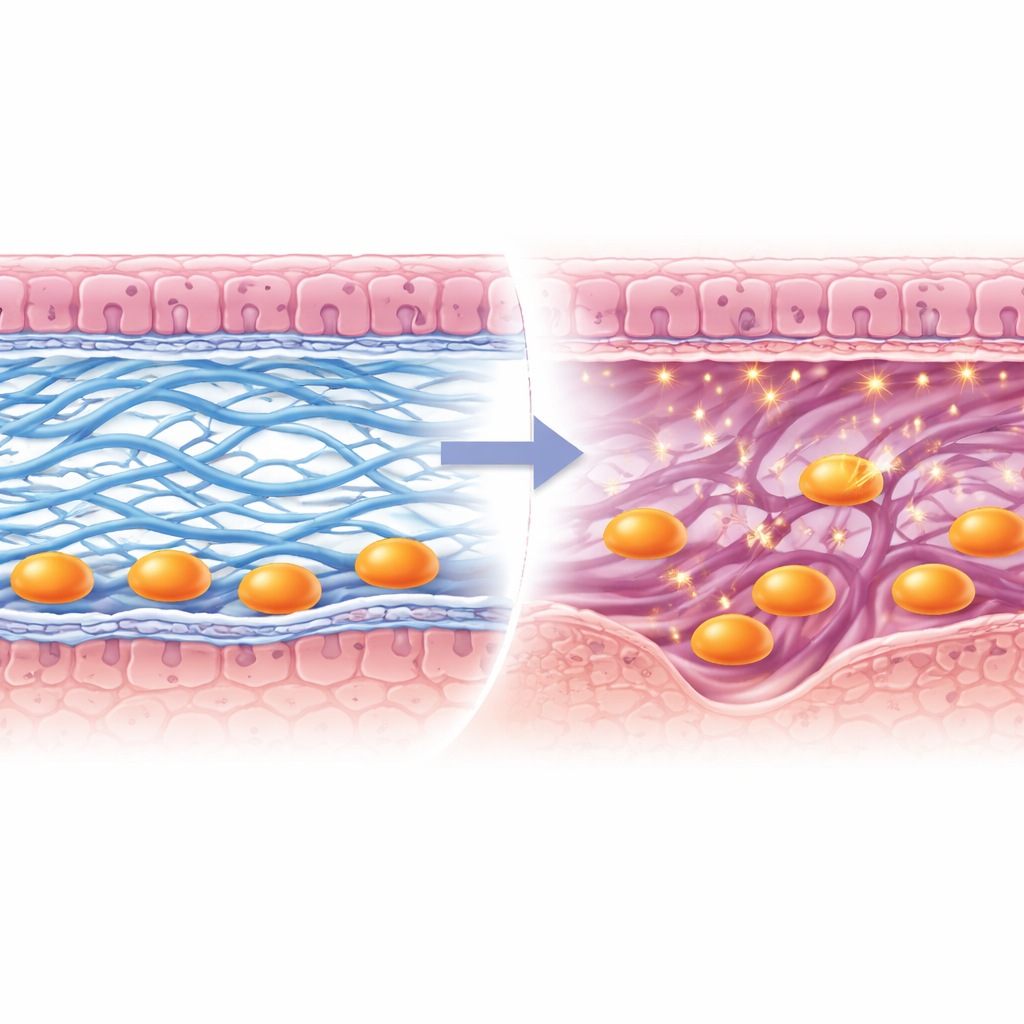
פתיחת מסלול עבור השלייה
דימות מדוקדק חשף מה השתבש כש־Lox נעדר. גיליון דק עשיר בחלבון הנקרא קרום בסיס (basement membrane), שלרוב נשבר כדי לאפשר לתאים העובריים לעבור, נותר במידה רבה שלם. סיבי קולגן מסוג I במטריקס שמתחתיו לא הצליחו ליצור צרורות רציפות וחזקות, בעוד קולגן מסוג IV בקרום הבסיס לא התאדה כראוי בקרבת התאים החודרים. כתוצאה מכך, תאי הטורופובלסט—חלוצים שמקורם בעובר ובונים את השלייה—נשארו כלואים על פני השטח במקום לחפור אל תוך שכבת האם. הצוות גם מצא שאנזים החותך קולגן, Mmp9, לא הוכרז בתאים אלה של הטורופובלסט, מה שהקשה עוד על התקדמותם. עם הזמן, מבני השלייה נוצרו לקוי, העוברים גדלו באופן חריג, והצלחת ההיריון ירדה.
מה משמעות הדבר לבריאות ההיריון
בהרכבה משולבת, הממצאים מתארים סדרת אירועים שבה חמצן נמוך באזור ההשתרשות המוקדם מפעיל את HIF2α, שהוא בתורו מגביר את Lox. Lox מעצב ומצליב סיבי קולגן ועוזר לפרק את קרום הבסיס, בעוד הוא גם מאפשר לאנזימים כמו Mmp9 לפנות נתיב. עיצוב מחודש זה מספק הן תשתית מבנית והן פתחה פתוחה לתאי הטורופובלסט לחדור ולבנות את השלייה. עבור הקורא שאינו מומחה, המסר הוא שהיריון מוצלח תלוי לא רק בעוברים בריאים ובהורמונים אלא גם בעיצוב השקט של ארכיטקטורת רקמת האם. שיבושים בציר ההיפותוקסיה–HIF2α–Lox עשויים לעמוד בבסיס חלק מהמקרים של פוריות בלתי מוסברת, הפלות והפרעות הקשורות לחדירה לקויה של השלייה, ומציעים סימנים אבחוניים חדשים ומטרות טיפוליות לתמיכה בהריונות מוקדמים.
ציטוט: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
מילות מפתח: השתרשות העובר, מטריקס חוץ־תאי של הרחם, ליזיל אוקסידאז, חדירת טורופובלסט, התפתחות השלייה