Clear Sky Science · he
שימוש חוזר במערכת קובעת גורל במלנומה: מודולטורים של TRPM8 מעוררים אפופטוזה ומגבירים ציטוטוקסיות של תאי NK
מדוע להפנות "חיישן קור" נגד סרטן העור משנה את הכל
מלנומה היא צורה מסוכנת של סרטן העור שלעתים קרובות מפתחת עמידות לתרופות ומצליחה להתחמק ממערכת החיסון. המחקר הזה חוקר נקודת תורפה בלתי צפויה בתאי המלנומה: חלבון בשם TRPM8, מוכר בעיקר כחיישן המאפשר לתאי עצב לחוש קור או מנטול. החוקרים מראים שתרכובות מתוכננות בקפידה החוסמות את TRPM8 יכולות לדחוף תאי מלנומה להתאבדות מתוכננת ובמקביל להפוך אותם לפגיעים יותר לתקיפת תאי הקילר הטבעיים (NK). פעולה כפולה זו מצביעה על גישה חדשה לטיפול במלנומה עקשנית ומתקדמת.
מתג מוסתר על תאי המלנומה
על־ידי כריית מאגרי מידע גדולים של סרטן ובחינת תאי מלנומה שמקורם בחולים במעבדה, הצוות מצא ש-TRPM8 רב יותר במלנומה גרורתית בהשוואה לעור תקין, כולל מלנוציטים תקינים ופיברובלסטים דרמליים. באמצעות הדמיה הם הראו ש-TRPM8 נמצא הן על פני התא והן על ממברנות פנימיות, מה שממקם אותו בנקודות אסטרטגיות להשפעה על התנהגות התא. כשיישמו לוח של מולקולות החדשות המכוונות ל-TRPM8, שתי תרכובות (שנסמנו 4 ו-9) בלטו בעקביות: הן הקטינו באופן חזק את הישרדות תאי המלנומה לאורך זמן בעוד שתאי עור תקינים נשארו במידה רבה ללא פגע. בדיקות גנטיות אישרו שכש-TRPM8 הוסר, תרופות אלה איבדו את כוח ההרג שלהן, וכאשר ביטוי TRPM8 הוגבר, תאי המלנומה הפכו רגישים אף יותר — הוכחה שהאפקט תלוי בערוץ הספציפי הזה. 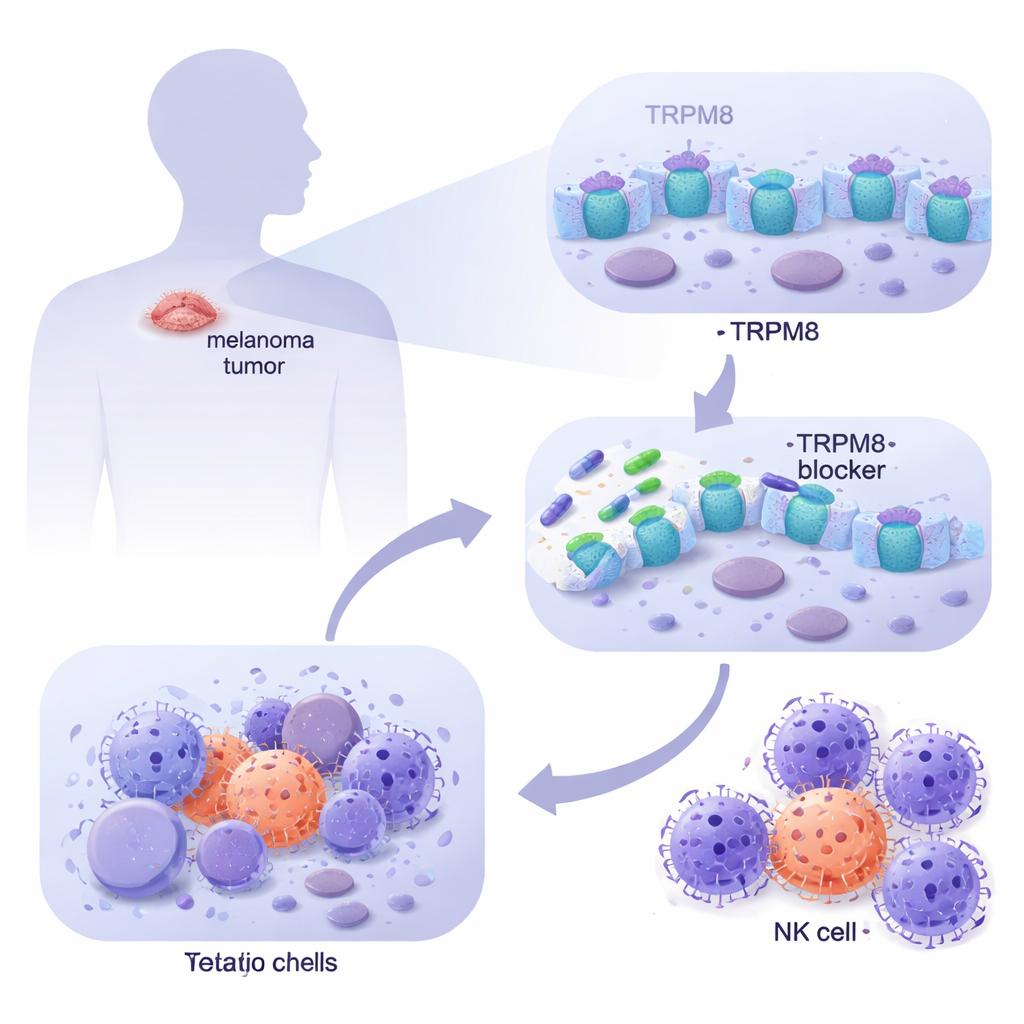
כפיית משבר אנרגיה בתאי הסרטן
בניגוד למפעילי TRPM8 קלאסיים כמו מנטול, שגורמים לעלייה בסידן בתוך התאים, החוסמים החדשים לא עוררו שינויי סידן. במקום זאת הם השיקו גל של לחץ חמצוני בתוך תאי המלנומה. התרכובות הגבוהו במהירות את רמות המולקולות המגיבות בחמצן, במיוחד בתוך המיטוכונדריות — מפעלי האנרגיה של התא. ההתפרצות החמצונית גרמה לאובדן המטען החשמלי במיטוכונדריה, לפיצול שלהן ולדליפה של ציטוכרום c, שלב מרכזי בהפעלה של תכנית ה"התאבדות" הפנימית של התא. נוגדי חמצון שסילקו מולקולות אלה הצילו במידה רבה את התאים, מה שמראה שאי־איזון חמצוני אינו תופעת לוואי אלא מנוע המוות. בהמשך, סמני מוות קלאסיים כגון הפעלת קאספאז-3 ושבירת PARP אישרו שהתאים עוברים אפופטוזה מתוכננת ולא נזק אקראי.
נטרול אותות הישרדות וה пробужת שומר
המכה החמצונית הרימה תגובת מתח רחבה יותר. התרופות הפעילו את ATM, חיישן לנזק בדנ"א, והובילו להצטברות ולהפעלה של p53, חלבון מדוכא גידולים מפורסם שמחליט אם תא פגוע יתוקן או ימות. במקביל, התרכובות החלישו אחד מנתיבי ההישרדות המרכזיים של המלנומה: מסלול PI3K–AKT. בדרך כלל TRPM8 מתקשר פיזית עם רכיבי PI3K כדי לסייע בשמירה על AKT בצורתו הפעילה המקדמת גדילה. לאחר הטיפול, שותפות זו נקרעה ופעילות AKT ירדה, מה שהטתה את המאזן אף יותר לכיוון מוות התא. חשוב לציין כי השינויים הללו היו בולטים בתאי מלנומה אך לא בתאים שאינם סרטניים, מה שמרמז על חלון טיפולי שבו הגידול נפגע בעוצמה בעוד רקמות בריאות נשמרות.
הפיכת הגידולים לגלויים יותר ל"כיתות חיסול" חיסוניות
הסכנה של המלנומה נובעת גם מיכולתה להתחמק ממעקב חיסוני. לכן החוקרים שאלו מה קורה לתאי הגידול ששרדו במינונים נמוכים של חוסמי TRPM8 לאורך זמן. הם גילו שהתאים הנותרים החלו להציג יותר סמן שטח הנקרא ULBP1, שמתפקד כדגל מצוקה שמזוהה על ידי קולטני NKG2D על תאי NK. דגלים קשורים אחרים לא השתנו, מה שמצביע על אפקט סלקטיבי. בכדורים תלת־ממדיים של מלנומה שמחקים טוב יותר גידולים אמיתיים, הטיפול המוקדם בחוסמי TRPM8 לא רק הקטין את המבנים והגביר את מוות התאים אלא גם עשה אותם פגיעים הרבה יותר לתקיפת תאי NK. כאשר ULBP1 או NKG2D נחסמו באמצעות נוגדנים, ההרג המוגבר נעלם ברובו, מה שמראה שהניקוי החיסוני המשופר נע דרך לחיצת היד הספציפית הזו בין הגידול לתאי NK. 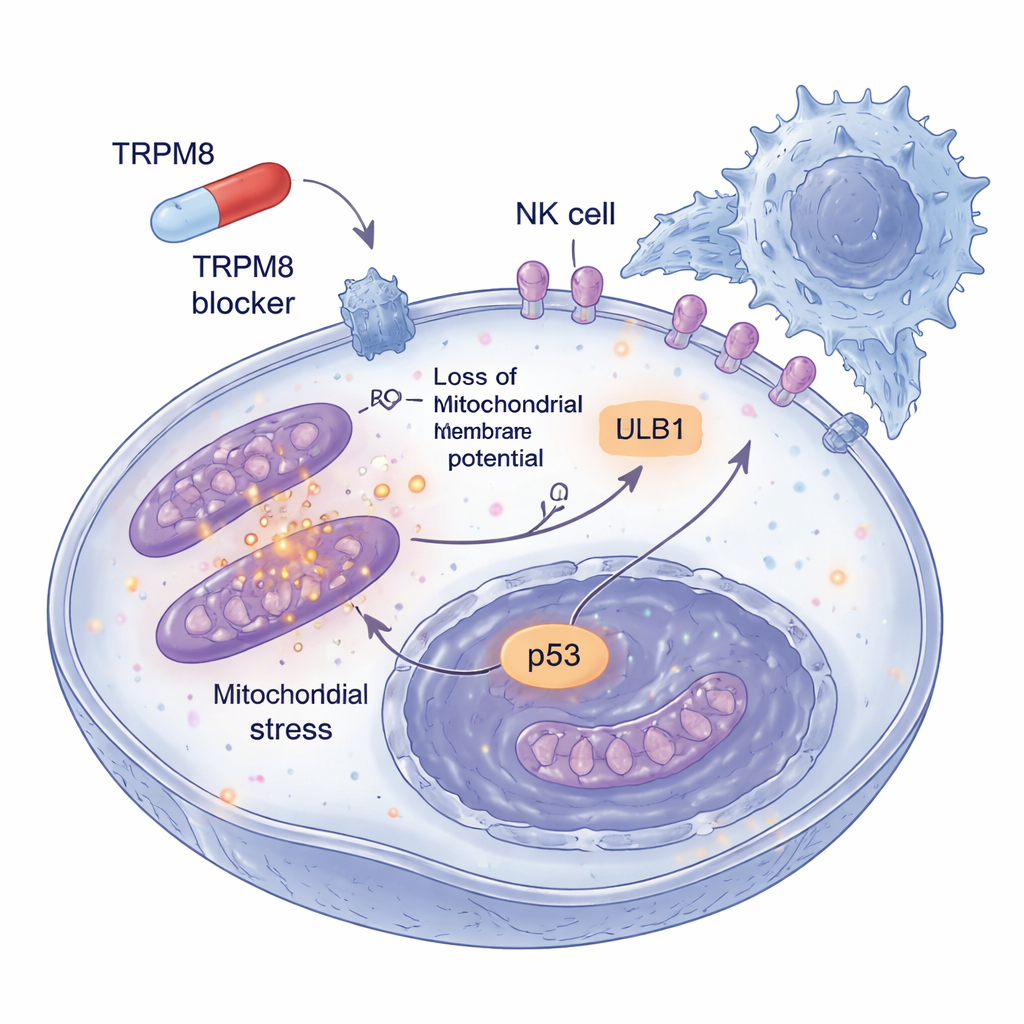
מה המשמעות של זה לטיפול עתידי במלנומה
במילים פשוטות, חסימת "חיישן הקור" TRPM8 הופכת אותו להילוך טיפולי: היא דוחפת תאי מלנומה למשבר מיטוכונדריאלי ודנ"א קטלני ובו־זמנית מסמנת אותם להשמדה על־ידי תאי NK. מאחר שהתרופות משאירות בחיים תאי עור תקינים ואינן מזיקות לתאי NK עצמם, הן מציעות בסיס מבטיח לטיפולים חדשים. המחברים מציעים שחוסמי TRPM8 יכולים להיות משולבים עם אימונותרפיות קיימות כדי לתקוף מלנומה עיקשת ועמידה בתרופות בשני חזיתות: להרוג תאי גידול ישירות ולהפוך את השורדים לקלים יותר לזיהוי ולהשמדה על ידי המערכת החיסונית.
ציטוט: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
מילות מפתח: מלנומה, TRPM8, מיטוכונדריה, לחץ חמצוני, תאי קילר טבעיים