Clear Sky Science · he
לַקטילציה מזרזת TRIM29 מעודדת התנהגות פולשנית ומטסטזות לבלוטות לימפה בסרטן הקיבה דרך מסלול Wnt/β-catenin מתווך על-ידי hnRNPA1
מדוע המחקר הזה חשוב
סרטן הקיבה הוא אחד הסרטנים הקטלניים בעולם בעיקר משום שהוא מתפשט מוקדם לבלוטות הלימפה הסמוכות, מה שהופך ריפוי באמצעות ניתוח לקשה. מחקר זה חושף כיצד שינוי כימי הקשור למטבוליזם של הגידול מייעל חלבון בשם TRIM29, ובכך מסייע לתאים הסרטניים לחדור לרקמות סמוכות, לייצר כלי לימפה חדשים ולהיתקל בעמידות לכימותרפיה. הבנת שרשרת האירועים הזו מצביעה על דרכים חדשות להאט או לחסום את פיזור סרטן הקיבה.
שותפות מסוכנת בגידולי הקיבה
החוקרים התחילו בהשוואת דגימות סרטן קיבה לרקמה בריאה סמוכה מ-100 מטופלים, וכן בניתוח מאגרי גנים ציבוריים נרחבים. הם מצאו כי TRIM29, חלבון שהיה מקושר בעבר לוויסות חיסוני ולסוגי סרטן אחרים, היה גבוה באופן קבוע בתאי הגידול. מטופלים שלגידוליהם היה ריכוז גבוה יותר של TRIM29 היו בעלי סבירות גבוהה יותר לנוכחות סרטן בבלוטות הלימפה ובכלי הדם ולתוחלת חיים נמוכה יותר. הדפוסים הללו מצביעים על כך ש-TRIM29 אינו רק קיים, אלא מעורב באופן פעיל בהפיכת סרטן הקיבה לאגרסיבי יותר.
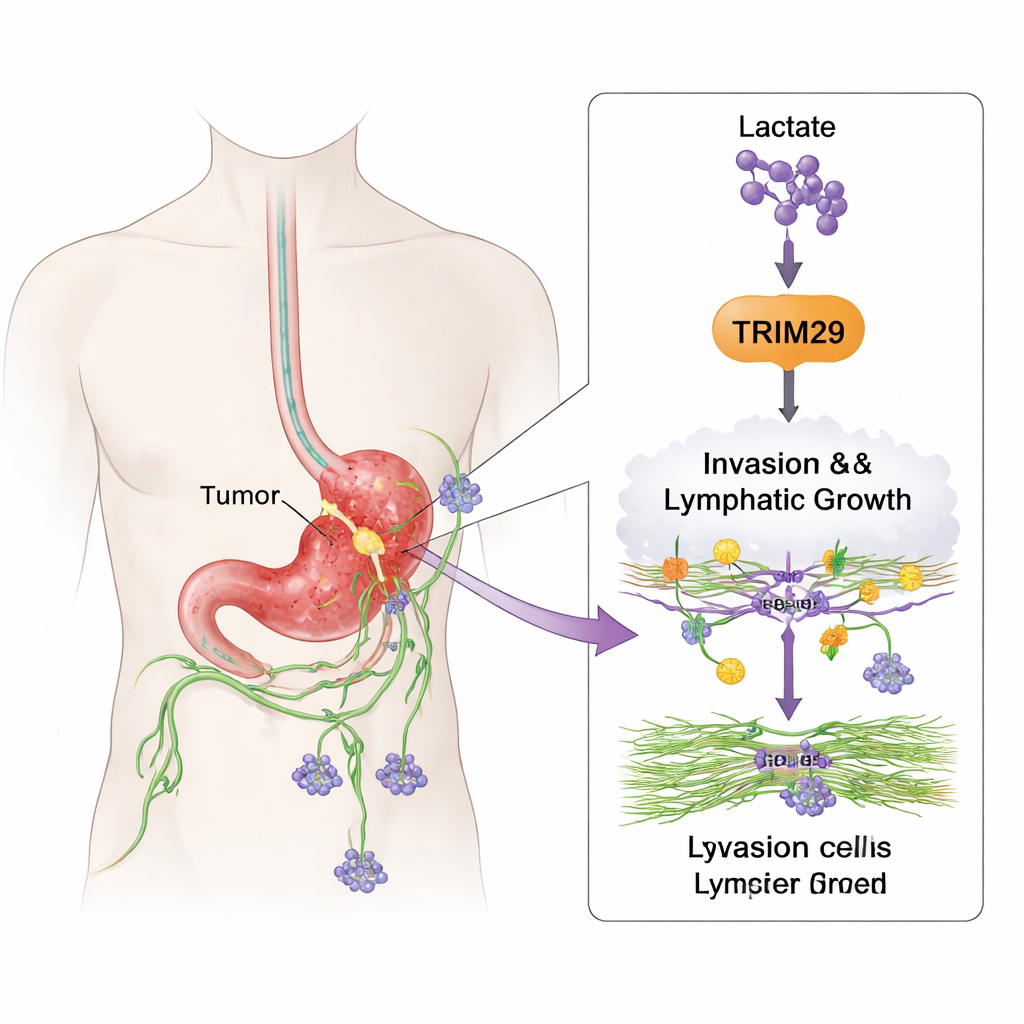
כיצד התאים הסרטניים לומדים לנדוד
כדי לבדוק מה TRIM29 עושה בפועל, הקבוצה שינתה את רמותיו בקווי תאי סרטן קיבה. כאשר הורידו את TRIM29, התאים הפכו לפחות ניידים ופחות מסוגלים לדחוף דרך ג'לים תלת־ממדיים המדמים רקמת גוף. העלאת רמת TRIM29 יצרה את ההשפעה ההפוכה והפכה את התאים לפולשניים יותר. החוקרים גם בחנו תאי אנדותל לימפטיים, התאים שמרפדים את כלי הלימפה. תאי סרטן עשירים ב-TRIM29 עודדו את תאי הכלי לנבוט וליצור מבנים צינוריים—אות המייצגת יצירת כלי לימפה חדשים (לימפנגיוגנזה). במודלים עכבריים, גידולים עם רמות גבוהות של TRIM29 יצרו יותר גרורות בכבד ובבלוטות לימפה, בעוד שבגידולים בהם הושמט TRIM29 הייתה פחות התפשטות ופחות כלי לימפה.
מעבר מולקולרי: הגנה על רגולטור מרכזי
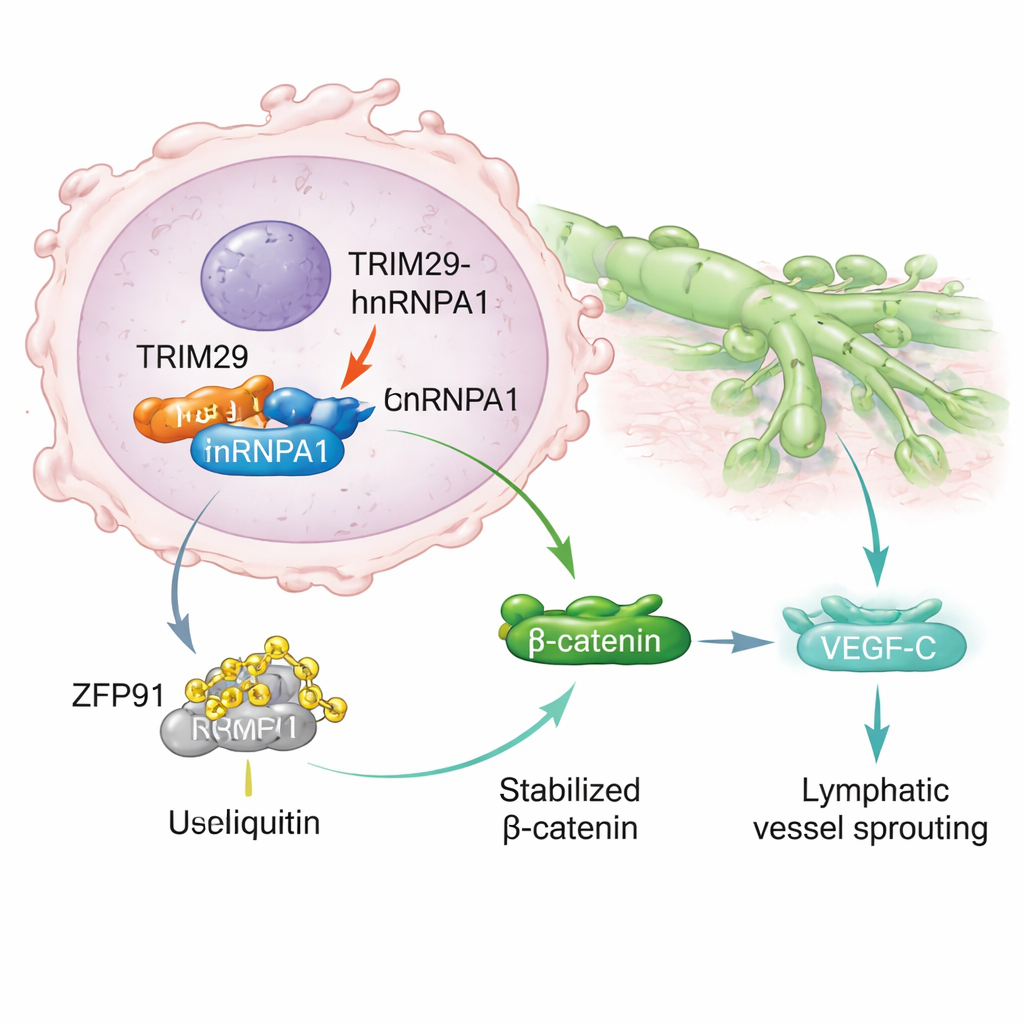
בחקירה עמוקה יותר גילו המדענים כי TRIM29 נקשר פיזית לחלבון אחר, hnRNPA1, הידוע כמשפיע על עיבוד גנים ומקושר לפיזור סרטן. באופן רגיל, hnRNPA1 עלול להיות מסומן להריסה על ידי חלבון אחר—אנזים בשם ZFP91—באמצעות מערכת הפינוי התאית. TRIM29 מפריע לתהליך זה על ידי תחרות על קשירה ל-hnRNPA1 מול ZFP91. כאשר TRIM29 רב, הוא מגן על hnRNPA1 מפני הסימון והפירוק. כתוצאה מכך, hnRNPA1 יציב יותר ומצטבר בתאי הסרטן, ומניע שרשרת של אותות שמסתיימת בהפעלת מסלול Wnt/β-catenin, מניע ידוע של גדילה ותנועתיות של הגידול. הדבר מעלה גם את הייצור של VEGF‑C, מולקולה שמעודדת יצירת כלי לימפה חדשים, ובכך מספקת לתאים הסרטניים "דרכים" נוספות להימלטות.
הזנה של הסרטן על-ידי לקטאט
המחקר מקשר גם את ההתנהגות הפולשנית למבנה האופן שבו הגידולים מעבדים סוכר. גידולים הגדלים במהירות מסתמכים לעתים קרובות על מטבוליזם שמייצר כמויות גדולות של לקטאט, תוצר לוואי שנחשב בעבר לפסולת בלבד. כאן מראים המחברים שלקטאט יכול לשנות כימית חלבוני היסטון שעוזרים לארוז DNA, במיוחד באתר הקרוי H3K9. ל"לַקטילציה" זו יש תפקיד כמתג הפעלה לגֵן TRIM29, ומגבירה את פעילותו. כאשר הורידו את ייצור הלקטאט בעזרת תרופות מטבוליות, רמות ה-TRIM29 ירדו; כאשר העלו את הלקטאט, ה-TRIM29 עלה. רקמות סרטן קיבה של מטופלים הציגו רמות גבוהות יותר של לקטילציה ב-H3K9, שקשור לרמות גבוהות יותר של TRIM29, יותר פיזור לבלוטות לימפה ותוחלת חיים ירודה יותר. במהותו, המטבוליזם השונה של הגידול מסייע לכתיבת תכנית גנטית אגרסיבית יותר.
דרכים חדשות לחזק כימותרפיה
כלי לימפה עושים יותר מלשאת תאים סרטניים; הם גם יכולים לנקז תרופות כימותרפיות מהגידולים. באמצעות השתלות גידול מטופלים שגדלו בעכברים, החוקרים בדקו האם חסימת TRIM29 וגדילת כלי הלימפה יכולה לשפר את ההשפעה של 5‑פלואורוציל (5‑FU), תרופת הסטנדרט בסרטן הקיבה. עיכוב TRIM29 או חסימת לימפנגיוגנזה כל אחת לחוד הגבירה את יעילות ה-5‑FU בצמצום הגידולים ובהפחתת חלוקת תאים. שילוב שתי האסטרטגיות נתן את התגובה החזקה ביותר, ומרמז על דרך פוטנציאלית להתגבר על חלק מעמידויות התרופות במצב מתקדם.
מה זה משמעותי עבור מטופלים
עבודה זו מציירת תמונה שלב-אחר-שלב: גידולי הקיבה מייצרים לקטאט עודף, שמפעיל את TRIM29; TRIM29 מגן על hnRNPA1, מייצב מסלול צמיחה ומגביר יצירת כלי לימפה והתפשטות לבלוטות. מבחינה קלינית, רמות גבוהות של TRIM29 וסימני לקטילציה קשורים מסמנים מטופלים בסיכון גבוה למחלה אגרסיבית. בעתיד, תרופות שמפחיתות איתות לקטאט, חוסמות את TRIM29 או מונעות יצירת כלי לימפה עשויות להיות משולבות עם כימותרפיה קיימת כדי למנוע התפשטות סרטן הקיבה ולשפר את יעילות הטיפול.
ציטוט: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
מילות מפתח: גרורות בסרטן הקיבה, TRIM29, לקטאט ולַקטילציה, יצירת כלי לימפה חדשים, מסלול Wnt בטא-קטנין