Clear Sky Science · he
CD36 מעלה את רגישות תאי סרטן חלבון שלילי משולש לפירוטוזה מושרת על‑ידי חומצת הפלמיטית
מדוע השומן סביב הגידולים יכול להיות גם ידיד וגם אויב
גידולי שד מתפתחים ברקמה שעשירה באופן טבעי בשומן, וידוע שתאי הסרטן "מניזים" מחומצות שומן באזור. המחקר הזה בוחן תפנית מפתיעה: בתנאים המתאימים, אחת מהשומנים השכיחים בגוף, חומצת הפלמיטית, יכולה למעשה לסייע בהרג צורה תוקפנית במיוחד של סרטן השד על‑ידי איתחול סוג מיוחד של מוות תאי. הבנת המנגנון עשויה להצביע על טיפולים חדשים עבור מטופלים שיש להם כיום מעט אפשרויות.
סרטן שד קשה לטיפול תחת המיקרוסקופ
סרטן שד שלילי משולש (TNBC) חסר את רצפטורים ההורמונליים וגורמי הגדילה שרבים מהתרופות המודרניות מכוונות אליהם, מה שהופך אותו לאחד מסוגי סרטן השד הקשים ביותר לטיפול. גידולים אלה חיים במגע צמוד עם תאי שומן שמשחררים כמויות גדולות של חומצות שומן, כולל השומן הרווי חומצת הפלמיטית. החוקרים רצו לדעת האם חומצת הפלמיטית פשוט מזינה את הגידול, או שייתכן שהיא גם יוצרת נקודת תורפה שאפשר לנצל להריגת תאי הסרטן.
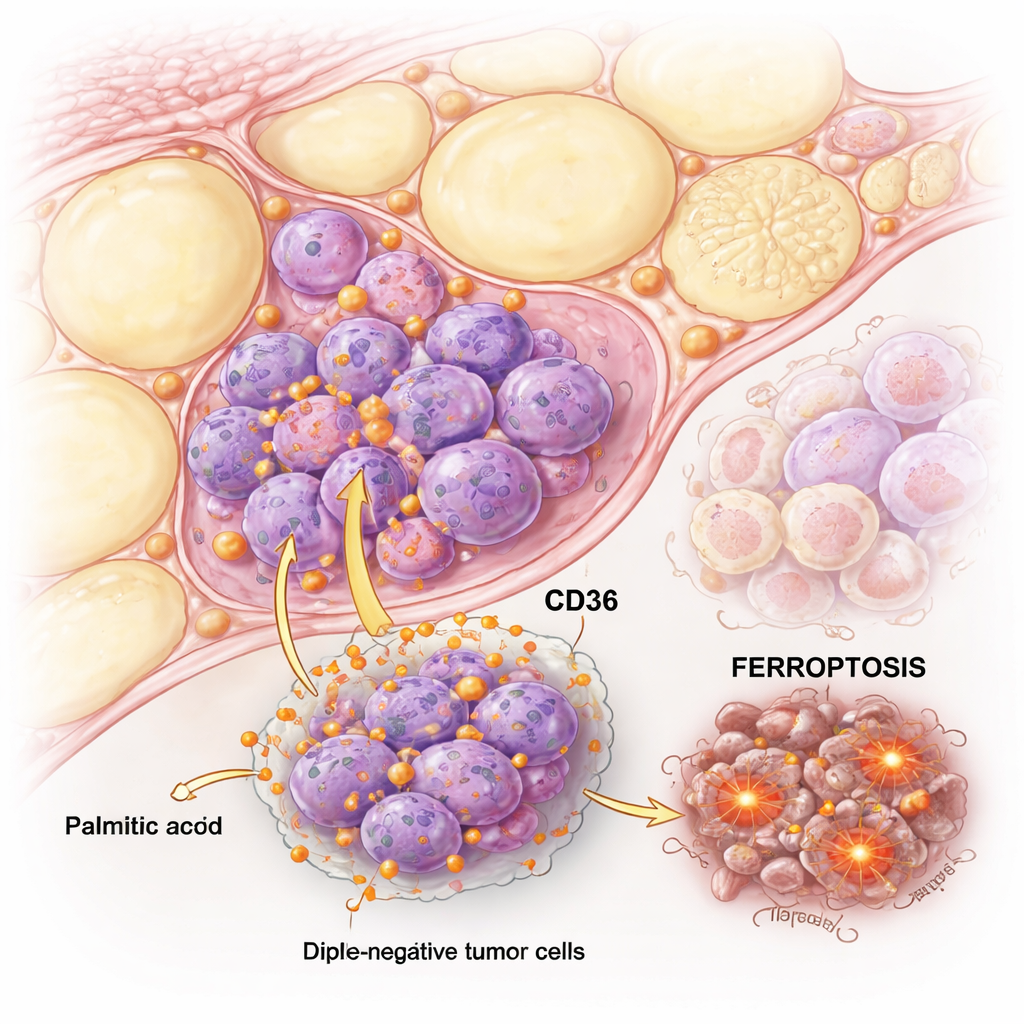
כשחומצת הפלמיטית דוחפת את תאי הסרטן אל הקצה
הצוות השווה בין תאי TNBC לתאי סרטן שד "לומינליים" הרגישים להורמונים וחשף אותם לכמויות עולה של חומצת פלמיטית. שתי סוגי התאים נפגעו במינונים גבוהים, אך תאי ה‑TNBC היו רגישים בהרבה. בדיקות מפורטות הראו שבתאים הלומינליים חומצת הפלמיטית עוררה בעיקר אפופטוזה קלאסית, צורה מסודרת של מוות תאי. בתאי ה‑TNBC, לעומת זאת, חומצת הפלמיטית הפעילה גם אפופטוזה וגם מסלול פחות מוכר שנקרא פירוטוזה, התלוי בברזל ובהרס שומני ממברנת התא.
מעבר של חומצות שומן בשם CD36
כדי להבין מדוע תאי ה‑TNBC הגיבו באופן כה שונה, החוקרים מיקדו את תשומת ליבם ב‑CD36, חלבון על פני התא הפועל כמעין מעבר לחומצות שומן ארוכות שרשרת. תאי ה‑TNBC נשאו באופן טבעי רמות גבוהות בהרבה של CD36 מאשר תאים לומינליים, וחשיפה לחומצת הפלמיטית העלתה עוד יותר את רמות ה‑CD36. משמעות הדבר הייתה שתאי ה‑TNBC סיננו פנימה יותר חומצת פלמיטית, צברו יותר ליפידים פגומים, ייצרו יותר חמצון ריאקטיבי במיטוכונדריה והצטברו יותר יוני ברזל חופשיים בתוך התא — כל אלה אותות מרכזיים של פירוטוזה. כאשר חסמו את CD36 בעזרת תרופה, או הקטינו אותו באמצעות כלים גנטיים, הפירוטוזה המושרת על‑ידי חומצת הפלמיטית ירדה בחדות.
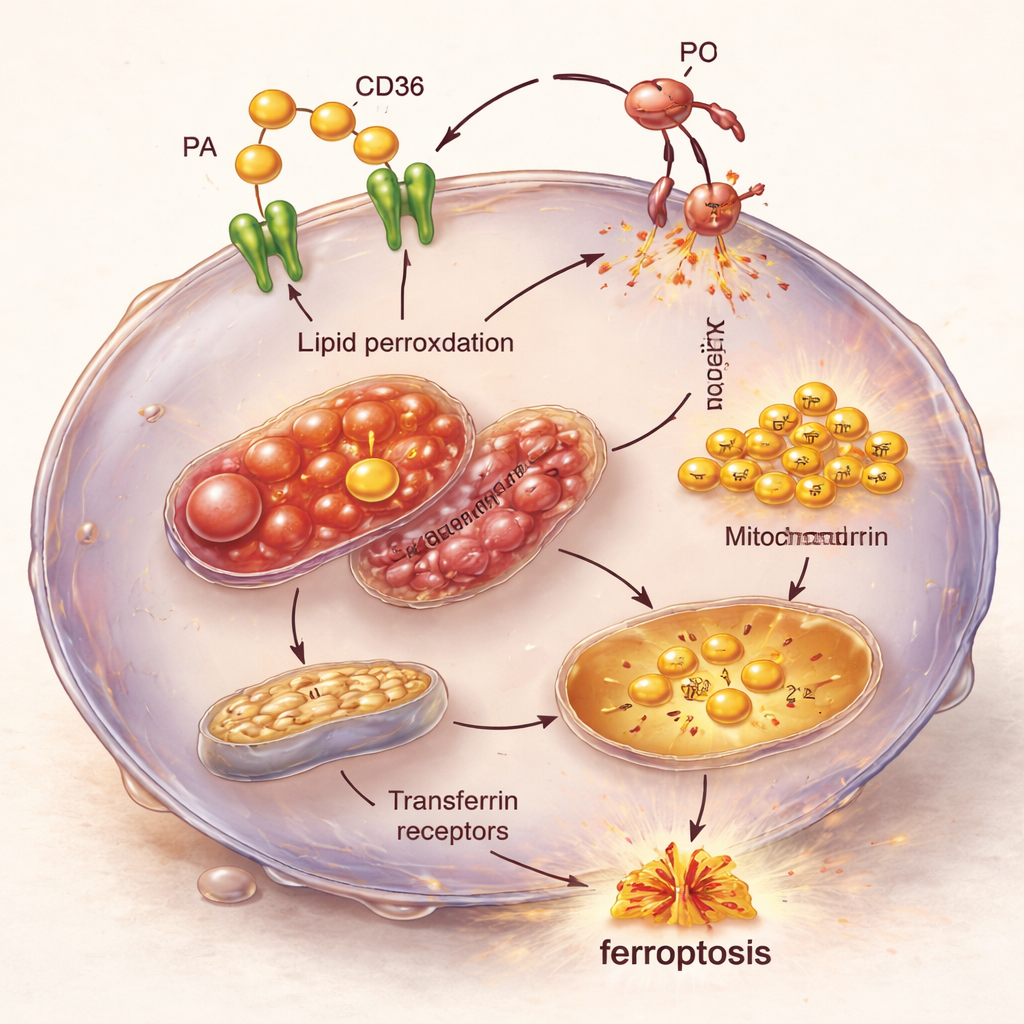
מקדחים פנימה את תגובת השרשרת בתוך התא
מיקרוסקופיה וניתוחי פעילות גנים חשפו את תגובת השרשרת הפנימית שמאחורי נקודת התורפה הזו. תאי TNBC שהוצפו בחומצת פלמיטית וב‑CD36 הראו מיטוכונדריות נפוחות ונזק מבני, ורמות ברזל עולות שהובאו דרך רצפטורי הטרנספרין. בו‑בזמן, גנים שמעודדים פירוטוזה הופעלו, בעוד שגנים שמגינים בדרך כלל מפני צורה זו של מוות תאי כובו. התוצאה היא סופה מושלמת: עומס שומנים נכנס פנימה, יותר ברזל זמין להנעת תגובות כימיות, והגנות מוחלשות נגד נזק לליפידים בממברנה — כל אלה דוחפים את תאי ה‑TNBC אל פירוטוזה.
אילו מטופלים עשויים להרוויח ביותר?
הסרטן אינו אחיד, גם בתוך TNBC. באמצעות דגימות גידול שגודלו בעכברים ומאגרי נתונים רחבים של מטופלים, המחברים מצאו שרמות CD36 היו גבוהות במיוחד בתת‑סוג TNBC מסוים שנקרא רצפטור האנדרוגן לומינלי (LAR), שכבר נצפה כרגיש יותר לפירוטוזה. תת‑סוגים אחרים של TNBC עם קליטה גבוהה של ברזל נטו גם הם להציג רמות CD36 מוגברות. דפוס זה מרמז ש‑CD36 יכול לשמש כסמן לזיהוי מטופלים שהגידולים שלהם מוכנים באופן טבעי לטיפולים המבוססים על פירוטוזה.
להפוך שומן שכיח לבעל ברית טיפולי
במילים פשוטות, עבודה זו מראה ששומן תזונתי וגופני נפוץ, חומצת הפלמיטית, יכול לסייע בהרג תאי סרטן שד שליליים משולש מסוימים כאשר הם מבטאים רמות גבוהות של משנעת השומן CD36. על‑ידי גרימת עומס שומני, הצטברות ברזל ונזק לממברנות התאים, CD36 עושה את תאי הסרטן הללו פגיעים יותר לפירוטוזה — גורל הרסני שלא יצליחו להימנע ממנו. אם טיפולים עתידיים יצליחו להגביר באופן בטוח נתיב זה — או לשלבו עם תרופות שמחלישות עוד יותר את מנגנוני ההגנה של התאים — יתכן שרופאים יוכלו להפוך נקודת תורפה מטבולית זו לדרך חדשה ומדויקת יותר לתקוף חלק מהגידולים האגרסיביים ביותר של השד.
ציטוט: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
מילות מפתח: סרטן שד שלילי משולש, פירוטוזה, CD36, חומצת פלמיטית, מטבוליזם גידולי