Clear Sky Science · he
תאי כבד דיפלואידים עמידים לפגיעה כבדית בעקבות עודף אצטמינופן באמצעות דיכוי מסלול ה-JNK
מדוע חלק מהכבדות שורדות מינוני יתר טוב יותר
אצטמינופן (פאראצטמול) נמצא בארונות תרופות רבים, אך נטילה מופרזת שלו היא גורם מוביל לאי־ספיקת כבד פתאומית. המחקר הזה שואל שאלה מפתיעה בפשטותה אך עם השלכות רחבות: האם כל תאי הכבד מגיבים לאסון תרופתי באותה צורה? החוקרים מראים שסוג מסוים של תאי כבד, הנקראים הפטוציטים דיפלואידים, מפתיע ביכולתו לשרוד ולתקן נזק לאחר מינון יתר של אצטמינופן, בזכות דיכוי של מסלול סטרס פנימי.
שני סוגי תאי כבד, שתי גורלות שונות
הכבד יוצא דופן בכך שרוב תאי העבודה בו (הפטוציטים) נושאים ערכות כרומוזומים נוספות, מה שהופך אותם לפוליפלואידיים. אחוז קטן יותר נשאר דיפלואידי, עם שתי ערכות כרומוזומים בלבד כמו רוב התאים בגוף. מדענים ידעו שקבוצות אלה נבדלות באופן חלוקתן ושחזורן, אך תפקידיהן בפגיעות כתוצאה מתרופות לא היו ברורים. המחברים השתמשו בעכברים מהונדסים שנולדו עם כבד מועשר בתאים דיפלואידים אך תפקוד תקין באופן כללי, והשוו אותם לעכברים טיפוסיים שכבדיהם ברובם פוליפלואידיים. לשתי הקבוצות ניתן מינון נמוך ומינון גבוה של אצטמינופן כדי לעקוב אחרי תגובת הכבד לאורך זמן.
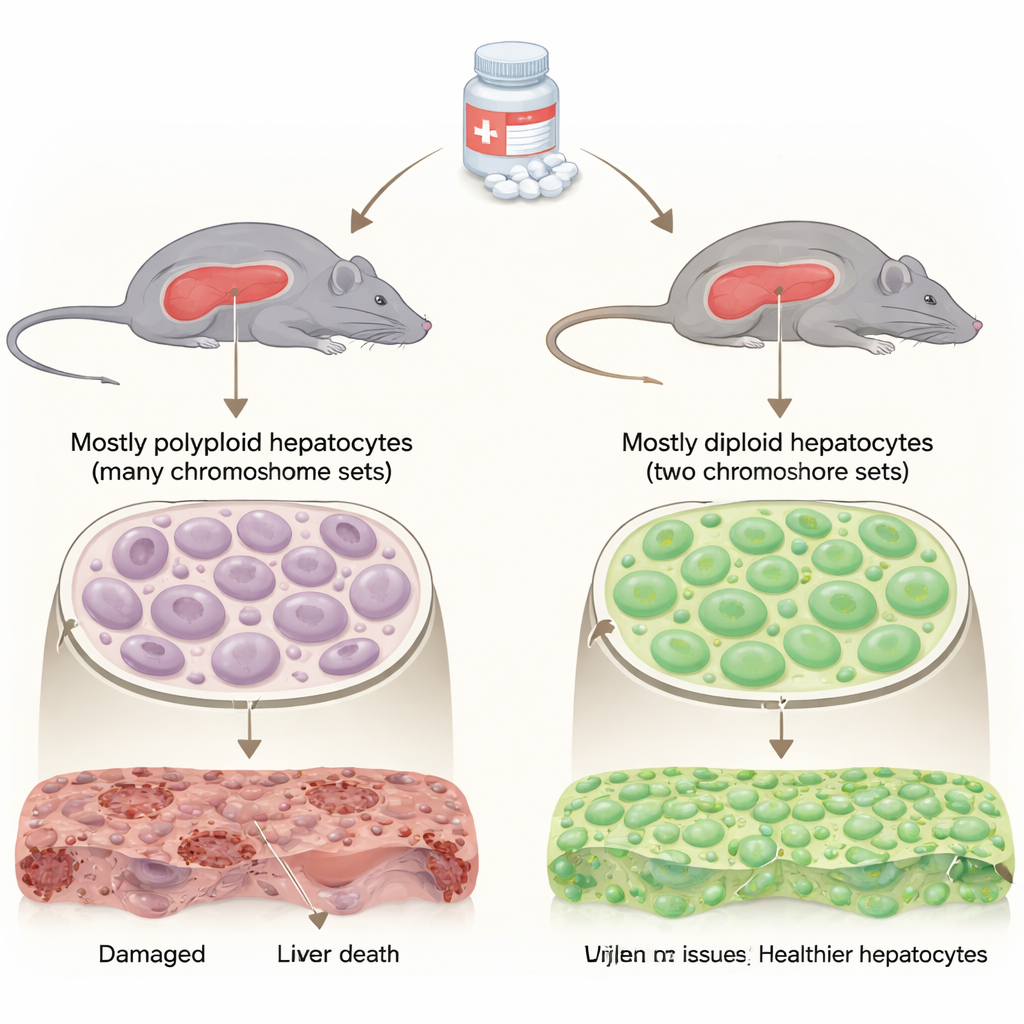
כבדות עשירות בדיפלואידים שורדות מינוני יתר ומשתקמות מהר יותר
כאשר העכברים קיבלו מינון "משחזר" של אצטמינופן, שתי הקבוצות הראו נזק לכבד, אך העכברים העשירים בדיפלואידים ביצעו הרבה יותר טוב. הייתה להם שרידות גבוהה יותר, רמות נמוכות יותר של אנזימי כבד בדם (סימן לנזק מופחת), ואזורים קטנים יותר של רקמת מתה ושברים ב-DNA תחת המיקרוסקופ. אפילו במינון חמור יותר — "שאינו משחזר" — שברוב המקרים גורם לפגיעה ממושכת ומוות, יותר ממחצית העכברים העשירים בדיפלואידים שרדו, לעומת פחות מאחד מתוך עשרה בקבוצת הביקורת. על אף ההגנה הזו, כבדות עתירות דיפלואידים לא נשארו פסיביות: הן הפעילו חלבוני חלוקה תאית מוקדם יותר, מה שמרמז שהן גם מתנגדות לנזק וגם מתחילות לבנות מחדש במהרה.
לא התרופה עצמה, אלא חיווט תגובת הלחץ
אפשרות ברורה הייתה שכבדות עשירות בדיפלואידים פשוט מטפלות באצטמינופן בצורה שונה. הצוות מדד אנזימים מרכזיים שממירים את התרופה לתוצר רעיל, רמות המולקולה המגינה גלוטטיון, וכמות התרופה הקשורה לחלבוני הכבד. כל המדדים היו דומים בין שני סוגי העכברים, כלומר שניהם ייצרו וטיפלו בכמות הרעילה זהה. ההבדל החשוב הופיע מאוחר יותר, באופן שבו התאים הגיבו לאותה רעל. בכבדות טיפוסיות, עשירות בפוליפלואידים, גנים וחלבונים המעורבים בלחץ תאי, נזק ל-DNA ופגיעה במיטוכונדריה הופרזו בעוצמה. בכבדות עשירות בדיפלואידים התגובות הללו היו מרוסנות ונפתרו מוקדם יותר, בעוד שגנים המקושרים לשחזור נדלקו קודם.
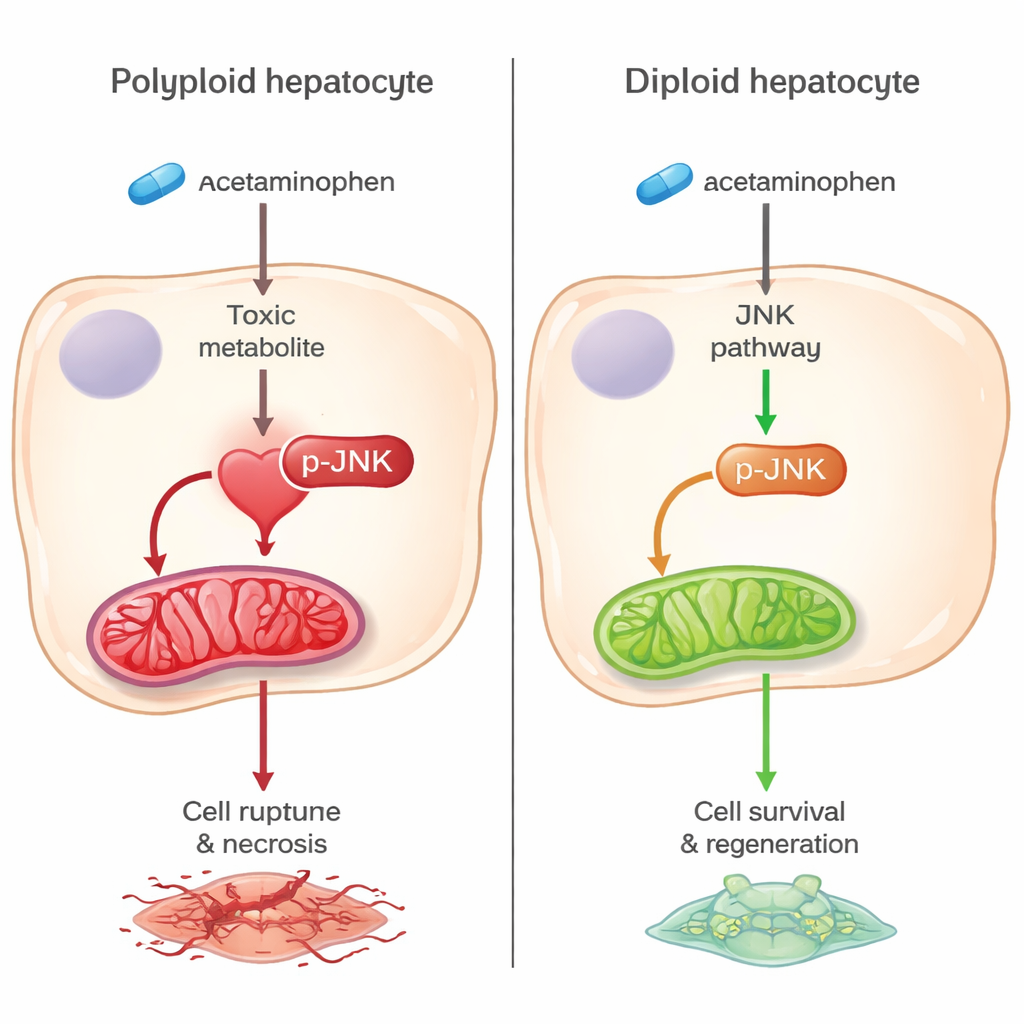
מסלול מוות שקט יותר מגן על תאים דיפלואידים
השחקן המרכזי בשוני הזה הוא מסלול איתות סטרס הידוע כ-JNK. בכבדות סטנדרטיות, התוצר הרעיל של האצטמינופן מפעיל אנזימים על־-זרם שמדליקים את JNK, אשר לאחר מכן נודד למיטוכונדריה — תחנות הכוח של התא — ומניע נזק חמצוני ומוות תאי. בכבדות עשירות בדיפלואידים, הפעלת האנזימים הללו ואת JNK עצמו הותאמה משמעותית כלפי מטה, וכמות JNK שהגיעה למיטוכונדריה הייתה נמוכה בהרבה. סימני לחץ חמצוני ושבירת מיטוכונדריה היו גם הם נמוכים יותר, מה שמצביע על כך שהתחנות האלה נשמרו טוב יותר. חשוב לציין שבמקרים בהם אותם גנים נמחקו רק בכבד בוגר בלי לשנות את הפלואידיות של התאים, לא נצפה אפקט מגן, מה שמצביע על כך שהשפע של תאים דיפלואידים — ולא שינוי גנטי בפני עצמו — הוא הגורם המרכזי.
מדוע סוג תא משנה בפגיעה כבדית אצל בני אדם
כדי לבדוק אם הדפוס תקף באופן רחב יותר, החוקרים חשפו תאי כבד עכבריים רגילים שגודלו במנות לתרבית לאצטמינופן. תאים בעלי ערכות כרומוזומים רבות (פוליפלואידיים גבוהים) מתו בקלות רבה יותר, בעוד שתאים דיפלואידים ובעלי פלואידיות נמוכה שרדו בשכיחות גבוהה יותר. יחד, הממצאים תומכים במודל שבו הפטוציטים הדיפלואידים הם "המגיבים הראשונים" של הכבד לפגיעה רעילה פתאומית: הם מדכאים מסלול מוות מרכזי, שומרים על המיטוכונדריה ונכנסים לשחזור במהירות. תאים פוליפלואידיים עשויים עדיין להיות מועילים בהקשרים אחרים, כמו הגנה מפני סרטן או התאמה לנזק כרוני ארוכת טווח. אבל במקרה של מינון יתר חד-פעמי, שיעור גבוה יותר של הפטוציטים הדיפלואידים עשוי להוות את ההבדל בין התאוששות לאי־ספיקת כבד.
ציטוט: Wilson, S.R., Delgado, E.R., Alencastro, F. et al. Diploid hepatocytes resist acetaminophen-induced liver injury through suppressed JNK signaling. Cell Death Dis 17, 203 (2026). https://doi.org/10.1038/s41419-026-08448-z
מילות מפתח: אצלטאמינופן במינון יתר, פגיעה בכבד, פלואידיות ההפטוציטים, אותות JNK, שחזור כבד