Clear Sky Science · he
טרנסגלוטמינאז 2 מחריף את הישרדות סרטן השחלות על‑ידי השבתה ישירה של GSK3β
מדוע מחקר זה חשוב לבריאות נשים
סרטן השחלות הוא אחד הגידולים הקטלניים ביותר בנשים, שכן הוא מאובחן בדרך כלל בשלב מאוחר ולעתים קרובות חוזר אף אחרי כימותרפיה אינטנסיבית. מחקר זה חושף כיצד חלבון מעט ידוע, טרנסגלוטמינאז 2 (TGase 2), מסייע לתאי סרטן השחלות לשרוד טיפול ולהתפשט בגוף. על ידי חשיפת ה״עזר הנסתר״ של הסרטן, העבודה מצביעה על דרכים חדשות לשפר את היעילות של תרופות קיימות ולעצור או להאט גרורות קטלניות.
נהג מוסתר בתוך גידולים אגרסיביים
רופאים כבר זמן רב מבחינים שרבים ממקרי סרטן השחלות מפתחים עמידות לכימותרפיה ומתפשטים במרחב הבטן. אחת הסיבות המרכזיות היא תהליך שנקרא המעבר האפיתליאלי‑מזנכימלי (EMT), שבו תאי סרטן משחררים את הקשרים ביניהם, נעשים ניידים יותר ומתנהגים יותר כ״נודדים״ פולשניים מאשר כתאים מאורגנים של רקמה. החוקרים מראים כי TGase 2, שנמצא ברמות נמוכות מאוד בשחלות נורמליות אך ברמות גבוהות בהרבה בגידולי שחלות, קשור בחוזקה לשינוי הזה. בלוח גדול של דגימות אנושיות, רמות TGase 2 עלו בהדרגה מגידולים בשלבים מוקדמים למחלה מתקדמת ומגרורתית, ושפע שלו התאמה באופן הדוק לפעילות של גנים רבים הקשורים ל‑EMT המבקרים תנועה תאית, גדילה ויצירת כלי דם. 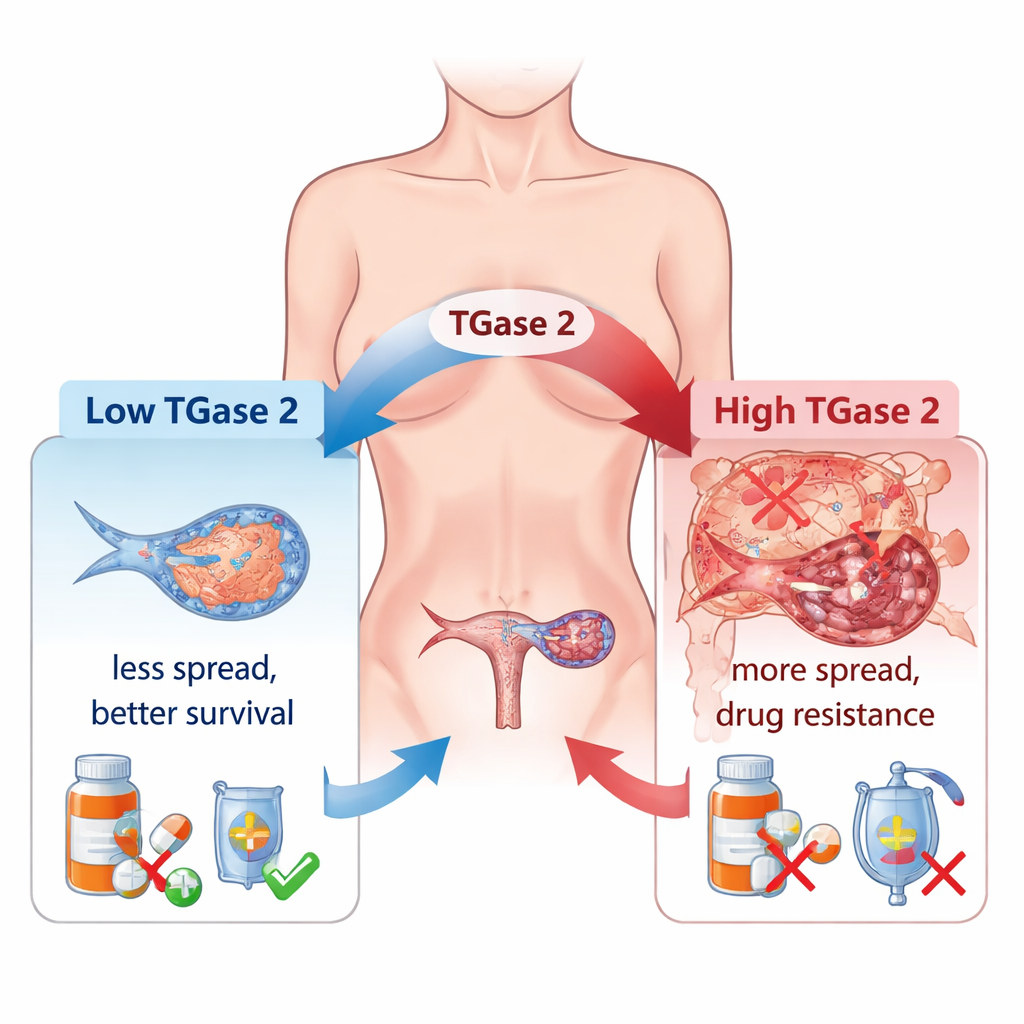
כיצד TGase 2 מכבה מתג ביטחון מרכזי
על מנת להבין מה TGase 2 עושה בתאי הסרטן, החוקרים התמקדו ביחסו לחלבון אחר, GSK3β. במצב בריא, GSK3β פועל כבלם על פלישה: הוא שומר על רמות נמוכות של מולקולת איתות שנקראת β‑catenin, מה שמייקר את ההגבלה על גנים שמניעים EMT. הצוות גילה ש‑TGase 2 נקשר פיזית ל‑GSK3β ומחליש הן את פעילותו והן מסייע בכיוונו להרס דרך מערכת המיחזור התאית, נתיב שנקרא אוטופגיה. כשה‑TGase 2 בשפע, תאי סרטן השחלות נדדו בקלות רבה יותר והציגו רמות גבוהות של סמני EMT קלאסיים כגון פיברונקטין, וימנטין ו‑β‑catenin. כאשר החוקרים הפחיתו את TGase 2 באמצעות כלים גנטיים, המאפיינים הפולשניים ירדו והאותות של β‑catenin הושתקו — מה שמראה ש‑TGase 2 מכבה מתג בטיחות קריטי נגד גרורות.
מתאי סרטן לחיות חיות
הצוות שאל בהמשך האם חסימת TGase 2 אכן יכולה להאט את הסרטן בחיות ניסוי. הם מהנדסים תאי סרטן שחלות חסרי גן TGase 2 והשתילו אותם בעכברים. בהשוואה לעכברים שקיבלו תאים סרטניים רגילים, בעלי החיים שקיבלו תאים חסרי TGase 2 פיתחו נטל גידולי קטן יותר וחיו זמן רב יותר. במודל נפרד המדמה התפשטות דרך זרם הדם, עכברים שהוזרקו בתאים חסרי TGase 2 פיתחו הרבה פחות וקטנים בהרבה גרורות ריאתיות. באופן חשוב, מאגרי הגרורות הללו הראו רמות גבוהות יותר של GSK3β, תומך ברעיון שהסרת TGase 2 משחזרת את הבלם הטבעי על הפלישה ועוזרת להכיל את המחלה.
הפיכת רמז מעבדה לאסטרטגיית תרופה
מכיוון שמחיקה גנטית אינה מעשית בחולים, החוקרים בדקו מולקולה קטנה בשם סטרפטוניגרין, שמוכרת בעבר כקשורה לקצה של TGase 2 המשמש לקשירת חלבונים אחרים. הם מצאו שסטרפטוניגרין יכול להפריע לאינטראקציה בין TGase 2 ל‑GSK3β בתאים, להפחית את הקוהורלוקליזציה שלהם ולהגבול תנועתיות תאי סרטן. במודלים עכבריים של סרטן השחלות, טיפול אוראלי בסטרפטוניגרין האט את גדילת הגידול, הקטין נגעים גרורתיים והאריך את ההישרדות. הממצא הבולט ביותר: כאשר סטרפטוניגרין שולב עם כימותרפיה סטנדרטית כגון ציספטין או פאצ'יטל, העכברים חיו שבועות יותר מאשר בכימותרפיה בלבד. כימותרפיה לבדה נטתה להעלות רמות TGase 2 ולהקטין GSK3β, דוחפת בעקיפין את התאים לעבר EMT, אך הוספת החוסם של TGase 2 הפכה מגמה זו ומיתנה את הניידות החדשה של התאים. 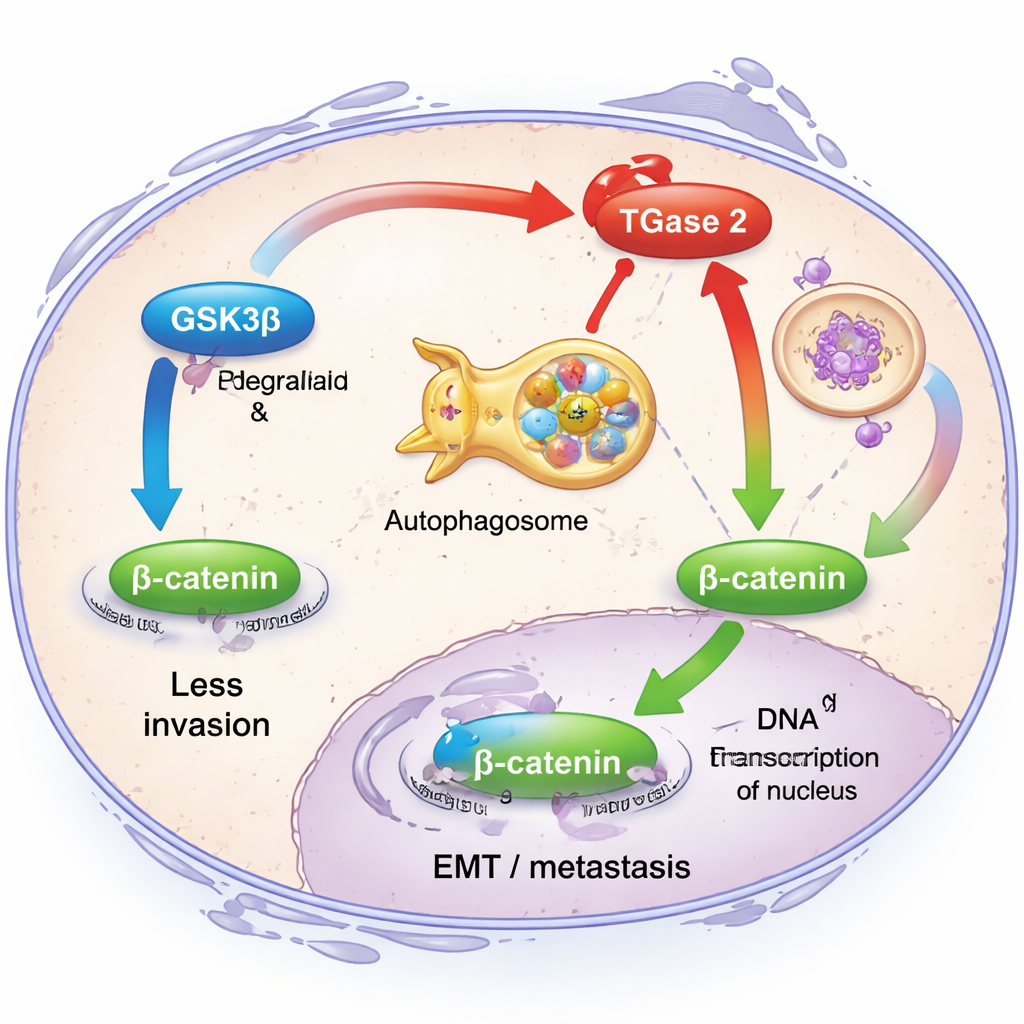
מה המשמעות לטיפולים עתידיים
עבור הקורא שאינו מומחה, המסר המרכזי הוא שתאי סרטן השחלות מנצלים את TGase 2 כדי לכבות בלם אנטי‑גרורתי משולב ולהתמודד עם סופת הכימותרפיה. על‑ידי השבתה ישירה של GSK3β וייצוב β‑catenin, TGase 2 מסייע לגידולים להפוך לפולשניים ועמידים לתרופות. עבודה זו מרמזת שתרופות המכוונות לאזור ה‑N‑טרמינלי של TGase 2 — כמו סטרפטוניגרין או תרכובות עתידיות ובטוחות יותר המודלות עליו — עשויות לשפר את יעילות הכימותרפיה הקיימת, להפחית את הסיכון לשחזור ולשפר הישרדות. בפשטות, מטרה ב‑TGase 2 עשויה לחסום ״נתיב הבריחה״ של הסרטן, לשמור על רגישות גבוהה יותר לטיפול ולהפחית את היכולת להתפשט של גידולי השחלות.
ציטוט: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
מילות מפתח: סרטן השחלות, עמידות לתרופות, תסתיידות (הסתיידות גרורות), השתנות אפיתליאלית־מזנכימלית, טיפול ממוקד