Clear Sky Science · he
ניתוח מולטי-אומי רזולוציית זמן של חשיפה לפאקלטקסל בעצבונים תחושתיים נגזרים מ‑iPSC אנושיות חושף מנגנונים של נוירופתיה היקפית המושרת על‑ידי כימותרפיה
מדוע חלק מתרופות הסרטן פוגעות בעצבים
הכימותרפיה עזרה למיליוני אנשים לשרוד סרטן, אך רבים מהחולים משלמים מחיר חבוי: חודשים או שנים של כאב צורב, דקירות והשתתקות בידיים ובכפות הרגליים. המחקר שואל שאלה פשוטה אך חשובה: מה בדיוק עושה התרופה רחבת‑השימוש פאקלטקסל לתאי עצב תחושתיים אנושיים, והאם הבנת השינויים האלה יכולה להצביע על דרכים טובות יותר למניעה וטיפול בנזק העצבי?
מתאי מטופלים לעצבים חשים שגודלו במעבדה
במקום להסתמך על ניסויים בבעלי חיים, החוקרים התחילו מתאים מחמישה תורמים אנושיים, כולל מטופלות בסרטן השד שקיבלו פאקלטקסל. הם תכנתו מחדש את התאים לתאי גזע פלוריפוטנטיים מושרים ואז הובילו אותם להתמיין לתאי עצב תחושתיים — אותו סוג תא שמעבירים תחושות מגע וכאב מהעור לעמוד השדרה. העצבונים שגודלו במעבדה יצרו סיבים ארוכים ועדינים והפגינו פעילות חשמלית הדומה לזו של עצבי כאב אמיתיים בגוף. הצוות חשף אותם למינונים גוברים של פאקלטקסל, המדמים רמות התרופה שנצפות בחולים, ועקב אחר בריאות התאים במשך מספר ימים. בריכוזים נמוכים העצבונים התמודדו היטב, אך במינון הרלוונטי קלינית (100 ננומולר) הישרדותם החלה לרדת אחרי כיממה־יומיים, וסימון תחילת נזק עצבי רעיל.
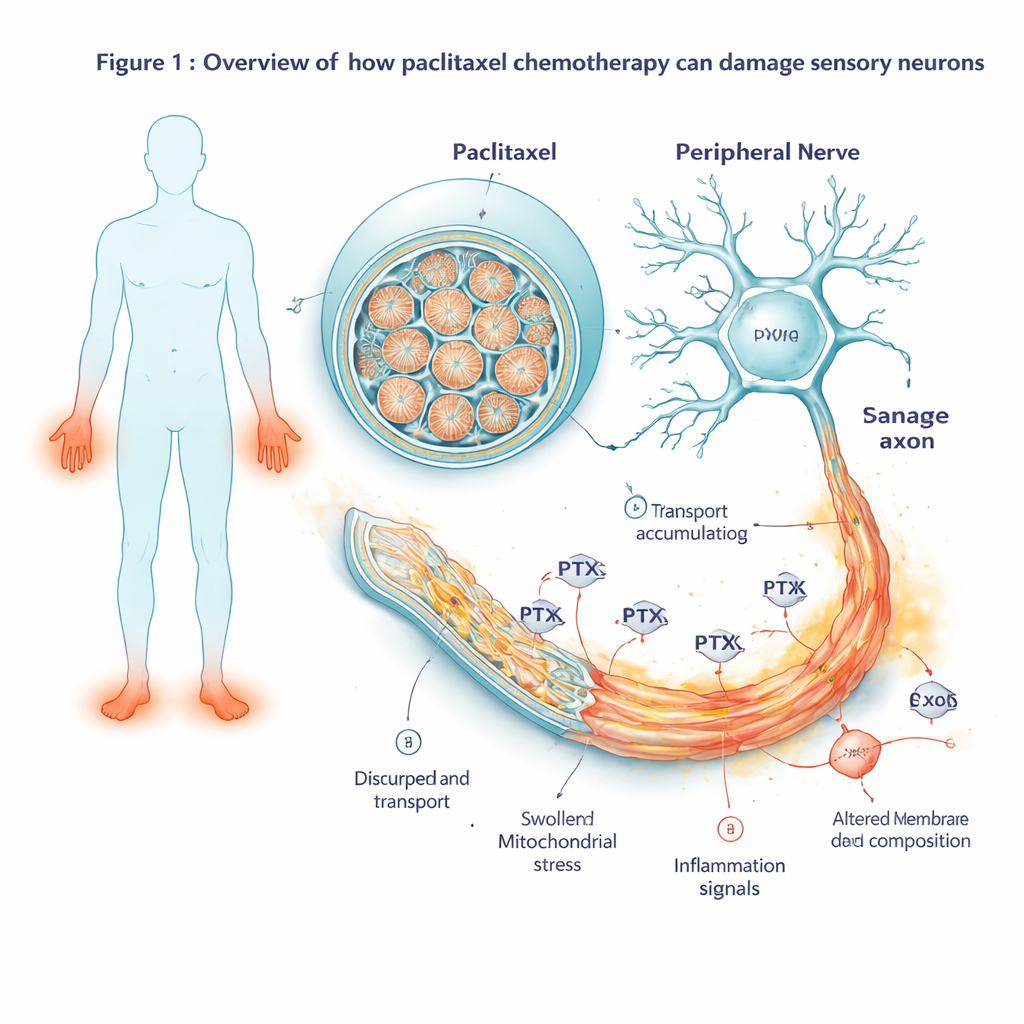
מעקב אחר שינוי פעילות הגנים לאורך זמן
כדי לראות כיצד התאים הגיבו לפני שהחלו להידרדר באופן ניכר, המדענים מדדו אילו גנים נדלקו או כבו בנקודות זמן רבות, משעתיים לאחר חשיפה לתרופה ועד כמה ימים אחרי שטופס התרופה הוסר. בתחילה נצפתה הפעלה של תכנית לחץ תאית קלאסית שמרכזת סביב הגן JUN. ככל שהחשיפה נמשכה, אות הלחץ התרחב לקסקדה של 'השמדת עצמי': גנים שמניעים תהליכים של מוות מתוכנת נדלקו בעוצמה, בעוד שותפים מגן הוצפו. במקביל, גנים המקושרים לדלקת ולסיגנלינג של כאב הפכו פעילים יותר. העצבונים החלו לייצר יותר מוליכי דלקת, פפטידים הקשורים לכאב וקולטנים שהופכים תאים לרגישים יותר לגירויים מזיקים — שינויים המשקפים את מה שנראה בהפרעות עצביות כואבות.
מבט מעמיק על חלבונים ושומנים בתוך העצבונים
מכיוון שגנים הם רק שרטוטים, הצוות בחן גם את החלבונים המוצאים בפועל בעצבונים ואת הרכב הליפידים (השומנים) שלהם. לאחר 48 שעות של חשיפה לפאקלטקסל, רבים מאותות הלחץ והדלקת שנמצאו ברמת ה‑RNA הופיעו גם כרמת חלבון מוגברת, מה שאישר שהעצבונים מבצעים את התכניות המזיקות האלה. באופן בולט, חלבונים הנדרשים לתעבורה אקסונלית — המנועים המולקולריים והדוממים שמעבירים מטענים לאורך הסיבים העצביים הארוכים — ירדו מאד. זאת כללה קינזינים וחלבונים רגולטוריים שמשמרים את היציבות של משטחי המיקרוטובולים. ברמת השומנים נצפה ירידה בבוני יסוד חשובים ליצירת כולסטרול וליפידים ממברנליים, לצד עלייה בשומנים מאוחסנים שנקראים טריאצילגליצרולים. יחד, השינויים האלה מרמזים שפאקלטקסל לא רק מפעיל מסלולי מוות תאי אלא גם מחליש את המבנה הפיזי ואת מאזן האנרגיה של הסיבים העצביים.
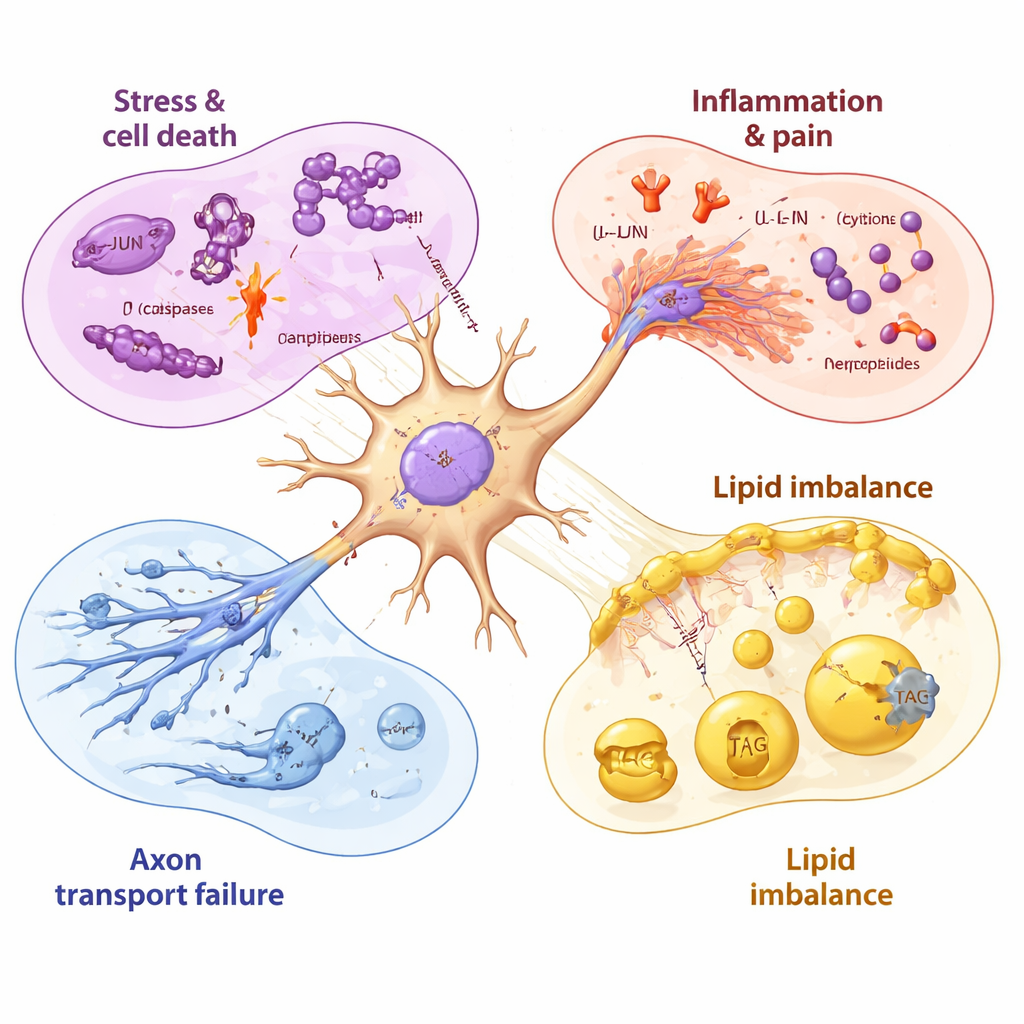
ציר זמן של פגיעה עצבית והתאוששות חלקית
על ידי דגימה מהעצבונים לפני, במהלך ולאחר חשיפה לתרופה, החוקרים יכלו לסדר את האירועים על פי הזמן. גנים מיטוכונדריאליים (קשורים לאנרגיה) הופרעו בתוך שעות, ואחריהם גן הלחץ JUN, ואז הפעלה חזקה יותר של תכניות מוות ותהליכי דלקת כאשר היכולת לשרוד החלה לרדת. גם לאחר הסרת הפאקלטקסל, אותות מזיקים רבים נשארו מורמים למשך ימים, בעוד שהגנים הדרושים לייצור ליפידים ממברנליים בריאים המשיכו לרדת. מולקולות שעלו באיחור, כגון משאבת השלכה של תרופות שיכולה לפלוט פאקלטקסל וכמה גורמי גדילה, רמזו שהעצבונים מנסים להגן ולתקן את עצמם — אך תגובות אלה נראו יחסית איטיות וחסרות שלמות בהשוואה לדחיפה המהירה והראשונית לעבר הנזק.
מה משמעות הדבר עבור מטופלים החיים עם כאב עצבי
לאדם מן השורה, המסר הוא שפאקלטקסל פוגע בעצבונים התחושתיים דרך סדרה מתואמת של מכות: הוא מייבב את מערכות האנרגיה שלהם, מפעיל מתגים גנטיים לכיוון מוות תאי, מעורר דלקת וסיגנלינג של כאב, משבש את "הכבישים" הפנימיים לתעבורה בתוך הסיבים העצביים ומשנה את השומנים ששומרים על יציבות ממברנות העצבים. על ידי מיפוי שינויים אלה בעצבונים נגזרים מאדם ברזולוציה גבוהה, המחקר מדגיש מטרות קונקרטיות הניתנות לטיפול — כגון רגולטורים ספציפיים של לחץ, קולטנים דלקתיים ואנזימים לייצור ליפידים — שאפשר לחסום או לתמוך בהם כדי להגן על העצבים מבלי להחליש את הטיפול בסרטן. אמנם טיפולים חדשים ידרשו בדיקות נוספות, עבודה זו מציעה מפת דרכים ברורה יותר למניעה או הקלה של נזק עצבי הנגרם על‑ידי כימותרפיה, ושיפור איכות החיים של שורדי סרטן.
ציטוט: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
מילות מפתח: נוירופתיה היקפית הנגרמת על‑ידי כימותרפיה, פאקלטקסל, תאי עצב תחושתיים, דלקת עצבית, ניוון אקסון